Când acizii carboxilici interacționează cu alcoolii (reacție de esterificare), esteri:
R1-COOH (acid) + R2-OH (alcool) ↔ R1-COOR2 (ester) + H2O
Această reacție este reversibilă. Produșii de reacție pot interacționa între ei pentru a forma substanțele inițiale - alcool și acid. Astfel, reacția esterilor cu apa - hidroliza esterului - este inversul reacției de esterificare. Echilibrul chimic, care se stabilește atunci când vitezele reacțiilor directe (esterificare) și inverse (hidroliză) sunt egale, poate fi deplasat către formarea eterului prin prezența substanțelor de eliminare a apei.
Esteri în natură și tehnologie
Esterii sunt distribuiți pe scară largă în natură și sunt utilizați în inginerie și în diverse industrii. Sunt buni solvenți ai substanțelor organice, densitatea lor este mai mică decât cea a apei și practic nu se dizolvă în ea. Astfel, esterii cu o greutate moleculară relativ mică sunt lichide inflamabile cu puncte de fierbere scăzute și miros de diferite fructe. Sunt folosiți ca solvenți pentru lacuri și vopsele, produse aromatizante din industria alimentară. De exemplu, esterul metilic al acidului butiric are miros de mere, alcoolul etilic al acestui acid are miros de ananas, esterul izobutilic al acidului acetic are miros de banane:
C3H7-COO-CH3 (ester metilic al acidului butiric);
C3H7-COO-C2H5 (ester etilic al acidului butiric);
CH3-COO-CH2-CH2 (ester izobutilic al acidului acetic)
Se numesc esterii acizilor carboxilici superiori și ai alcoolilor monobazici superiori ceară. Astfel, ceara de albine constă în principal din esterul acidului palmitic al alcoolului miricilic C 15 H 31 COOC 31 H 63; ceara de cachalot - spermaceti - un ester al aceluiasi acid palmitic si alcool cetilic C 15 H 31 COOC 16 H 33
Acum să vorbim despre cele complexe. Esterii sunt larg răspândiți în natură. A spune că esterii joacă un rol important în viața umană înseamnă a nu spune nimic. Le întâlnim atunci când mirosim o floare, care își datorează parfumul celor mai simpli esteri. Uleiul de floarea soarelui sau de măsline este, de asemenea, un ester, dar deja cu greutate moleculară mare - la fel ca grăsimile animale. Spălăm, spălăm și spălăm cu produse care sunt obținute printr-o reacție chimică de prelucrare a grăsimilor, adică esteri. De asemenea, sunt folosite în diverse domenii de producție: sunt folosite pentru a face medicamente, vopsele și lacuri, parfumuri, lubrifianți, polimeri, fibre sintetice și multe, multe altele.
Esterii sunt compuși organici pe bază de acizi organici carboxilici sau anorganici care conțin oxigen. Structura unei substanțe poate fi reprezentată ca o moleculă acidă în care atomul de H din hidroxil-OH este înlocuit cu un radical de hidrocarbură.
Esterii se obțin prin reacția unui acid și a unui alcool (reacție de esterificare).
Clasificare
 - Esteri de fructe - lichide cu miros fructat, molecula nu conține mai mult de opt atomi de carbon. Obținut din alcooli monohidroxilici și acizi carboxilici. Esterii cu miros floral se obțin folosind alcooli aromatici.
- Esteri de fructe - lichide cu miros fructat, molecula nu conține mai mult de opt atomi de carbon. Obținut din alcooli monohidroxilici și acizi carboxilici. Esterii cu miros floral se obțin folosind alcooli aromatici.
- Ceruri - substante solide, contin de la 15 la 45 de atomi de carbon intr-o molecula.
- Grasimi - contin 9-19 atomi de carbon intr-o molecula. Se obține din glicerol a (alcool trihidroxilic) și acizi carboxilici superiori. Grăsimile pot fi lichide (grăsimi vegetale, numite uleiuri) și solide (grăsimi animale).
- Esterii acizilor minerali din punct de vedere al proprietăților lor fizice pot fi, de asemenea, atât lichide uleioase (până la 8 atomi de carbon), cât și solide (de la nouă atomi de carbon).
Proprietăți
În condiții normale, esterii pot fi lichizi, incolori, cu miros fructat sau floral, sau solidi, plastici; de obicei inodor. Cu cât lanțul de hidrocarburi este mai lung, cu atât substanța este mai dură. Aproape insolubil în apă. Se dizolvă bine în solvenți organici. Inflamabil.
Ele reacţionează cu amoniacul formând amide; cu hidrogen (aceasta reacție transformă uleiurile vegetale lichide în margarine solide).
Ca rezultat al reacției de hidroliză, se descompun în alcool și acid. Hidroliza grăsimilor într-un mediu alcalin duce la formarea nu a acidului, ci a sării sale - săpun.
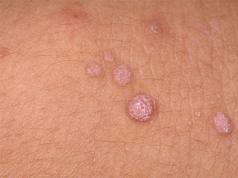
Esterii acizilor organici au toxicitate scăzută, au un efect narcotic asupra oamenilor și aparțin în principal clasei de pericol a 2-a și a 3-a. Unii reactivi în producție necesită utilizarea unei protecții speciale pentru ochi și căile respiratorii. Cu cât este mai lungă molecula de ester, cu atât este mai toxică. Esterii acizilor fosforici anorganici sunt otrăvitori.
Substanțele pot pătrunde în organism prin sistemul respirator și prin piele. Simptomele intoxicației acute sunt agitația și coordonarea afectată a mișcărilor, urmate de deprimarea sistemului nervos central. Expunerea regulată poate duce la boli ale ficatului, rinichilor, sistemului cardiovascular și tulburări ale numărului de sânge.
Aplicație
în sinteza organică.
- Pentru producerea de insecticide, erbicide, lubrifianți, impregnări pentru piele și hârtie, detergenți, glicerină, nitroglicerină, uleiuri sicante, vopsele în ulei, fibre și rășini sintetice, polimeri, plexiglas, plastifianți, reactivi pentru prepararea minereurilor.
- Ca aditiv la uleiurile de motor. 
- In sinteza parfumurilor de parfumerie, esentelor de fructe alimentare si parfumurilor cosmetice; medicamente, de exemplu, vitaminele A, E, B1, validol, unguente.
- Ca solventi pentru vopsele, lacuri, rasini, grasimi, uleiuri, celuloza, polimeri.
În sortimentul magazinului PrimeChemicalsGroup, puteți cumpăra esteri populari, inclusiv acetat de butil și Tween-80.
Acetat de butil
Folosit ca solvent; în industria parfumurilor pentru fabricarea parfumurilor; pentru tăbăcirea pielii; în produse farmaceutice – în procesul de fabricare a unor medicamente.
Twin-80
Este, de asemenea, polisorbat-80, monooleat de polioxietilen sorbitan (pe bază de sorbitol de ulei de măsline). Emulgator, solvent, lubrifiant industrial, modificator de vâscozitate, stabilizator de ulei esențial, surfactant neionic, umectant. Inclus în solvenți și fluide de tăiere. Este folosit pentru producerea de produse cosmetice, alimentare, casnice, agricole, tehnice. Are proprietatea unică de a transforma un amestec de apă și ulei într-o emulsie.
5 martie 2018Esterii sunt de obicei numiți compuși obținuți prin reacția de esterificare din acizii carboxilici. În acest caz, OH- este înlocuit din grupa carboxil cu radicalul alcoxi. Ca rezultat, se formează esteri, a căror formulă este în general scrisă ca R-COO-R.
Structura grupului ester
Polaritatea legăturilor chimice din moleculele de ester este similară cu polaritatea legăturilor din acizii carboxilici. Principala diferență este absența unui atom de hidrogen mobil, în locul căruia este plasat un reziduu de hidrocarbură. Cu toate acestea, centrul electrofil este situat pe atomul de carbon al grupului ester. Dar atomul de carbon al grupării alchil conectată la acesta este, de asemenea, polarizat pozitiv.
Electrofilia și, prin urmare, proprietățile chimice ale esterilor, sunt determinate de structura reziduului de hidrocarbură care a luat locul atomului de H în gruparea carboxil. Dacă radicalul de hidrocarbură formează un sistem conjugat cu atomul de oxigen, atunci reactivitatea crește semnificativ. Acest lucru se întâmplă, de exemplu, în esterii acrilici și vinilici.
Proprietăți fizice
Majoritatea esterilor sunt substanțe lichide sau cristaline cu o aromă plăcută. Punctul lor de fierbere este de obicei mai mic decât cel al acizilor carboxilici cu greutate moleculară similară. Acest lucru confirmă scăderea interacțiunilor intermoleculare, iar aceasta, la rândul său, se explică prin absența legăturilor de hidrogen între moleculele învecinate.
Cu toate acestea, la fel ca proprietățile chimice ale esterilor, cele fizice depind de caracteristicile structurale ale moleculei. Mai exact, pe tipul de alcool și acid carboxilic din care se formează. Pe această bază, esterii sunt împărțiți în trei grupuri principale:
- Esteri de fructe. Sunt formați din acizi carboxilici inferiori și aceiași alcooli monohidroxilici. Lichide cu mirosuri caracteristice plăcute floral-fructate.
- Ceară. Sunt derivați ai acizilor și alcoolilor superiori (număr de atomi de carbon de la 15 la 30) având fiecare câte o grupă funcțională. Acestea sunt substanțe plastice care se înmoaie ușor în mâini. Componenta principală a cerii de albine este palmitatul de miricil C 15 H 31 COOS 31 H 63 și esterul chinezesc al acidului cerotinic C 25 H 51 COOS 26 H 53. Sunt insolubile în apă, dar solubile în cloroform și benzen.
- Grasimi. Format din glicerol și acizi carboxilici medii și superiori. Grăsimile animale, de regulă, sunt solide în condiții normale, dar se topesc ușor când temperatura crește (unt, untură etc.). Grasimile vegetale se caracterizeaza printr-o stare lichida (uleiuri de in, masline, soia). Diferența fundamentală în structura acestor două grupe, care afectează diferențele în proprietățile fizice și chimice ale esterilor, este prezența sau absența legăturilor multiple în reziduul acid. Grăsimile animale sunt gliceride ale acizilor carboxilici nesaturați, iar grăsimile vegetale sunt acizi saturați.
Proprietăți chimice
Esterii reacţionează cu nucleofilii, rezultând substituirea grupării alcoxi şi acilarea (sau alchilarea) agentului nucleofil. Dacă există un atom de hidrogen α în formula structurală a esterului, atunci este posibilă condensarea esterului.
1. Hidroliză. Este posibilă hidroliza acidă și alcalină, care este reacția inversă de esterificare. În primul caz, hidroliza este reversibilă, iar acidul acționează ca un catalizator:
R-COO-R"+ H2O<―>R-COO-H + R"-OH
Hidroliza bazică este ireversibilă și se numește de obicei saponificare, iar sărurile de sodiu și potasiu ale acizilor grași carboxilici sunt numite săpunuri:
R-COO-R" + NaOH ―> R-COO-Na + R"-OH

2. Amonoliza. Amoniacul poate acționa ca un agent nucleofil:
R-COO-R"+ NH3-> R-CO-NH2 + R"-OH
3. Intereserificare. Această proprietate chimică a esterilor poate fi atribuită și metodelor de preparare a acestora. Sub acțiunea alcoolilor în prezența H + sau OH - este posibil să se înlocuiască radicalul de hidrocarbură combinat cu oxigen:
R-COO-R" + R""-OH ―> R-COO-R"" + R"-OH
4. Reducerea cu hidrogen duce la formarea de molecule a doi alcooli diferiți:
R-СО-OR "+ LiAlH 4 ―> R-СΗ 2 -ОH + R"OH
5. Arderea este o altă reacție tipică pentru esteri:
2CΗ 3 -COO-CΗ 3 + 7O 2 \u003d 6CO 2 + 6H 2 O
6. Hidrogenarea. Dacă există mai multe legături în lanțul de hidrocarburi al unei molecule de eter, atunci moleculele de hidrogen pot fi atașate de ele, ceea ce are loc în prezența platinei sau a altor catalizatori. Deci, de exemplu, este posibil să se obțină grăsimi solide hidrogenate (margarină) din uleiuri.

Utilizarea esterilor
Esterii și derivații lor sunt utilizați în diverse industrii. Multe dintre ele dizolvă bine diverși compuși organici, sunt utilizate în parfumerie și industria alimentară, pentru producerea de polimeri și fibre de poliester.
Acetat etilic. Este folosit ca solvent pentru nitroceluloză, acetat de celuloză și alți polimeri, pentru fabricarea și dizolvarea lacurilor. Datorită aromei sale plăcute, este folosit în industria alimentară și a parfumurilor.
Acetat de butil. Folosit și ca solvent, dar deja rășini poliesterice.
Acetat de vinil (CH3-COO-CH=CH2). Se folosește ca bază a unui polimer necesar în prepararea adezivilor, lacurilor, fibrelor sintetice și a peliculelor.
Eter malonic. Datorită proprietăților sale chimice speciale, acest ester este utilizat pe scară largă în sinteza chimică pentru a obține acizi carboxilici, compuși heterociclici, acizi aminocarboxilici.

ftalați. Esterii acidului ftalic sunt utilizați ca plastifianți pentru polimeri și cauciucuri sintetice, iar ftalatul de dioctil este, de asemenea, folosit ca repulsiv.
Acrilat de metil și metacrilat de metil. Polimerizare usor cu formarea de foi de sticla organica rezistente la diverse influente.
Introducere -3-
1. Clădirea -4-
2. Nomenclatură și izomerie -6-
3. Proprietăți fizice și prezență în natură -7-
4. Proprietăți chimice -8-
5. Obținerea -9-
6. Aplicație -10-
6.1 Utilizarea esterilor acizilor anorganici -10-
6.2 Utilizarea esterilor acizilor organici -12-
Concluzia -14-
Surse de informare utilizate -15-
Aplicație -16-
Introducere
Dintre derivații funcționali ai acizilor, un loc aparte îl ocupă esterii - derivați ai acizilor în care hidrogenul acid este înlocuit cu radicali alchil (sau în general hidrocarburi).
Esterii sunt împărțiți în funcție de acidul din care provin (anorganic sau carboxilic).
Printre esteri, un loc aparte îl ocupă esterii naturali - grăsimi și uleiuri, care sunt formate din alcoolul trihidroxilic glicerol și acizii grași superiori care conțin un număr par de atomi de carbon. Grăsimile fac parte din organismele vegetale și animale și servesc ca una dintre sursele de energie ale organismelor vii, care este eliberată în timpul oxidării grăsimilor.
Scopul lucrării mele este de a mă familiariza în detaliu cu o astfel de clasă de compuși organici precum esterii și de a analiza în profunzime domeniul de aplicare al reprezentanților individuali ai acestei clase.
1. Structura
Formula generală pentru esterii acidului carboxilic este:
unde R și R" sunt radicali hidrocarburi (în esterii acidului formic, R este un atom de hidrogen).
Formula generala pentru grasimi:

unde R", R", R"" sunt radicali de carbon.
Grăsimile sunt „simple” și „mixte”. Compoziția grăsimilor simple include reziduuri ale acelorași acizi (adică R’ = R "= R"), compoziția grăsimilor mixte include și altele diferite.
Cei mai frecventi acizi grași găsiți în grăsimi sunt:
Acizi alcanoici
1. Acid butiric CH 3 - (CH 2) 2 - COOH
3. Acid palmitic CH 3 - (CH 2) 14 - COOH
4. Acid stearic CH 3 - (CH 2) 16 - COOH
Acizi alchenici
5. Acid oleic C17H33COOH
CH3-(CH2)7-CH === CH-(CH2)7-COOH
Acizi alcadienici
6. Acid linoleic C17H31COOH
CH 3 -(CH 2) 4 -CH \u003d CH-CH 2 -CH \u003d CH-COOH
Acizi alkatrienoici
7. Acid linolenic C17H29COOH
CH 3 CH 2 CH \u003d CHCH 2 CH \u003d\u003d CHCH 2 CH \u003d CH (CH 2) 4 COOH
2. Nomenclatură și izomerie
Numele esterilor sunt derivate din numele radicalului de hidrocarbură și numele acidului, în care se folosește sufixul în locul terminației -ova - la , de exemplu:
Esterii se caracterizează prin următoarele tipuri de izomerie:
1. Izomeria lanțului de carbon începe la reziduul de acid cu acid butanoic, la restul de alcool - cu alcool propilic, de exemplu, izobutirat de etil, acetat de propil și acetat de izopropil sunt izomeri la butiratul de etil.
2. Izomeria poziției grupării esterice -CO-O-. Acest tip de izomerie începe cu esteri ale căror molecule conțin cel puțin 4 atomi de carbon, cum ar fi acetatul de etil și propionatul de metil.
3. Izomeria interclasă, de exemplu, acidul propanoic este izomeric la acetatul de metil.
Pentru esterii care conțin acid nesaturat sau alcool nesaturat, sunt posibile încă două tipuri de izomerie: izomeria poziției legăturii multiple și izomeria cis-, trans.
3. Proprietăți fizice și prezență în natură
Esterii acizilor carboxilici inferiori și ai alcoolilor sunt lichide volatile, insolubile în apă. Multe dintre ele au un miros plăcut. Deci, de exemplu, butirat de butil miroase a ananas, acetatul de izoamil miroase a pere etc.
Esterii acizilor grași superiori și ai alcoolilor sunt substanțe ceroase, inodore, insolubile în apă.
Aroma plăcută a florilor, fructelor, fructelor de pădure se datorează în mare măsură prezenței anumitor esteri în ele.
Grăsimile sunt larg distribuite în natură. Alături de carbohidrați și proteine, ele fac parte din toate organismele vegetale și animale și constituie una dintre principalele părți ale alimentelor noastre.
În funcție de starea lor de agregare la temperatura camerei, grăsimile sunt împărțite în lichide și solide. Grăsimile solide, de regulă, sunt formate din acizi saturați, grăsimile lichide (deseori sunt numite uleiuri) sunt nesaturate. Grăsimile sunt solubile în solvenți organici și insolubile în apă.
4. Proprietăți chimice
1. Reacția de hidroliză sau saponificare. Deoarece reacția de esterificare este reversibilă, prin urmare, în prezența acizilor, reacția de hidroliză inversă are loc:
Reacția de hidroliză este catalizată și de alcalii; în acest caz, hidroliza este ireversibilă, deoarece acidul rezultat cu alcalii formează o sare:
2. Reacția de adiție. Esterii care conțin un acid nesaturat sau alcool în compoziția lor sunt capabili de reacții de adiție.
3. Reacția de recuperare. Reducerea esterilor cu hidrogen duce la formarea a doi alcooli:
4. Reacția de formare a amidelor. Sub acțiunea amoniacului, esterii sunt transformați în amide acide și alcooli:
5. Chitanță
1. Reacție de esterificare:
Alcoolii reacţionează cu acizii minerali şi organici pentru a forma esteri. Reacția este reversibilă (procesul invers este hidroliza esterilor).

Reactivitatea alcoolilor monohidroxilici în aceste reacții scade de la primar la terțiar.
2. Interacțiunea anhidridelor acide cu alcooli:

3. Interacțiunea halogenurilor acide cu alcooli:

6. Aplicare
6.1 Utilizarea esterilor acizilor anorganici
Esteri ai acidului boric - trialchilboraţi- se obtin usor prin incalzirea alcoolului si acidului boric cu adaos de acid sulfuric concentrat. Eterul metilic de bor (borat de trimetil) fierbe la 65 ° C, eterul de bor (borat de trietil) - la 119 ° C. Esterii acidului boric sunt ușor hidrolizați de apă.
Reacția cu acidul boric servește la stabilirea configurației alcoolilor polihidroxici și a fost folosită în mod repetat în studiul zaharurilor.
Eteri de ortosilicon- lichide. Esterul metilic fierbe la 122° C, esterul etilic la 156° C. Hidroliza cu apă este ușoară deja la rece, dar se desfășoară treptat și, în lipsa apei, duce la formarea anhidridei cu molecul mare în care se formează atomi de siliciu. sunt conectate între ele prin oxigen (grupe siloxani):
Aceste substanțe cu greutate moleculară mare (polialcoxisiloxani) sunt utilizate ca lianți care pot rezista la temperaturi destul de ridicate, în special pentru acoperirea suprafeței matrițelor pentru turnarea de precizie a metalelor.Dialchildiclorosilanii reacţionează în mod similar cu SiCl4, de exemplu ((CH3)2SiCl2, formând derivaţi dialcoxi:
Hidroliza lor cu lipsă de apă dă așa-numiții polialchilsiloxani:
Au greutăți moleculare diferite (dar foarte semnificative) și sunt lichide vâscoase utilizate ca lubrifianți rezistenti la căldură, și cu schelete siloxanice și mai lungi, rășini termoizolante și cauciucuri rezistente la căldură.
Esteri ai acidului ortotitanic. Lor obținut în mod similar cu eterii ortosilicici prin reacție:
Acestea sunt lichide care se hidrolizează cu ușurință în alcool metilic și TiO 2 și sunt folosite pentru a impregna țesăturile pentru a le face impermeabile.
Esteri ai acidului azotic. Sunt obținute prin acțiunea unui amestec de acizi sulfuric și azotic concentrat asupra alcoolilor. Azotatul de metil CH 3 ONO 2, (b.p. 60 ° C) și azotatul de etil C 2 H 5 ONO 2 (b.p. 87 ° C) pot fi depășiți cu o muncă atentă, dar când sunt încălzite peste punctul de fierbere sau în timpul detonării, sunt foarte puternice aruncă în aer.

Ca explozivi sunt folosiți etilenglicolul și nitrații de glicerină, numiți incorect nitroglicol și nitroglicerină. Nitroglicerina în sine (un lichid greu) este incomod și periculos de manipulat.
Pentritul - tetranitrat de pentaeritritol C (CH 2 ONO 2) 4, obținut prin tratarea pentaeritritolului cu un amestec de acizi azotic și sulfuric, este, de asemenea, un exploziv puternic de sablare.
Azotatul de glicerol și nitratul de pentaeritritol au efect vasodilatator și sunt utilizați ca agenți simptomatici pentru angina pectorală.
Grăsimile și uleiurile sunt esteri naturali care sunt formați dintr-un alcool trihidroxilic - glicerol și acizi grași superiori cu un lanț de carbon neramificat care conține un număr par de atomi de carbon. La rândul lor, sărurile de sodiu sau potasiu ale acizilor grași superiori sunt numite săpunuri.
Când acizii carboxilici interacționează cu alcoolii ( reacție de esterificare) se formează esterii:
Această reacție este reversibilă. Produșii de reacție pot interacționa între ei pentru a forma substanțele inițiale - alcool și acid. Astfel, reacția esterilor cu apa - hidroliza esterului - este inversul reacției de esterificare. Echilibrul chimic, care se stabilește atunci când vitezele reacțiilor directe (esterificare) și inverse (hidroliză) sunt egale, poate fi deplasat către formarea eterului prin prezența agenților de eliminare a apei.

Esteri în natură și tehnologie
Esterii sunt distribuiți pe scară largă în natură și sunt utilizați în inginerie și în diverse industrii. Ele sunt bune solvenți substanțe organice, densitatea lor este mai mică decât densitatea apei și practic nu se dizolvă în ea. Astfel, esterii cu o greutate moleculară relativ mică sunt lichide foarte inflamabile, cu puncte de fierbere scăzute și miros de diferite fructe. Sunt folosiți ca solvenți pentru lacuri și vopsele, arome ale produselor din industria alimentară. De exemplu, esterul metilic al acidului butiric are miros de mere, esterul etilic al acestui acid are miros de ananas, esterul izobutilic al acidului acetic are miros de banane:

Se numesc esterii acizilor carboxilici superiori și ai alcoolilor monobazici superiori ceară. Deci, ceara de albine este principala
împreună dintr-un ester de acid palmitic și alcool miricilic C 15 H 31 COOC 31 H 63 ; ceara de cachalot - spermaceti - un ester al aceluiasi acid palmitic si alcool cetilic C 15 H 31 COOC 16 H 33.

Grasimi

Cei mai importanți reprezentanți ai esterilor sunt grăsimile.
Grasimi- compuși naturali care sunt esteri ai glicerolului și acizilor carboxilici superiori.
Compoziția și structura grăsimilor pot fi reflectate de formula generală:

Majoritatea grăsimilor sunt formate din trei acizi carboxilici: oleic, palmitic și stearic. Evident, două dintre ele sunt limitative (saturate), iar acidul oleic conține o legătură dublă între atomii de carbon din moleculă. Astfel, compoziția grăsimilor poate include reziduuri de acizi carboxilici atât saturați, cât și nesaturați în diferite combinații.
În condiții normale, grăsimile care conțin reziduuri de acizi nesaturați în compoziția lor sunt cel mai adesea lichide. Se numesc uleiuri. Practic, acestea sunt grăsimi de origine vegetală – uleiuri din semințe de in, cânepă, floarea soarelui și alte uleiuri. Mai puțin frecvente sunt grăsimile lichide de origine animală, cum ar fi uleiul de pește. Majoritatea grăsimilor naturale de origine animală în condiții normale sunt substanțe solide (fuzibile) și conțin în principal reziduuri de acizi carboxilici saturați, de exemplu, grăsimea de oaie. Deci, uleiul de palmier este o grăsime solidă în condiții normale.
Compoziția grăsimilor determină proprietățile lor fizice și chimice. Este clar că pentru grăsimile care conțin reziduuri de acizi carboxilici nesaturați, toate reacțiile compușilor nesaturați sunt caracteristice. Ele decolorează apa de brom, intră în alte reacții de adiție. Cea mai importantă reacție din punct de vedere practic este hidrogenarea grăsimilor. Esterii solizi se obțin prin hidrogenarea grăsimilor lichide. Această reacție stă la baza producției de margarină - grăsime solidă din uleiurile vegetale. În mod convențional, acest proces poate fi descris prin ecuația reacției:

hidroliză:


săpunuri
Toate grăsimile, ca și alți esteri, sunt supuse hidroliză. Hidroliza esterilor este o reacție reversibilă. Pentru a deplasa echilibrul spre formarea produșilor de hidroliză, se realizează într-un mediu alcalin (în prezența alcalinelor sau a Na 2 CO 3 ). În aceste condiții, hidroliza grăsimilor se desfășoară ireversibil și duce la formarea sărurilor acizilor carboxilici, care se numesc săpunuri. Hidroliza grăsimilor într-un mediu alcalin se numește saponificarea grăsimilor.
Când grăsimile sunt saponificate, se formează glicerol și săpunuri - săruri de sodiu sau potasiu ale acizilor carboxilici superiori:

Pat de copil