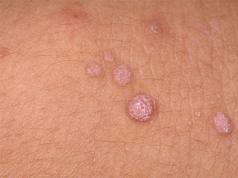
Pirocineza este un termen parapsihologic care se referă la capacitatea de a provoca incendiu sau o creștere semnificativă a temperaturii la distanță cu puterea gândirii. O ființă capabilă de pirocineză se numește pirocinetică, capabilă să influențeze materia cu puterea gândirii. În plus, cazurile de ardere spontană neașteptată și inexplicabilă a oamenilor, când un corp viu se transformă într-o mână de cenușă, sunt de asemenea considerate pirocineză.
Cazuri din istorie
Interesant, materialul inflamabil din apropierea victimei (lenjerie de pat, îmbrăcăminte sau hârtie) a fost neatins.
Așadar, în secolul al XVIII-lea a avut loc moartea misterioasă a contesei Bandi din Casena. Din ea nu mai rămăsese decât capul, trei degete și ambele picioare într-un morman de cenușă care se afla la 4 picioare de pat. Nu erau semne de incendiu pe podea sau pe pat.
În a doua jumătate a secolului al XIX-lea, medicii au început să scrie și despre pirocineză. Unul dintre ei, profesor asistent la Universitatea din Aberdeen, a citit lucrările colegilor și s-a convins că aproximativ jumătate dintre medici consideră că arderea umană spontană este destul de posibilă.
Deci, în raportul unui anume doctor Berthall către Societatea de Medicină și Chirurgie există un mesaj despre o femeie care, la 1 august 1869, a ars în apartamentul ei. Potrivit unui martor ocular, cadavrul arăta ca și cum ar fi fost într-un cuptor de topire. Totuși, totul în jur era intact, doar podeaua ardea puțin - tocmai în locul unde se afla cadavrul. Victima nu a scos niciun țipăt, nu a chemat ajutor, deoarece locuitorii apartamentelor învecinate nu au auzit nimic.
Chiar și la mijlocul secolului al XX-lea, credința că o persoană ar putea epuiza din cauza beției era foarte puternică. Colonelul O. Arkhipov în eseul militar-istoric „În pădurile Bryansk” povestește despre un incident ciudat, la care a asistat personal. În timpul Marelui Război Patriotic, pe unul dintre aerodromurile de câmp, un soldat bolnav a fost încărcat în spatele unui camion vechi pentru a fi trimis la infirmerie. Ei au spus că a băut ceva obscen, numit „șasiu” – un lichid care era destinat să umple amortizoarele. Și pe parcurs, în fața soldaților însoțitori, trupul victimei a izbucnit brusc cu o flacără albastră. Când șoferul a frânat brusc, toată lumea a sărit din corp și s-a repezit în toate direcțiile, iar după un timp au găsit cadavrul carbonizat al unui coleg de călătorie în camion. Cel mai ciudat lucru a fost că pardesiul pe care stătea întins nu a luat foc. Cazul incredibil a fost anulat drept „combustie spontană prin ingestia unui lichid inflamabil”.
Tipuri de aprindere
În ultimele trei secole, pirocineza, inclusiv în prezența martorilor, a depășit sute de oameni, indiferent de sexul lor și dacă au fost bețivi sau abstinenti în timpul vieții. Este destul de dificil să se obțină o regularitate în selectivitatea obiectelor pentru arderea spontană. Pirocineza este omniprezentă și nemiloasă în orice cadru. Prin urmare, specialiștii nu pot decât să înregistreze fapte noi și să sistematizeze acolo unde s-a manifestat din nou. Revista americană de știință populară Discovery raportează că în ultimii 12 ani, numărul cazurilor de pirocineză aproape sa dublat. Se notează două tipuri de aprindere: transformarea victimei în cenușă și sinterizarea acesteia într-o masă carbonizată. În unele cazuri, o parte a corpului nu este atinsă de flăcări. S-a stabilit că în timpul arderii spontane a corpurilor umane, temperatura focului a ajuns la 3000 °C.

arderea spontană a oamenilor. cazuri
1905, iarnă - în Anglia au fost trei incendii ciudate. În micul sat Batlocks Het (Hampshire), într-una dintre case au fost găsite cadavrele carbonizate ale soților Kylie. Interesant este că nici mobilierul, nici draperiile, nici covorul, pe care cuplul de bătrâni căsătoriți a luat brusc foc, nu a fost atins de foc. În Lincolnshire, un fermier a murit într-un incendiu similar, împreună cu aproximativ 300 de gâște și găini. Și câteva zile mai târziu, o femeie în vârstă a luat brusc foc în apropiere.
Billy Peterson (SUA) a izbucnit în flăcări în timp ce își parca mașina într-o parcare din Detroit. Când salvatorii i-au scos corpul carbonizat, s-a descoperit că temperatura din mașină era atât de ridicată încât piesele de pe panoul de bord s-au topit complet.
1956 - Mabel Andrews, în vârstă de 19 ani, dansa cu prietenul ei Billy Clifford pe unul dintre ringurile de dans din Londra și a izbucnit brusc în flăcări. Deși Clifford și cei din jurul lui au încercat să o ajute, ea a murit în drum spre spital. Potrivit lui Billy, nu existau surse de foc în apropiere și i se părea că focul iese direct din corpul ei.
1969 - Dora Metzel, așezată în mașina ei pe una dintre străzile din Luxemburg, s-a aprins brusc, a ars din temelii în câteva secunde. Mai multe persoane au încercat să o ajute, dar fără rezultat. Dar când s-a terminat, s-a dovedit că ornamentele interioare și scaunele mașinii, spre deosebire de cazul lui Peterson, nu au fost deteriorate.
1996 - o fată goală a sărit dintr-o cameră de motel din Brisbane (Australia) cu un strigăt sălbatic. După ce s-a trezit, a spus că a venit aici în weekend cu iubitul ei. S-a culcat, iubitul ei s-a dus să facă baie. Și când a ieșit de acolo și s-a întins lângă ea, a luat deodată foc și un minut mai târziu s-a transformat în praf.
Totuși, conform unei versiuni curioase, vinovatul de pirocineză este o pirobacterie specială care „mâncă” zahărul conținut în corpul uman și produce substanțe combustibile volatile - de exemplu, alcool. Apoi pirocineza poate fi explicată ca arderea unui organism „alcoolizat” dintr-o scânteie imperceptibilă, întâmplătoare. Această bacterie nu a fost încă descoperită și există doar sub forma unui model computerizat complex.

Harugi Ito din Japonia a prezentat o versiune conform căreia cauza pirocinezei este o schimbare a fluxului timpului. În stare normală, corpul uman produce și radiază o anumită cantitate de căldură în spațiu, dar dacă, dintr-un anumit motiv, procesele fizice care au loc în natură încetinesc brusc brusc în interior, iar viteza lor rămâne constantă pe suprafața pielii, atunci căldura generată pur și simplu nu are timp să radieze în spațiu și incinerează o persoană.
Candidatul de științe tehnice A.Stekhin oferă propria sa versiune. Potrivit acestuia, pirocineza este arderea cu plasmă rece. „Trei sferturi dintr-o persoană sunt formate din formațiuni lichide, adică din apă. Radicalii liberi din moleculele sale sunt capabili să „iducă” energie. Poate fi fie energie solară, fie energie biologică. În cazuri excepționale, este eliberat și izbucnește într-un flux de cuante. Mai mult, temperatura exterioară a corpului nu depășește 36 ° C, iar temperatura internă ajunge la 2000 ° C, ceea ce explică paradoxul menționat în sursele scrise: corpul arde până la cenușă, în timp ce încălțămintea, hainele, lenjeria de pat etc. rămân intacte. .
În cele din urmă, un număr de oameni de știință aderă la un punct de vedere foarte fantastic, susținând că sursa de energie dintr-o celulă vie este o reacție termonucleară. În anumite condiții, în celulele corpului apar procese energetice necunoscute, similare cu cele care au loc în timpul exploziei unei bombe atomice. Astfel de procese autodistructive nu depășesc corpul și nu se reflectă în moleculele materiei învecinate - de exemplu, pe haine sau pe tapițeria mașinii.
Omul de știință francez Jacques Millon rezolvă pirocineza de mulți ani. La început, el a întâlnit acest fenomen în spitalele de psihiatrie, unde țineau pacienți acuzați că au încercat să se sinucidă prin auto-imolare. Dar, după cum sa dovedit, pacienții au negat complet chiar și gândul de sinucidere. Au vorbit despre arderea spontană neașteptată a corpului, și-au descris sentimentele și.
După ce a abordat îndeaproape studiul acestei probleme, domnul Milon a primit două educații suplimentare (fizică și fizica câmpului) și a prezentat propria sa versiune a pirokinezei, bazată pe existența unui piropol. Se știe că în natură există diverse tipuri de câmpuri - electrice, magnetice, gravitaționale și, în sfârșit, un câmp bio. Mai mult, toate tipurile de câmpuri interacționează între ele, iar învelișul energetic al unei ființe vii rămâne cel mai misterios. Oamenii de știință nu pot explica până în prezent de ce temperatura corpului unei persoane sănătoase fluctuează cu 0,5 ° C în timpul zilei sau de ce apare o febră bruscă în timpul stresului nervos.
Există un alt tip de câmp în natură - așa-numitul piropol, capabil să încălzească materia proteică. Dar nu oricare, ci doar materie cu un biocâmp puternic, adică corpul uman. Apoi, fluctuațiile de temperatură diurne sunt rezultatul fluctuațiilor piropolului în jurul nivelului său mediu. Iar febra în timpul stresului nervos, așa-numita termonevroză, este rezultatul interacțiunii piropolului cu biocâmpul slăbit al subiectului. Se știe, de asemenea, că câmpul electric și magnetic al Pământului din când în când emite în mod inexplicabil o creștere puternică a energiei sale într-o zonă limitată a spațiului.
Piropolul se comportă exact în același mod, care, în timpul fulgerelor, aruncă fascicule înguste de energie, similare descărcărilor de fulgere invizibile. Astfel de extreme sunt mortale pentru oameni. O persoană prinsă într-un fascicul invizibil se aprinde și se arde instantaneu. Și cu cât biocâmpul este mai puternic, cu atât un individ devine momeală mai gustoasă pentru forțele arzătoare ale naturii. La rândul său, piropolul nu acționează asupra obiectelor neînsuflețite (haine, pantofi, pat, mașină etc.). Acesta, ca un foc adus la o baltă de alcool de pe masă, arde alcoolul, iar zona mesei nici măcar nu se încălzește.
Având în vedere problema apariției arderii ca urmare a încălzirii amestecului combustibil la temperatura de autoîncălzire, merită să acordați atenție faptului că în natură există un număr mare de substanțe și materiale combustibile a căror temperatură de autoîncălzire este egală sau mai mică decât temperatura obișnuită a incintei. Deci, pulberea de aluminiu, atunci când intră în contact cu aerul, este capabilă să se oxideze și, în același timp, să se autoîncălzească până când arderea cu foc are loc chiar și la o temperatură ambientală de 10 0 C. Un astfel de proces de aprindere a substanțelor și materialelor se numește ardere spontană. . Conform standardelor GOST și CMEA combustie spontana- aceasta este: 1) o creștere bruscă a ratei proceselor exoterme într-o substanță, conducând la apariția unui centru de ardere; 2) aprinderea ca urmare a unor procese exoterme autoinițiate.
Arderea spontană ca stadiu inițial al arderii nu diferă fundamental de autoaprindere (vezi Fig. 2.4). Tendința substanțelor și materialelor la combustie spontană poate fi caracterizată în funcție de căldura de ardere a compusului, viteza reacției de oxidare, conductibilitatea termică, capacitatea termică, umiditatea, prezența impurităților, densitatea în vrac, suprafața specifică, pierderea de căldură etc. Arderea spontană este considerată dacă procesul de auto-încălzire a substanțelor și materialelor are loc în intervalul de temperatură de la 273 K la 373 K, adică la temperaturi mai scăzute decât cu autoaprindere.
Orez. 2.4. Schema producerii arderii
Temperatura de autoincalzire numită cea mai scăzută temperatură a unei substanțe la care are loc autoîncălzirea acesteia, care se termină cu autoaprindere. Substanțele combustibile spontan se împart în trei grupe: uleiuri, grăsimi și alte produse de origine vegetală; substanțe chimice inflamabile spontan; combustibili fosili.
Cauza autoîncălzirii care duce la aprindere poate fi o serie de factori: proces microbiologic, adsorbție, polimerizare, căldură reacțiilor chimice. În mod convențional, arderea spontană se clasifică în funcție de cauzele inițiale ale autoîncălzirii și se distinge: ardere spontană termică, ardere spontană microbiologică și chimică (vezi Fig. 2.5).
Să luăm în considerare mai detaliat fiecare tip de ardere spontană.
Arderea termică spontană. Termic numită ardere spontană cauzată de autoîncălzire, care a apărut sub influența încălzirii externe a unei substanțe, material, amestec peste temperatura de autoîncălzire. Arderea termică spontană are loc atunci când o substanță este încălzită la o temperatură care asigură descompunerea ei termică și auto-accelerarea ulterioară a autoîncălzirii datorită căldurii reacțiilor exoterme din volumul de combustibil. În acest caz, reacțiile de oxidare ale produselor de descompunere termică joacă un rol important. Procesul în sine se desfășoară sub formă de mocnire în adâncimea materialului, care apoi se transformă într-o ardere de foc la suprafață. Multe substanțe și materiale sunt predispuse la arderea termică spontană, în special uleiurile și grăsimile, cărbunii și unele substanțe chimice. Autoîncălzirea uleiurilor și grăsimilor de origine vegetală, animală și minerală are loc ca urmare a proceselor oxidative sub acțiunea oxigenului atmosferic cu o suprafață dezvoltată de contact cu acestea. Uleiuri minerale - mașină, transformator, motorină și altele, care se obțin în timpul rafinării petrolului. Sunt în principal un amestec de hidrocarburi saturate și se oxidează în aer doar la temperaturi ridicate. Uleiurile minerale uzate care au fost încălzite la temperaturi ridicate pot conține compuși nesaturați care sunt capabili să se autoîncălzească, adică se pot aprinde spontan.

Orez. 2.5. Schema desfasurarii procesului de ardere spontana a substantelor si materialelor solide. Impulsuri de autoîncălzire (autoaprindere): 1 - termice, 2 - chimice, 3 - microbiologice
Uleiurile vegetale (bumbac, seminte de in, floarea soarelui etc.) si animale (unt, ulei de peste) se deosebesc prin compozitie de uleiurile minerale. Sunt un amestec de gliceride de acizi grași: palmitic C 15 H 31 COOH, stearic C 17 H 35 COOH, oleic C 17 H 33 COOH, linoleic C 17 H 31 COOH, linolenic C 17 H 29 COOH etc. Acizi palmitic și stearic sunt limitative, oleice, linoleice și linolenice - nesaturate. Gliceridele acizilor saturați și, în consecință, uleiurile și grăsimile care le conțin în cantități mari, se oxidează la temperaturi peste 150 0 C, ceea ce înseamnă următoarele: nu sunt capabile de ardere spontană (vezi Tabelul 2.3). Uleiurile care conțin o cantitate mare de gliceride de acizi nesaturați încep să se oxideze la temperaturi mult sub 100 0 C, prin urmare, sunt capabile de ardere spontană.
Tabelul 2.3.
Compoziția grăsimilor și uleiurilor
|
Numele grăsimilor și uleiurilor |
Gliceride ale acizilor, % (greutate) |
|||
|
palmitic și stearic |
olei-nou |
lino-stânga |
linol-nou |
|
|
floarea soarelui | ||||
|
Bumbac | ||||
Uleiurile și grăsimile se aprind spontan numai în anumite condiții: a) dacă în compoziția uleiurilor și grăsimilor există o cantitate semnificativă de gliceride ale acizilor nesaturați; b) în prezența unei suprafețe mari de oxidare a acestora și transfer redus de căldură; c) dacă materiale combustibile fibroase sunt impregnate cu grăsimi și uleiuri; d) materialele unse cu ulei au o anumită densitate.
Capacitatea diferită a uleiurilor vegetale și a grăsimilor animale de a arde spontan se explică prin faptul că acestea conțin gliceride de compoziție, structură diferită și nu în aceeași cantitate.
Gliceridele acizilor nesaturați sunt capabile să se oxideze în aer la temperatura normală a camerei datorită prezenței dublelor legături în moleculele lor:

Peroxizii se descompun ușor pentru a forma oxigen atomic, care este foarte reactiv:
Oxigenul atomic interacționează chiar și cu componentele uleiului care sunt greu de oxidat. Concomitent cu oxidarea, are loc și reacția de polimerizare a compușilor nesaturați

Procesul are loc la o temperatură scăzută cu degajare de căldură. Cu cât glicerida are mai multe legături duble, cu atât se atașează mai multe molecule de oxigen, cu atât mai multă căldură este eliberată în timpul reacției, cu atât este mai mare capacitatea sa de a se aprinde spontan.
Cantitatea de gliceride ale acizilor nesaturați din ulei și grăsimi se apreciază după numărul de iod al uleiului, adică după cantitatea de iod absorbită de 100 g de ulei. Cu cât este mai mare numărul de iod, cu atât este mai mare capacitatea acestei grăsimi sau ulei de a se aprinde spontan (vezi Tabelul 2.4).
Uleiul de in are cea mai mare valoare a iodului. Materialele fibroase impregnate cu ulei de in, în toate celelalte condiții identice, se aprind spontan mai repede decât materialele impregnate cu alte uleiuri. Uleiurile uscate preparate pe baza de uleiuri vegetale au un număr de iod mai mic decât baza, dar capacitatea lor de a se aprinde spontan este mai mare. Acest lucru se datorează faptului că uleiului de uscare se adaugă un desicant, care accelerează uscarea acestuia, adică oxidarea și polimerizarea. Uleiurile de uscare semi-naturale, care sunt amestecuri de semințe de in oxidate sau alte uleiuri vegetale cu solvenți, au un număr scăzut de iod și nu sunt foarte capabile de ardere spontană. Uleiurile de uscare sintetice sunt complet incapabile de ardere spontană.
Tabelul 2.4.
Numărul de iod de grăsimi și uleiuri
Grăsimile de pește și animale marine au un număr mare de iod, dar au o ușoară capacitate de a se aprinde spontan. Acest lucru se datorează faptului că acestea conțin produse care încetinesc procesul de oxidare.
Capacitatea materialelor unse cu ulei de a se autoaprinde crește odată cu prezența catalizatorilor în ele, care accelerează procesul de oxidare și polimerizare a uleiurilor. O creștere a temperaturii ambientale contribuie și ea la accelerarea acestor procese. Catalizatorii pentru arderea spontană a uleiurilor sunt săruri ale diferitelor metale: mangan, plumb, cobalt. Cea mai scăzută temperatură la care s-a observat în practică arderea spontană a uleiurilor și grăsimilor a fost 10-15 0 С.
Perioada de inducție pentru autoaprinderea materialelor uleiate poate varia de la câteva ore la câteva zile. Depinde de volumul materialului uns, gradul de compactare a acestuia, tipul de ulei sau grăsime și cantitatea acestora, temperatura aerului și alți factori.
cărbuni fosili(piatră, maro), care sunt depozitate în grămezi sau stive, sunt capabile de ardere spontană la temperaturi scăzute. Principalele cauze ale arderii spontane sunt capacitatea cărbunilor de a oxida și adsorbi vapori și gaze la temperaturi scăzute. Procesul de oxidare în cărbune la temperaturi scăzute este destul de lent și se eliberează puțină căldură. Dar în acumulări mari de cărbune, transferul de căldură este dificil, iar arderea spontană a cărbunelui încă are loc. Autoîncălzirea într-o grămadă de cărbune are loc inițial în întregul volum, excluzând doar stratul de suprafață de 0,3-0,5 m grosime, dar pe măsură ce temperatura crește, capătă un caracter focal. Creșterea temperaturii în sursa de ardere spontană până la 60 0 C este lentă și se poate opri atunci când coșul este ventilat. Începând de la 60 0 C, viteza de autoîncălzire crește brusc, această temperatură a cărbunelui se numește critic. Tendința cărbunilor de a se autoaprinde în grămezi este diferită, depinde de cantitatea de substanțe volatile eliberate din aceștia, de gradul de măcinare, de prezența umidității și a piritei. Conform standardelor de depozitare, toți cărbunii fosili sunt împărțiți în două categorii în funcție de tendința lor de ardere spontană: A - periculos, B - stabil.
Categoria A include cărbunii bruni și negri, cu excepția gradului T, precum și amestecurile de diferite categorii. Cele mai periculoase în raport cu arderea spontană sunt cărbunii de clase OS (Kuznetsk), Zh (Tkvarchelsk), G (Tkibulsk), D (Pechersk, Kuznetsk și Donețk), B (Raychikhinsky, ucraineană, Lenirovsky, Angrensky etc.). Acești cărbuni nu pot fi depozitați mult timp. Categoria B include antracitul și cărbunele de gradul T. Toate antracitele și brichetele de cărbune, cărbunele de gradul T (Donețk, Kuznetsk), Zh (Pechersk și Suchansk), G (suchansk), D (Chernehov) sunt stabile în timpul depozitării pe termen lung.
Pentru a preveni arderea spontană a cărbunelui în timpul depozitării, s-au stabilit următoarele standarde: 1) limitarea înălțimii stivelor de cărbune; 2) compactarea cărbunelui în coș pentru a limita accesul aerului la volumul interior al coșului.
Implementarea acestor măsuri minimizează viteza proceselor de oxidare și adsorbție, creșterea temperaturii în coș, împiedică pătrunderea precipitațiilor atmosferice în coș și reduce în mod natural posibilitatea arderii spontane.
De asemenea, multe substanțe chimice sunt predispuse la arderea termică spontană.. Sulfurile de fier FeS, FeS 2, Fe 2 S 3 sunt capabile de ardere spontană, deoarece pot reacționa cu oxigenul din aer la temperaturi obișnuite cu eliberarea unei cantități mari de căldură:
FeS 2 + O 2 → FeS + SO 2 + 222,3 kJ.
Au existat cazuri de ardere spontană a piritei sau piritei sulfuroase (FeS 2) în depozitele uzinelor de acid sulfuric, precum și în mine. Umiditatea favorizează arderea spontană a piritei. Se presupune că reacția în acest caz decurge conform următoarei ecuații:
2FeS 2 + 7,5O 2 + H 2 O → Fe 2 (SO 4) 3 + K 2 SO 4 + 2771 kJ.
Odată cu formarea sulfatului de fier, volumul crește și pirita se crăpă și se macină, ceea ce favorizează procesul de ardere spontană.
Sulfurile FeS și Fe 2 S 3 se formează în rezervoare pentru depozitarea produselor petroliere, gazelor combustibile și în echipamentele diverselor industrii, unde sunt prezente impurități de hidrogen sulfurat. Formarea sulfurilor de fier are loc diferit în funcție de temperatură. Dacă temperatura este peste temperatura de disociere a hidrogenului sulfurat, adică peste 310 0 C, sulfurile de fier se formează prin interacțiunea fierului cu sulful elementar rezultat din descompunerea hidrogenului sulfurat sau a altor compuși ai sulfului. Sulful elementar poate fi obținut și ca urmare a oxidării hidrogenului sulfurat, iar apoi formarea sulfurei de fier are loc în funcție de următoarele reacții:
2H2S + O2 → 2H2O + 2S,
La temperaturi sub 310 0 C, sulfurile de fier din echipamentele industriale se formează ca urmare a acțiunii hidrogenului sulfurat nu asupra fierului, ci asupra produselor sale de coroziune:
2Fe(OH)3 + 3H2S → Fe2S2 + 6H2O.
Toate incendiile din echipamentele industriale care au apărut ca urmare a arderii spontane a sulfurilor de fier au avut loc după ce echipamentul a fost eliberat din produsul depozitat sau prelucrat în acesta.
De exemplu, la o rafinărie de petrol care prelucrează ulei acru, o coloană de distilare a benzinei a fost pusă pentru reparație. La deschiderea trapei s-a găsit un strat de sulfură de fier pe pereții coloanei și ai plăcilor. Alimentarea rapidă cu abur a coloanei a făcut posibilă prevenirea oxidării și arderii spontane a sulfurei de fier. După cum puteți vedea, sulfura de fier din coloană s-a format cu mult timp în urmă, dar din cauza absenței aerului, oxidarea nu a avut loc.
Arderea spontană a sulfurilor de fier în echipamentele industriale este împiedicată prin următoarele metode: curățarea produsului prelucrat sau depozitat de hidrogen sulfurat, acoperirea anticorozivă a suprafeței interioare a echipamentului, suflarea echipamentului cu abur sau produse de ardere pentru îndepărtarea vaporilor combustibili și gaze, umplând echipamentul cu apă și coborând încet, ceea ce duce la oxidarea sulfurei fără a accelera răspunsul.
Fosfor alb (galben), hidrogen fosfurat (fosfină), siliciu hidrogen (silan), praf de zinc, pulbere de aluminiu, carburi de metale alcaline, sulfuri de metal - rubidiu și cesiu, arsine, stibine, fosfine, cărbune sulfonat și alte substanțe pot fi de asemenea oxidate în aer cu degajare de căldură, datorită căreia reacția este accelerată până la ardere. Unele dintre aceste substanțe sunt capabile de ardere spontană foarte rapid după contactul cu aerul, în timp ce altele - după o perioadă lungă de timp.
De exemplu, fosforul alb (galben) este oxidat intens la temperatura camerei, prin urmare se încălzește rapid și se aprinde cu formarea de fum alb:
4P + 5O 2 → 2P 2 O 5 + 3100,6 kJ.
Când substanțele combustibile sunt umezite cu o soluție de fosfor în disulfură de carbon, disulfura de carbon se evaporă; stratul subțire de fosfor rămas la suprafață se oxidează rapid și se aprinde spontan. În funcție de concentrația soluției, substanțele umezite cu aceasta se aprind spontan la intervale diferite.
Fosforul trebuie depozitat și tăiat sub apă, deoarece în aer se poate aprinde de la căldura frecării, iar fosforul alb este foarte otrăvitor.
Unele metale, pulberi metalice, pulberi sunt capabile de ardere spontană în aer datorită căldurii degajate în timpul reacției de oxidare. Din metale în stare compactă, rubidiul și cesiul au această capacitate, din pulberile metalice - pulbere de aluminiu etc. Pentru a preveni arderea spontană a pulberii de aluminiu, se prepară într-un mediu gazos inert și apoi se măcina cu grăsimi, a căror peliculă protejează. pulberi de la oxidare. Există cazuri când pulberea de aluminiu sub acțiunea unui solvent sau încălzire a fost degresată și aprinsă spontan.
Carburele metalelor alcaline K 2 C 2 , Na 2 C 2 , Li 2 C 2 se aprind spontan nu numai în aer, ci chiar și în atmosfere de CO 2 și SO 2.
Eterul dietil și terebentina sunt, de asemenea, capabili să se autoaprinde în aer. Eterul dietil, la contact prelungit cu aerul în lumină, este capabil să formeze peroxid de dietil (C 2 H 5) O 2, care, la impact sau încălzire la 75 0 C, se descompune cu o explozie și aprinde eterul. De asemenea, terebentina se poate aprinde spontan dacă materialele fibroase sunt umezite cu ea. Cauza arderii spontane este capacitatea terebentinei de a se oxida în aer la temperaturi scăzute. Există un caz cunoscut de ardere spontană a vatei umezite cu terebentină. Un astfel de bumbac a fost spălat de vopsea de ulei din peisaj. Noaptea, vata colectată într-un singur loc s-a aprins spontan. Există și cazuri de ardere spontană a mușchilor umeziți cu terebentină.
Cărbunele sulfonat, aflat în pungi de hârtie stivuite într-o grămadă, este capabil de ardere spontană. Au fost cazuri de ardere spontană a acestuia în primele 2-3 zile de la stivuirea pungilor.
Arderea microbiologică spontană. Microbiologic numită ardere spontană rezultată din autoîncălzire sub influența activității vitale a microorganismelor în masa unei substanțe, material, amestec. Astfel de substanțe includ turba (în principal măcinată), materiale vegetale: fân, trifoi, siloz, malț, cereale, bumbac, acumulare de rumeguș și materiale similare.
Materialele subuscate sunt deosebit de susceptibile la arderea spontană. Umiditatea și căldura contribuie la reproducerea microorganismelor în masa acestor materiale deja la 10-18 0 C. Datorită conductivității termice slabe a materialelor vegetale, căldura eliberată în timpul descompunerii merge la încălzirea materialului în descompunere, temperatura acestuia crește și poate ajunge la 70 0 C. Microorganismele mor la această temperatură, totuși creșterea temperaturii în material nu se oprește, deoarece unii compuși organici sunt deja carbonizați în acest moment. Cărbunele poros rezultat tinde să adsorbe vapori și gaze, ceea ce este însoțit de eliberarea de căldură. În cazul transferului scăzut de căldură, cărbunele este încălzit înainte de începerea procesului de oxidare și temperatura materialelor vegetale crește, ajungând la 200 0 C. Aceasta duce la descompunerea fibrelor și la carbonizarea în continuare a masei. Se intensifică procesul de oxidare a cărbunelui poros, în urma căruia temperatura crește și are loc arderea. La umezirea materialelor vegetale, atât la temperaturi normale, cât și la temperaturi ridicate, se eliberează gaze, inclusiv combustibile. Deci, atunci când materiile prime vegetale sunt înmuiate cu vapori de apă sau apă, la stingerea unui produs care arde, eliberarea de CO, CH 4 , H 2 începe în cantități care depășesc semnificativ NKPRP pentru fiecare dintre aceste gaze. Prin urmare, utilizarea numai a apei sau aburului pentru suprimarea surselor de ardere a materiilor prime vegetale din silozuri și buncăre poate duce la o explozie a instalațiilor de depozitare.
Arderea chimică spontană. Chimic numită ardere spontană, rezultată din interacțiunea chimică a substanțelor. Arderea chimică spontană are loc în punctul de contact al substanțelor care interacționează care reacționează cu degajarea de căldură. În acest caz, arderea spontană este de obicei observată pe suprafața materialului și apoi se răspândește în profunzime. Procesul de autoincalzire incepe la temperaturi sub 50 0 C. Unii compusi chimici sunt predispusi la autoincalzire ca urmare a contactului cu oxigenul atmosferic si alti agenti oxidanti, intre ei si cu apa. Motivul auto-încălzirii este reactivitatea lor ridicată.
Substante care se aprind spontan la contactul cu oxiziimembrii. Multe substanțe, în mare parte organice, sunt capabile de ardere spontană atunci când sunt amestecate sau în contact cu agenți oxidanți. Agenții oxidanți care provoacă arderea spontană a unor astfel de substanțe includ: oxigenul aerului, oxigenul comprimat, halogenii, acidul azotic, peroxidul de sodiu și bariu, permanganatul de potasiu, anhidrida cromică, dioxidul de plumb, salitrul, clorații, perclorații, înălbitorul etc. Unele dintre amestecuri a oxidanților cu substanțe combustibile sunt capabili de ardere spontană numai atunci când sunt expuși la acid sulfuric sau azotic sau la impact și încălzire scăzută.
ardere spontană în aer. Unii compuși chimici sunt predispuși la auto-încălzire ca urmare a contactului cu oxigenul atmosferic. Motivul arderii spontane este reactivitatea lor ridicată în contact cu alți compuși. Deoarece acest proces are loc mai ales la temperatura camerei, este denumit și ardere spontană. De fapt, un proces notabil de interacțiune între componente este observat la temperaturi mult mai ridicate și, prin urmare, temperatura lor de autoaprindere este dată ca indicator de temperatură al pericolului de incendiu al unor astfel de substanțe. De exemplu, pulberea de aluminiu se aprinde spontan în aer. Cu toate acestea, reacția de formare a aluminei are loc la 913 K.
oxigen comprimat Provoaca arderea spontana a unor substante (ulei mineral) care nu se aprind spontan in oxigen la presiune normala.
Clor, brom, fluor și iod se combină extrem de activ cu unele substanțe combustibile, iar reacția este însoțită de eliberarea unei cantități mari de căldură, ceea ce duce la arderea spontană a substanțelor. Deci, acetilena, hidrogenul, metanul și etilena amestecate cu clorul se aprind spontan la lumina sau la lumina arderii magneziului. Dacă aceste gaze sunt prezente în momentul eliberării clorului din orice substanță, arderea lor spontană are loc chiar și în întuneric:
C2H2 + C12 → 2HC1 + 2C,
CH 4 + 2C1 2 → 4HC1 + C etc.
Nu depozitați halogeni împreună cu lichide inflamabile. Se știe că terebentina, distribuită în orice substanță poroasă (în hârtie, țesătură, bumbac), se aprinde spontan în clor. Vaporii de eter dietil se pot aprinde, de asemenea, spontan într-o atmosferă de clor:
C2H5OS2H5 + 4C12 → H2O + 8HC1 + 4C.
Fosforul roșu se aprinde instantaneu spontan când intră în contact cu clorul sau bromul.
Nu numai halogenii în stare liberă, ci și compușii lor reacţionează energic cu unele metale. Deci, interacțiunea tetraclorurii de etan C 2 H 2 CI 4 cu potasiul metalic are loc cu o explozie:
C2H2C14 + 2K → 2KS1 + 2HC1 + 2C.
Un amestec de tetraclorură de carbon CC1 4 sau tetrabromură de carbon cu metale alcaline explodează când este încălzit la 70 0 C.
Acidul azotic, descompunându-se, eliberează oxigen, prin urmare este un agent oxidant puternic capabil să provoace arderea spontană a unui număr de substanțe.
4HNO8 → 4NO2 + O2 + 2H2O.
În contact cu acidul azotic, terebentina și alcoolul etilic se aprind spontan.
Materialele vegetale (paie, in, bumbac, rumeguș și așchii) se aprind spontan dacă sunt expuse la acid azotic concentrat.
În contact cu peroxidul de sodiu, următoarele lichide combustibile și inflamabile sunt capabile de ardere spontană: alcooli metil, etil, propil, butilic, izoamil și benzilic, etilen glicol, dietil eter, anilină, terebentină și acid acetic. Unele lichide se aprind spontan cu peroxid de sodiu după introducerea unei cantități mici de apă în ele. Așa se comportă eterul acetic (acetat de etil), acetona, glicerina și alcoolul izobutilic. Începutul reacției este interacțiunea apei cu peroxidul de sodiu și eliberarea de oxigen atomic și căldură:
Na2O2 + H2O → 2NaOH + O.
Oxigenul atomic în momentul eliberării oxidează lichidul combustibil și se aprinde spontan. Pulberea de aluminiu, rumegușul, cărbunele, sulful și alte substanțe amestecate cu peroxid de sodiu se aprind instantaneu când o picătură de apă le lovește.
Un agent oxidant puternic este permanganatul de potasiu KMnO 4 . Amestecurile sale cu substanțe combustibile solide sunt extrem de periculoase. Acestea se aprind spontan din acțiunea acizilor sulfuric și azotic concentrați, precum și din impact și frecare. Glicerina C 3 H 5 (OH) 3 şi etilenglicolul C 2 H 4 (OH) 2 se aprind spontan într-un amestec cu permanganat de potasiu la câteva secunde după amestecare.
Anhidrida cromică este, de asemenea, un agent oxidant puternic. La contactul cu anhidrida cromică, următoarele lichide se aprind spontan: alcooli metilici, etilici, butilici, izobutilici și izoamilici; aldehide acetice, butirice, benzoice, propionice și paraldehide; dietil eter, acetat de etil, acetat de amil, metildioxan, dimetildioxan; acizi acetic, pelargonic, nitrilacrilic; acetonă.
Amestecurile de salpetru, clorați, perclorați sunt capabile de ardere spontană atunci când sunt expuse la acid sulfuric și uneori la acid azotic. Cauza arderii spontane este eliberarea de oxigen sub acțiunea acizilor. Când acidul sulfuric reacționează cu sarea Berthollet, are loc următoarea reacție:
H2SO4 + 2KSlO3 → K2SO4 + 2НClO3.
Acidul percloric este instabil și, atunci când este format, se descompune odată cu eliberarea de oxigen:
2HClO3 → 2HC1 + 3O2.
Carburele metalelor alcaline K 2 C 2, Na 2 C 2, Li 2 C 2 se aprind spontan nu numai în aer, ci chiar și într-o atmosferă de CO 2, SO 2.
De exemplu, carbura de calciu Ca 2 C, în contact cu apa, eliberează gaz inflamabil acetilenă C 2 H 2, care se aprinde în amestec cu aerul ca urmare a încălzirii prin căldura degajată în timpul reacției, T sv acetilena este de 603 K.
Substante care se aprind spontan la contactul cu apa. Acest grup de materiale include potasiu, sodiu, rubidiu, cesiu, carbură de calciu și carburi de metale alcaline, hidruri de metale alcaline și alcalino-pământoase, fosfuri de calciu și sodiu, silani, var nestins, hidrosulfură de sodiu etc.
Metalele alcaline - potasiu, sodiu, rubidiu și cesiu - interacționează cu apa cu eliberarea de hidrogen și o cantitate semnificativă de căldură:
2Na + 2H2O → 2NaOH + H2,
2K + 2H2O → 2KOH + H2.
Hidrogenul eliberat se aprinde și arde în mod spontan împreună cu metalul numai dacă bucata de metal este mai mare ca volumul unui bob de mazăre. Interacțiunea acestor metale cu apa este uneori însoțită de o explozie cu stropire de metal topit. Hidrururile metalelor alcaline și alcalino-pământoase (KH, NaH, CaH 2) se comportă în același mod atunci când interacționează cu o cantitate mică de apă:
NaH + H2O → NaOH + H2.
Când carbura de calciu reacţionează cu o cantitate mică de apă, se eliberează atât de multă căldură încât, în prezenţa aerului, acetilena rezultată se aprinde spontan. Cu multă apă, acest lucru nu se întâmplă. Carburele metalelor alcaline (de exemplu, Na 2 C 2, K 2 C 2) explodează la contactul cu apa, iar metalele ard, iar carbonul este eliberat în stare liberă:
2Na2C2 + 2H2O + O2 → 4NaOH + 4C.
Fosfura de calciu Ca 3 P 2, atunci când interacționează cu apa, formează fosfură de hidrogen (fosfină):
Ca 3 P 2 + 6H 2 O → 3Ca (OH) 2 + 2PH 3.
Fosfina pH 3 este un gaz combustibil, dar nu este capabil de ardere spontană. Împreună cu PH 3, se eliberează o anumită cantitate de lichid P 2 H 4, care este capabil de ardere spontană în aer și poate provoca aprinderea PH 3.
Silanii, adică compuși ai siliciului cu diferite metale, de exemplu Mg2Si, Fe2Si, sub acțiunea apei, eliberează hidrogen siliciu, care se aprinde spontan în aer:
Mg a Si + 4H2O → 2Mg (OH)2 + SiH4,
SiH4 + 2O2 → SiO2 + 2H2O.
Deși peroxidul de bariu și peroxidul de sodiu interacționează cu apa, în timpul acestei reacții nu se formează gaze combustibile. Arderea poate apărea dacă peroxizii sunt amestecați sau în contact cu substanțe combustibile.
Oxidul de calciu (var nestins), reacționând cu o cantitate mică de apă, se încălzește pentru a străluci și poate aprinde materiale combustibile în contact cu acesta.
Hidrosulfitul de sodiu, fiind umed, se oxidează viguros cu degajarea de căldură. Ca urmare a acestui fapt, are loc arderea spontană a sulfului, care se formează în timpul descompunerii hidrosulfitului.
Astfel, arderea spontană și autoîncălzirea amestecurilor combustibile, substanțelor și materialelor care se desfășoară la temperaturi scăzute sunt de aceeași natură cu autoaprinderea, dar datorită prevalenței lor mai mari, provoacă incendii mult mai des decât autoaprinderea.
Capacitatea explozivă a gazelor combustibile, vaporilor și prafului din aer este menținută în anumite intervale ale concentrațiilor acestora. Există limite inferioare și superioare de concentrație și temperatură pentru propagarea flăcării.
Limita inferioară (superioară) de concentrație a propagării flăcării (NKPRP) este conținutul minim (maxim) al unei substanțe combustibile într-un amestec omogen cu mediu oxidant, la care propagarea flăcării prin amestec este posibilă la orice distanță de sursa de aprindere. Imposibilitatea aprinderii amestecului combustibil la o concentrație sub NKPRP se datorează cantității mici de substanță combustibilă și excesului de aer. Cu cât este mai mic raportul de aer în exces, cu atât este mai mare viteza de ardere și presiunea vaporilor în timpul exploziei este mai mare. Limita superioară de concentrație a propagării flăcării se caracterizează printr-un exces de combustibil și o cantitate mică de aer. Cu cât limita inferioară de concentrație este mai mică și cu cât zona de concentrare a propagării flăcării este mai mare, cu atât riscul de incendiu al substanțelor combustibile este mai mare.
În primul caz, explozia nu se produce din cauza lipsei unei substanțe combustibile, în al doilea caz, din cauza lipsei de aer (oxigen) necesar oxidării unei substanțe combustibile.
9. Tipuri de ardere spontană
Arderea spontană este inerentă tuturor substanțelor și materialelor combustibile solide.
Combustie spontana- acesta este un fenomen de creștere bruscă a vitezei reacțiilor interne (exoterme) într-o substanță, care duce la ardere în absența unei surse de aprindere. Dacă arderea spontană produce o flacără, atunci acest fenomen se numește autoaprindere.
Combustie spontana apare din cauza faptului că degajarea de căldură în timpul reacțiilor este mai mare decât îndepărtarea căldurii către mediu. Debutul arderii spontane se caracterizează prin temperatura de autoîncălzire ( T sn), care este temperatura minimă la care este detectată degajarea de căldură.
Când se atinge o anumită temperatură în procesul de auto-încălzire, numită temperatură de autoaprindere ( T livrare.), are loc arderea materialului, manifestată fie prin ardere mocnită, fie prin ardere aprinsă. In ultimul caz T livrare. este adecvat pentru temperatura de autoaprindere ( T Sf.), care se înțelege ca apariția arderii gazelor și lichidelor atunci când sunt încălzite la o anumită temperatură critică. În principiu, arderea spontană și autoaprinderea sunt similare în esență fizică și diferă doar prin tipul de ardere, autoaprinderea are loc numai sub formă de ardere a flăcării.
În cazul autoaprinderii, autoîncălzirea se dezvoltă în doar câteva grade și, prin urmare, nu este luată în considerare la evaluarea pericolului de incendiu și explozie al gazelor și lichidelor. În timpul arderii spontane, zona de autoîncălzire poate ajunge la câteva sute de grade (de exemplu, pentru turbă de la 70 la 225 °C). Ca urmare, fenomenul de autoîncălzire trebuie luat în considerare la determinarea tendinței solidelor la ardere spontană.
Autoaprinderea se studiază prin termostatarea materialului studiat la o temperatură dată și stabilirea relației dintre temperatura la care are loc arderea, mărimea probei și timpul în care este încălzită în termostat. Procesele care au loc în timpul arderii spontane a probelor de materiale combustibile sunt prezentate în Figura 3.1.
Orez. 3.1. Procese de autoaprindere
Posibilitatea arderii spontane a unui material situat într-o zonă cu potențial pericol de incendiu se stabilește cu ajutorul ecuațiilor:
lg T înv. = A 1 – n 1 lg ℓ , (3.1)
lg T înv. = A 2 – n 2 lg τ , (3.2)
Unde T înv. − temperatura ambiantă, °C; ℓ − definirea dimensiunii (de obicei grosimea) materialului; τ - timpul în care se poate produce arderea spontană; DAR 1 , P 1 și DAR 2 , P 2 - coeficienți determinați pentru fiecare material conform datelor experimentale (vezi Tabelul 3.1).
Conform ecuației (3.1) pentru un dat ℓ găsi T înv., la care poate avea loc arderea spontană a unui anumit material, conform ecuației (3.2) cu un T înv. − valoare τ .
La temperaturi sub cele calculate T înv. , sau când τ , mai mic decât timpul calculat prin ecuația (3.2), are loc arderea spontană.
În funcție de natura procesului inițial care a determinat autoîncălzirea materialului și de valori T sn . , distinge chimic, microbiologicȘi ardere spontană termică.
Căldura unei conducte obișnuite de apă caldă sau de abur ( T\u003d 100 ÷ 150 ºС) poate fi sursa de căldură, care este suficientă pentru arderea spontană a produselor din țesătură, hârtie sau lemn. Prin urmare, conductele de apă caldă sau de abur trebuie protejate numai cu ecrane din materiale incombustibile. Grilele decorative sunt permise în clădirile publice, dar în primul și al doilea caz, distanța de la conducte la ecrane, precum și la orice material combustibil (perdele, de exemplu) trebuie să fie de cel puțin 100 mm. În condiții de producție, cărbunele, turba, rumegușul și unele lichide combustibile se aprind spontan, de obicei sub formă de pelicule subțiri obținute prin aplicarea lichidului pe suprafețe lanuoase (bumbac, vată etc.). Aceste lichide includ uleiuri vegetale, terebentină. La întreprinderi, există cazuri de ardere spontană a materialelor de curățare, salopete uleiate, prin urmare, salopetele trebuie atârnate astfel încât să ofere acces la aer, să elimine căldura, materialele de curățare unse cu ulei sunt colectate în recipiente ignifuge cu capace și sunt îndepărtate, ars sau distrus în fiecare schimb. Există cazuri de mocnire și ardere a cărbunelui în mormane, turbă și bumbac, cazuri de ardere spontană a pâslelor de acoperiș în rulouri, celofan și celuloid, hârtie, iar materialele au fost observate în mod repetat.
Cerința generală de siguranță la incendiu pentru cazurile de ardere spontană termică este formulată destul de simplu: temperatura de siguranță pentru încălzirea prelungită a unei substanțe este considerată a fi o temperatură care nu depășește 90% din temperatura de autoîncălzire.
Arderea chimică spontană asociat cu capacitatea substanțelor și materialelor de a intra într-o reacție chimică cu aerul sau alți agenți oxidanți în condiții normale cu eliberare de căldură suficientă pentru a le aprinde (de exemplu, atunci când acidul azotic condiționat ajunge pe hârtie, rumeguș etc.). Exemplele cele mai tipice sunt cazurile de ardere spontană a cârpelor uleioase sau a fosforului în aer, lichide inflamabile în contact cu permanganatul de potasiu, rumeguș cu acizi etc. Uleiuri care conțin compuși cu legături chimice nesaturate și se caracterizează printr-un număr mare de iod (bumbac, floarea soarelui, iută etc.) d.).
Un alt tip de reacții chimice ale substanțelor este asociat cu interacțiunea apei sau umidității. În același timp, se eliberează și o temperatură suficientă pentru arderea spontană a substanțelor și materialelor. Exemple sunt substanțe precum potasiul, sodiul, carbura de calciu, varul nestins, etc. O caracteristică a metalelor alcalino-pământoase este capacitatea lor de a arde chiar și fără oxigen. Ei înșiși produc oxigenul necesar reacției, împărțind umiditatea aerului în hidrogen și oxigen sub influența temperaturii ridicate. De aceea stingerea unor astfel de substanțe cu apă duce la o explozie a hidrogenului rezultat. Pentru a preveni arderea chimică spontană, procedura de depozitare în comun a substanțelor și materialelor combustibile este strict reglementată.
predispus la ardere microbiologică spontană posedă materiale combustibile, mai ales umede, servind drept mediu nutritiv pentru microorganismele a căror activitate vitală este asociată cu degajarea de căldură (turbă, rumeguș etc.). Din acest motiv, un număr mare de incendii și explozii apar atunci când produsele agricole (de ex. siloz, fân umed) sunt depozitate în silozuri. Arderea spontană microbiologică și chimică se caracterizează prin faptul că T sn. nu depaseste valorile normale T înv.și poate fi negativ. Materiale care au T sn. peste temperatura camerei, sunt capabile de ardere termică spontană.
Multe materiale solide cu o suprafață dezvoltată (de exemplu, fibroasă), precum și unele substanțe lichide și în topire care conțin compuși nesaturați depuși pe o suprafață dezvoltată (inclusiv necombustibilă), au tendința la toate tipurile de ardere spontană. Toate tipurile de ardere spontană au o diviziune pur condiționată, iar pentru majoritatea substanțelor combustibile, procesul de ardere spontană este o combinație de termic, chimicȘi reacție microbiologică.
Arderea spontană este rezultatul autoîncălzirii substanţelor, adică. proces spontan care se încheie cu ardere mocnită sau ardere.
Apariția arderii spontane este influențată de căldura de ardere, conductivitatea termică, suprafața specifică și densitatea în vrac a substanței, precum și condițiile schimbului de căldură cu mediul extern.
Auto-încălzirea unei substanțe poate fi cauzată din diverse motive. Poate fi inițiată de procese microbiologice care au loc în mediul nutritiv, expunerea la temperaturi ridicate și eliberarea de căldură ca rezultat al reacțiilor chimice.
Pentru ca procesul de autoincalzire sa se incheie cu ardere spontana este necesar ca substanta sa aiba capacitatea de a se oxida si sa se formeze conditiile necesare pentru acumularea de caldura.
Esența fizică a proceselor de ardere spontană și autoaprindere este aceeași și condițiile de autoaccelerare a reacției sunt aceleași. Principala diferență dintre ele este că arderea spontană are loc la o temperatură a aerului ambiental egală sau mai mare decât temperatura de autoaprindere, iar aprinderea spontană are loc la o temperatură a aerului ambiental mai mică decât temperatura de autoaprindere, iar pentru ca acest proces să aibă loc, combustibilul trebuie să fie incalzit din exterior. Pe baza cauzelor arderii spontane a substanțelor, se disting trei mecanisme ale acestui proces - microbiologic, termic și chimic, precum și diferitele combinații ale acestora.
Procesele microbiologice de ardere spontană sunt cauza principală a arderii spontane a substanțelor de origine vegetală, cum ar fi fânul subuscat, rumegușul, frunzele uscate, bumbacul.
Procesele microbiologice explică și arderea spontană a turbei măcinate. Activitatea vitală a bacteriilor și ciupercilor în gât poate începe deja la 10 - 18 ° C și se termină la 70 ° C. Mediul nutritiv pentru bacterii sunt substanțele solubile în apă formate ca urmare a degradarii plantelor.
Materialele subuscate sunt deosebit de predispuse la arderea spontană, deoarece umiditatea și căldura contribuie la activitatea vitală a microorganismelor. Conductibilitatea termică scăzută a materialelor vegetale duce și la încălzire. La o temperatură care depășește 75 "C, microorganismele, de regulă, mor, dar creșterea temperaturii nu se oprește, deoarece la 70 ° C unele substanțe organice pot fi carbonizate. Cărbunele poros rezultat adsorb gaze și tată și procesul de autoîncălzire. continuă.La 200 ° C începe să se descompună fibrele, care fac parte din uleiurile vegetale, ceea ce duce la o intensificare suplimentară a oxidării și la apariția arderii spontane.
Autoaprinderea termică este inerentă substanțelor dispersate cu o suprafață foarte dezvoltată, capabile să adsorbă oxigenul și să reacționeze cu acesta, în timp ce schimbul de căldură al substanțelor cu mediul extern nu este intens.
Se știe că cărbunii fosili (cărbuni brun și cărbune tare) depozitați în grămezi sau stive sunt predispuși la ardere spontană. Motivul arderii spontane este capacitatea cărbunilor de a oxida și adsorbi vapori și gaze la temperaturi scăzute.
Autoîncălzirea cărbunelui care apare în stive are loc mai întâi pe întregul volum al stivei, excluzând stratul superior (30 - 50 cm). Odată cu creșterea temperaturii, procesul de autoîncălzire capătă un caracter de cuibărit. Până la 60 °C, temperatura crește foarte lent - ventilația intensivă împiedică creșterea acesteia. Cu toate acestea, începând de la 60 °C, viteza de autoîncălzire crește brusc. Această temperatură este considerată critică pentru cărbune.
Arderea spontană a cărbunilor este facilitată și de o creștere a gradului de măcinare a acestora și de prezența impurităților - pirita și umiditatea.
În arderea chimică spontană, o creștere a vitezei unei reacții chimice cu creșterea temperaturii este de mare importanță. Îndepărtarea insuficientă a căldurii contribuie la încălzirea materialului ca urmare a apariției proceselor oxidative și, în consecință, la atingerea condițiilor critice pentru apariția arderii sau mocnit.
Substanțele chimice combustibile spontan pot fi împărțite în trei grupuri principale.
Mai multe despre tema arderii spontane:
- 5.4. Costul reproducerii și plata resurselor naturale
- 5.3. Evaluarea economică comparativă a resurselor naturale
- 4.3. Principalele direcții ale progresului științific și tehnologic și impactul acestora asupra protecției mediului și managementului rațional al naturii
Combustie- un proces fizic și chimic complex de transformare a componentelor unui amestec combustibil în produse de ardere cu degajare de radiații termice, lumini și energie radiantă. Aproximativ, natura arderii poate fi descrisă ca o oxidare viguroasă.
Arderea subsonică (deflagrația), spre deosebire de explozie și detonare, are loc la viteze mici și nu este asociată cu formarea unei unde de șoc. Arderea subsonică include propagarea normală a flăcării laminare și turbulente, iar arderea supersonică include detonarea.
Arderea este împărțită în termică și în lanț. Arderea termică se bazează pe o reacție chimică capabilă să continue cu auto-accelerare progresivă datorită acumulării căldurii degajate. Arderea în lanț are loc în unele reacții în fază gazoasă la presiuni scăzute.
Condițiile de autoaccelerare termică pot fi asigurate pentru toate reacțiile cu efecte termice și energii de activare suficient de mari.
Arderea poate începe spontan ca urmare a autoaprinderii sau poate fi inițiată prin aprindere. În condiții externe fixe, arderea continuă poate decurge în regim staționar, când principalele caracteristici ale procesului - viteza de reacție, viteza de eliberare a căldurii, temperatura și compoziția produsului - nu se modifică în timp, sau într-un mod periodic, când aceste caracteristici. fluctuează în jurul valorii lor medii. Datorită dependenței neliniare puternice a vitezei de reacție de temperatură, arderea este foarte sensibilă la condițiile externe. Aceeași proprietate a arderii determină existența mai multor regimuri staționare în aceleași condiții (efect de histerezis).
Există următoarele tipuri de ardere: autoaprindere, ardere spontană, flash, aprindere, explozie.
Autoaprindere- arderea rezultată din încălzirea exterioară a unei substanțe la o anumită temperatură fără contactul direct al substanței combustibile cu flacăra unei surse externe de ardere.
Combustie spontana- arderea solidelor rezultate din încălzirea lor sub influența proceselor care au loc în interiorul substanței în sine. Procesele fizice sau chimice aflate în desfășurare în interiorul substanței sunt asociate cu formarea de căldură, care accelerează procesul de oxidare, care se transformă în ardere cu foc deschis.
Flash- arderea rapidă, dar, în comparație cu o explozie, de scurtă durată a unui amestec de vapori a unei substanțe combustibile cu aer sau oxigen, rezultată dintr-o creștere locală a temperaturii, care poate fi cauzată de o scânteie electrică sau de atingerea unui amestec de o flacără sau un corp incandescent. Temperatura la care apare un fulger se numește punct de aprindere. Fenomenul fulgerului este similar cu fenomenul unei explozii, dar, spre deosebire de acesta din urmă, are loc fără un sunet puternic și nu are un efect distructiv.
Aprindere- aprinderea persistentă a unui amestec de vapori și gaze ale unei substanțe combustibile de la o creștere locală a temperaturii, care poate fi cauzată de atingerea unei flăcări sau a unui corp incandescent. Aprinderea poate dura până când întreaga cantitate de substanță combustibilă se arde, iar vaporizarea are loc datorită căldurii degajate în timpul arderii.
Aprinderea diferă de bliț în ceea ce privește durata sa. În plus, în timpul unei fulgerări, degajarea de căldură în fiecare secțiune este suficientă pentru a aprinde o secțiune adiacentă a unui amestec combustibil deja preparat, dar nu suficient pentru a o completa prin evaporarea unor noi cantități de combustibil; prin urmare, după epuizarea aportului de vapori combustibili, flacăra se stinge și fulgerul se termină acolo, până când vaporii combustibili se acumulează din nou și primesc supraîncălzire locală. Când este aprinsă, substanța care formează vapori este adusă la o astfel de temperatură încât căldura de ardere a vaporilor acumulați este suficientă pentru a restabili alimentarea amestecului combustibil.
Explozie- arderea sau descompunerea instantanee a unei substanțe, însoțită de eliberarea unei cantități uriașe de gaze, care se extind instantaneu și provoacă o creștere bruscă a presiunii în mediu. În contact cu aerul: produșii de descompunere gazoasă a anumitor substanțe au capacitatea de a se aprinde, ceea ce nu numai că duce la distrugere prin acțiunea undei de explozie, dar provoacă și incendii mari.
De asemenea, este izolată sinteza cu autopropagare la temperatură înaltă (SHS), un proces chimic care are loc cu eliberarea de căldură într-un mod de ardere automată și duce la formarea de produse solide. SHS este un mod de reacție exotermă în care eliberarea de căldură este localizată într-un strat și este transferată de la strat la strat prin transfer de căldură.
Trei factori sunt necesari pentru a se produce un incendiu:
- cald
- oxigen
- substanță combustibilă (combustibil)
Sensul întrebării este că numai atunci când aceste trei componente sunt prezente în proporția adecvată poate apărea o flacără.
Există, de asemenea, arderea fără flacără. Spre deosebire de arderea convențională, când se observă zone de flacără oxidantă și flacără reducătoare, este posibil să se creeze condiții pentru arderea fără flacără. Un exemplu este oxidarea catalitică a substanțelor organice pe suprafața unui catalizator adecvat, de exemplu, oxidarea etanolului pe negru de platină.
Un incendiu este o ardere necontrolată în afara unui focus special.
1. Substanță combustibilă (combustibil)
Substanțele (materialele) combustibile sunt substanțe (materiale) capabile să interacționeze cu un agent oxidant (oxigenul aerului) în modul de ardere. În funcție de combustibilitatea substanțelor (materialelor) sunt împărțite în trei grupe:
substanțe și materiale incombustibile care nu se pot autocombusti în aer;
substanțe și materiale cu ardere lentă - capabile să ardă în aer atunci când sunt expuse la energie suplimentară de la sursa de aprindere, dar nu sunt capabile să ardă independent după îndepărtarea acesteia;
substanțe și materiale combustibile – capabile să se autoarde după aprindere sau autoaprindere de ardere spontană.
Substanțe (materiale) combustibile este un concept condiționat, deoarece în alte moduri decât metodologia standard, substanțele și materialele necombustibile și cu ardere lentă devin adesea combustibile.
Printre substantele combustibile se numara substantele (materialele) in diverse stari de agregare: gaze, vapori, lichide, solide (materiale), aerosoli. Aproape toate substanțele chimice organice sunt inflamabile. Printre substanțele chimice anorganice se numără și substanțele combustibile (hidrogen, amoniac, hidruri, sulfuri, azide, fosfuri, amoniaați ai diverselor elemente).
Substanțele (materialele) combustibile sunt caracterizate de indicatori de pericol de incendiu. Prin introducerea diverșilor aditivi (promotori, retardanți de flacără, inhibitori) în compoziția acestor substanțe (materiale), este posibilă modificarea indicatorilor de pericol de incendiu într-o direcție sau alta.
2. Oxidant
Oxidantul este cealaltă parte a triunghiului de ardere. De obicei, oxigenul aerului acționează ca un agent oxidant în timpul arderii, dar pot exista și alți agenți oxidanți - oxizi de azot etc.
Indicatorul critic pentru oxigenul atmosferic ca agent oxidant este concentrația acestuia în aerul unui spațiu închis al vasului în limitele de volum de peste 12-14%. Sub această concentrație nu are loc arderea marii majorități a substanțelor combustibile. Cu toate acestea, unele substanțe combustibile sunt capabile să ardă chiar și la concentrații mai mici de oxigen în mediul înconjurător gaz-aer.
3.Temperatura de aprindere (caldura)
Există multe concepte aplicate temperaturilor la care aprinderea este posibilă. Cele mai importante dintre ele:
Punctul de aprindere este cea mai scăzută temperatură la care o substanță eliberează destui vapori inflamabili pentru a se aprinde atunci când este expusă la o flacără deschisă, dar arderea nu continuă.
Punctul de aprindere este cea mai scăzută temperatură la care o substanță produce suficienți vapori inflamabili pentru a se aprinde și a continua să ardă atunci când se aplică o flacără deschisă.
Notă. Se poate observa că diferența dintre punctul de aprindere și temperatura de ardere este că în primul caz are loc o fulgerare instantanee, iar în al doilea temperatura trebuie să fie suficient de mare pentru a produce suficienți vapori combustibili pentru ardere, indiferent de sursa de ardere. aprindere.
Autoaprinderea este auto-accelerarea rapidă a unei reacții chimice exoterme, care duce la apariția unei străluciri strălucitoare - o flacără. Autoaprinderea apare ca urmare a faptului că, atunci când materialul este oxidat de oxigenul din aer, se generează mai multă căldură decât are timp să fie îndepărtată în afara sistemului de reacție. Pentru substanțele combustibile lichide și gazoase, acest lucru are loc la parametrii critici de temperatură și presiune.
Este important să înțelegeți pe deplin cum se dezvoltă de obicei un incendiu. Dacă sunt excluse exploziile și fulgerările, procesul de ardere poate fi împărțit în următoarele patru perioade:
- perioada de plajă
- dezvoltarea incendiului
- perioada de ardere
- perioada de decădere
În acest sens, este semnificativ faptul că, de obicei, un incendiu se răspândește în sus foarte repede, lateral - la o viteză relativ mică, și în jos - foarte lent.
Acest lucru poate fi ilustrat după cum urmează: Dacă a avut loc arderea (triunghiul s-a închis), acțiunile de stingere a incendiului ar trebui să aibă ca scop aducerea indicatorilor triunghiului (cel puțin unul) dincolo de limitele valorilor critice - ruperea triunghiului de ardere. Aceasta este baza teoretică a arderii și stingerii.
În funcție de starea de agregare a componentelor combustibile (oxidant sau combustibil), se disting trei tipuri de ardere.
ardere omogenă- arderea gazelor şi a substanţelor combustibile vaporoase într-un oxidant gazos.
ardere eterogenă- arderea combustibililor lichizi si solizi (substante combustibile) intr-un oxidant gazos. O variație a arderii eterogene este arderea picăturilor lichide de combustibil.
Arderea explozivilor și a prafului de pușcă.
În funcție de viteza de propagare a flăcării, arderea este împărțită în deflagrație și detonare. Arderea prin deflagrație este un regim de ardere în care flacăra se propagă la viteze subsonice. În timpul detonării, flacăra se propagă cu viteză supersonică, de exemplu, în aer - cu o viteză mai mare de 300 m/s. Arderea subsonică este împărțită în laminară și turbulentă. Viteza de ardere laminară depinde de compoziția amestecului, de valorile inițiale ale temperaturii și presiunii, precum și de viteza transformărilor chimice în flacără. Viteza de propagare a unei flăcări turbulente, pe lângă acești factori, depinde de debitul, gradul și scara turbulenței.
Arderea spontană, apariția arderii ca urmare a autoîncălzirii materialelor solide combustibile, cauzată de autoaccelerarea în acestea exotermice. reactii. Arderea spontană are loc datorită faptului că degajarea de căldură în timpul reacțiilor este mai mare decât îndepărtarea căldurii către mediu.
Debutul arderii spontane se caracterizează prin temperatura de autoîncălzire (Tsn), care este temperatura minimă în condiții experimentale la care este detectată degajarea de căldură.
Când se atinge o anumită temperatură în procesul de auto-încălzire, numită temperatură de autoaprindere (Tsvoz), are loc arderea materialului, care se manifestă fie prin ardere mocnită, fie prin ardere în flăcări. În acest din urmă caz, Tsvoz este adecvat pentru temperatura de autoaprindere (Tsv), care în inginerie de incendiu este înțeleasă ca apariția arderii gazelor și lichidelor atunci când sunt încălzite la o anumită temperatură critică. (vezi Aprinderea în domeniul incendiilor). În principiu, arderea spontană și autoaprinderea sunt similare în esență fizică și diferă doar prin tipul de ardere, autoaprinderea are loc numai sub formă de ardere a flăcării.
În cazul autoaprinderii, autoîncălzirea (încălzirea pre-explozie) se dezvoltă în doar câteva grade și, prin urmare, nu este luată în considerare la evaluarea pericolului de incendiu și explozie al gazelor și lichidelor. În timpul arderii spontane, zona de autoîncălzire poate ajunge la câteva sute de grade (de exemplu, pentru turbă de la 70 la 225 °C). Ca urmare, fenomenul de autoîncălzire este întotdeauna luat în considerare la determinarea tendinței solidelor la ardere spontană.
Arderea spontană este studiată prin termostatarea materialului de testat la o temperatură dată și stabilirea relației dintre temperatura la care are loc arderea, dimensiunea probei și timpul în care este încălzită în termostat.
Procesele care au loc în timpul arderii spontane a probelor de materiale combustibile sunt prezentate în figură. La temperaturi de până la Tsn (ex. T1), materialul se încălzește neschimbat (fără generare de căldură). Când se atinge Tsn, în material apar reacții exoterme. Acesta din urmă, în funcție de condițiile de acumulare a căldurii (masa materialului, densitatea de ambalare a atomilor și moleculelor sale, durata procesului etc.), poate, după o perioadă de mică autoîncălzire după epuizarea componentele de autoîncălzire ale materialului, se încheie cu răcirea probei la temperatura inițială a termostatului (curba 1) sau continuă autoîncălzirea până la Tair (curba 2). Zona dintre Tsn și Tsvoz este potențial periculoasă de incendiu, sub Tsn este sigură.
Posibilitatea arderii spontane a unui material situat într-o zonă cu potențial pericol de incendiu se determină folosind ecuațiile:
unde Tamb este temperatura ambiantă, °С; l-determinarea dimensiunii (de obicei grosimea) materialului; t este timpul în care se poate produce arderea spontană; Factorul A1, n1 și A2, n2 determinat pentru fiecare material conform datelor experimentale.
Conform ecuației (1), la un l dat se găsește Tacr, la care se poate produce arderea spontană a acestui material, conform ecuației (2), cu un Tacr cunoscut, valoarea lui m. La o temperatură mai mică decât cea calculată. Tacr, sau la t mai mic decât timpul calculat prin ecuația (2), arderea spontană nu va avea loc.
În funcție de natura procesului inițial care a provocat autoîncălzirea materialului și de valorile Tsn, se distinge arderea spontană:
- chimic
- microbiologic
- termic
LA ardere chimică spontană includ interacțiunea exotermă a substanțelor (de exemplu, atunci când HNO3 concentrat ajunge pe hârtie, rumeguș etc.). Exemplul cel mai tipic și răspândit al unui astfel de proces este arderea spontană a cârpelor uleioase sau a altor materiale fibroase cu o suprafață dezvoltată. Mai ales periculoase sunt uleiurile care conțin compuși cu legături chimice nesaturate și care se caracterizează printr-un număr mare de iod (bumbac, floarea soarelui, iută etc.). Fenomenele de ardere chimică spontană includ și aprinderea unui număr de substanțe (de exemplu, Al și Fe fin divizat, hidruri de Si, B și unele metale, compuși organometalici - organoaluminiu etc.) la contactul cu aerul în absența Incalzi. Capacitatea substanțelor de a se aprinde spontan în astfel de condiții se numește piroforicitate. Particularitatea substanțelor piroforice este că Tdv (sau Tb) lor este sub temperatura camerei: - 200°C pentru SiH4, - 80°C pentru A1(C2H5)3. Pentru a preveni arderea chimică spontană, procedura de depozitare în comun a substanțelor și materialelor combustibile este strict reglementată.
Există, de asemenea, un tip de reacții chimice ale substanțelor, care este asociat cu interacțiunea cu apa sau umiditatea. În același timp, se eliberează și o temperatură suficientă pentru arderea spontană a substanțelor și materialelor. Exemple sunt substanțe precum potasiul, sodiul, carbura de calciu, varul nestins, etc. O caracteristică a metalelor alcalino-pământoase este capacitatea lor de a arde chiar și fără oxigen. Ei înșiși produc oxigenul necesar reacției, împărțind umiditatea aerului în hidrogen și oxigen sub influența temperaturii ridicate. De aceea stingerea unor astfel de substanțe cu apă duce la o explozie a hidrogenului rezultat.
predispus la ardere microbiologică spontană posedă materiale combustibile, mai ales umede, servind drept mediu nutritiv pentru microorganismele a căror activitate vitală este asociată cu degajarea de căldură (turbă, rumeguș etc.). Din acest motiv, un număr mare de incendii și explozii apar atunci când produsele agricole (de ex. siloz, fân umed) sunt depozitate în silozuri. Pentru arderea spontană microbiologică și chimică, este caracteristic ca Tsn să nu depășească valorile obișnuite ale Tacr și poate fi negativ. Materialele cu TSN peste temperatura camerei sunt capabile de ardere termică spontană.
În general, multe materiale solide cu o suprafață dezvoltată (de exemplu, fibroase) au tendința la toate tipurile de ardere spontană, precum și unele substanțe lichide și în topire care conțin compuși nesaturați depuși pe o suprafață dezvoltată (inclusiv necombustibilă). Calculul condițiilor critice pentru arderea spontană chimică, microbiologică și termică se realizează conform ecuațiilor (1) și (2).
Datorită atracției Pământului în timpul arderii, are loc convecția (mișcarea aerului): aerul încălzit devine mai ușor și se repezi în sus, iar frigul de jos vine să-l înlocuiască. Acest flux de aer are ca rezultat un gradient de temperatură semnificativ de-a lungul flăcării.

Reprezentare schematică a flăcării unei lumânări care indică temperatura în diferitele sale puncte în timpul arderii în condiții normale
Prin urmare, flacăra unei lumânări în gravitate zero arată puțin diferit:

Culoarea galben-portocalie a vârfului flăcării în condiții normale se datorează strălucirii particulelor de funingine transportate în sus de fluxul de aer fierbinte în creștere. Funinginea este microparticule care conțin carbon care nu a avut timp să se ardă, de exemplu. se transformă în CO2. În imponderabilitate, flacăra lumânării este mai mică și nu la fel de fierbinte ca de obicei, pentru că. nu există suficient aer proaspăt care să conțină oxigen. Prin urmare, există foarte puțină funingine, deoarece. nu se formează la temperaturi sub 1000°C. Dar, chiar dacă ar fi suficient, și atunci, din cauza temperaturii scăzute, ar străluci în intervalul infraroșu, ceea ce înseamnă că culoarea flăcării în imponderabilitate este întotdeauna albăstruie.
Culoarea flăcării depinde și de ce elemente „ard” în ea. Temperatura ridicată a flăcării permite atomilor să sară pentru ceva timp în stări de energie mai înaltă, iar apoi, revenind la starea lor inițială, emit lumină de o anumită frecvență, care corespunde structurii învelișurilor de electroni ale acestui element. De exemplu, un arzător cu gaz arde cu o flacără albastră din cauza prezenței CO, monoxidului de carbon, iar flacăra galben-portocalie a unui chibrit se explică prin prezența sărurilor de sodiu în lemn.
Lista literaturii de bază pe această temă:
Literatura principală
1. Da.B. Zeldovich, G.I., G.I. Barenblatt, W.B. Librovici, G.M. Makhviladze. Teoria matematică a arderii și exploziei. M.: Nauka, 1980 - 478 p.
2. V.V. Pomerantsev, K.M. Arefiev, D.B. Akhmedov et al. Fundamentele teoriei practice a arderii. Leningrad: Energoatomizdat, Leningrad. Catedra, 1986 - 309 p.
3. Grishin A.M. Modelarea matematică a incendiilor forestiere și noi modalități de combatere a acestora. - Novosibirsk: Nauka, Sib. Catedra, 1992. - 408 p.
literatură suplimentară
1. Conceptul dezvoltării arderii și exploziei ca domeniu al progresului științific și tehnologic. Cernogolovka: Teritoriu, 2001.
2. Alekseev B.V., Grishin A.M. Un curs de prelegeri despre aerotermochimie. Partea 1. Elemente de teorie cinetică, termodinamică și cinetică chimică. Partea 2. Elemente ale unei teorii riguroase a coeficienților de transfer, teoria transferului de energie prin radiație și sistemul de bază de ecuații ale aerotermochimiei. Tomsk: Editura Vol. universitate 1971.
3. Volokitina A.V., Sofronov M.A. Clasificarea și cartografierea materialelor combustibile din plante. Novosibirsk: Editura Nauka, Sib. Departamentul Academiei Ruse de Științe, 2002 - 306 p.