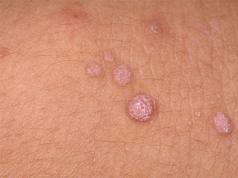
Defecte ale cristalelor. Cristalul este plin de defecte. Cum afectează defectele rezistența cristalelor. Ei scad puterea de sute, mii de ori. Dar, pe măsură ce deformarea cristalului crește, crește și numărul de defecte ale acestuia. Și din moment ce defectele interacționează între ele, cu cât sunt mai multe, cu atât le este mai dificil să se miște în cristal. Se dovedește un paradox: dacă există un defect în cristal, cristalul este deformat și distrus mai ușor decât dacă nu există niciun defect. Și dacă sunt prea multe defecte, atunci cristalul devine din nou puternic și cu cât sunt mai multe defecte, cu atât este mai ordonat. Deci, dacă învățăm să controlăm numărul și localizarea defectelor, putem controla rezistența materialelor.
diapozitivul 21 din prezentare "Cristal". Dimensiunea arhivei cu prezentarea este de 1397 KB.Chimie clasa a 11-a
rezumatul altor prezentări„Clasificarea substanțelor” - Distribuiți substanțele. Substanțele simple sunt metalele. Aur. Zn. Sulf. Clasificarea substantelor. CO. Cl2. Metale și nemetale. Eliminați substanța care este de prisos conform caracteristicii de clasificare. Substanțele simple sunt nemetale. Na2o. O2. Argint. O.S.Gabrielyan. Clasa a 11a. Sortați substanțele în clase.
„Circulația elementelor în natură” – Bacteriile denitrificatoare. proteine vegetale. bacterii. Atmosfera. Fulger. Ciclul azotului. Cercul mare. Organisme în descompunere. Fosforul se găsește în diferite minerale sub formă de fosfation anorganic (PO43-). Fosforul face parte din genele și moleculele care transportă energia în celule. Forma dominantă a oxigenului în atmosferă este molecula de O2. Îngrășăminte artificiale cu fosfat; detergenti. Fosfații sunt solubili în apă, dar nu volatili.
"Chimia sistemelor dispersate" - Sistem dispersat solid - lichid. Ciocolata poroasa. cartilaj. Fum. Minerale. Mediul și faza sunt lichide. Ceramică. Syneresis determină perioada de valabilitate a gelurilor alimentare, medicale și cosmetice. În medicină. Bauturi acidulate. Sistem dispersat gaz-lichid. Smog. În industria alimentară. Cauciuc spumă. Zoli Geli. solutii adevarate. Polistiren. Suspensii. Sistem dispersat lichid - gaz. Geluri. Faza și mediul sunt ușor separate prin decantare.
„Sistemul periodic al chimiei” - I. Döbereiner, J. Dumas, chimistul francez A. Shancourtua, ing. chimiștii W. Odling, J. Mendeleev despre locul unui element într-un sistem; poziţia elementului este determinată de numerele perioadei şi grupelor. predicția „ekaaluminiu” (viitorul Ga, descoperit de P. Lecoq de Boisbaudran în 1875), „ecabor” (Sc, descoperit de omul de știință suedez L. Nilsson în 1879) și „ecasilience” (Ge, descoperit de către om de știință german K. Winkler în 1886). 1829 - „triade” Döbereiner 1850 „sisteme diferențiale” Pettenkofer și Dumas. 1864 Meyer - un tabel care arată raportul dintre greutățile atomice pentru mai multe grupuri caracteristice de elemente. Newlands - existența unor grupuri de elemente care sunt similare în proprietăți chimice. Kolchina N. 11 „A”. Legea periodică, Sistemul periodic al elementelor chimice a lui D. I. Mendeleev.
„Mijloace de igienă și cosmetică” - Ca detergent. Acțiunea celui de-al doilea grup de deodorante se bazează pe suprimarea parțială a proceselor de transpirație. Pentru artiști Pulbere Peroxid de hidrogen. Sensul cuvintelor. Pulberile cosmetice decorative sunt amestecuri multicomponente. Instrumente cosmetice. Realizat de: Svetlana Shesterikova, elevă în clasa a XI-a, gimnaziul nr. 186. Un pic de istorie. Eu pun în scenă. Funcții de detergent. Săpunuri și detergenți.
„Chimia argintului” - nitrat de argint sau lapis - cristale ale sistemului rombic. Negi după cauterizare cu nitrat de argint. Argint în artă. AgNO3 este foarte solubil. Și ce pericole este plină de un metal misterios? Formează aliaje cu multe metale. Majoritatea sărurilor de argint sunt ușor solubile în apă, iar toți compușii solubili sunt toxici. Tehnologii pentru obținerea argintului metalic pur.
slide 1
Fizica stării solide. Partea 2.
Cristale adevărate - (la fel ca „băieții adevărați”) sunt cristale perfecte care cresc în locuri greșite.

slide 2
Creșterea cristalelor Știți, desigur, că apa (sub presiune normală) îngheață la 0°. Dacă temperatura scade, atunci exact la 0 ° apa va începe să înghețe, se va transforma în cristale de gheață. Până când toată apa îngheață, temperatura ei nu va mai scădea. Dacă, pe de altă parte, un cristal de gheață este încălzit la 0°, acesta va rămâne neschimbat. De îndată ce temperatura ajunge la 0°, cristalul va începe imediat să se topească. Indiferent cât de mult ne-am încălzi în continuare, temperatura gheții nu va crește până când toată gheața nu se va topi. Numai când întregul cristal, topit, se transformă în apă (cu alte cuvinte, până când sistemul tuturor particulelor se dezintegrează), temperatura apei poate începe să crească. Orice substanță cristalină se topește și se cristalizează la un punct de topire strict definit: fier - la 1530 °, staniu - la 232 °, cuarț - la 1713 °, mercur - la minus 38 °. Solidele necristaline nu au un punct de topire constant (și, prin urmare, temperatura de cristalizare), atunci când sunt încălzite, se înmoaie treptat.

slide 3
Modalități de creștere a cristalelor Una dintre ele este răcirea unei soluții saturate fierbinți. La fiecare temperatură, nu mai mult de o anumită cantitate de substanță se poate dizolva într-o anumită cantitate de solvent (de exemplu, în apă). Dacă soluția se răcește lent, se formează puține nuclee și, treptat, crescând excesiv din toate părțile, se transformă în cristale frumoase de forma corectă. Odată cu răcirea rapidă, se formează multe nuclee, iar particulele din soluție se vor „turna” pe suprafața cristalelor în creștere, precum mazărea dintr-o pungă ruptă; desigur, cristalele corecte nu vor fi obținute în acest caz, deoarece particulele în soluție pur și simplu nu au timp să se „așeze” pe suprafața cristalului în locul lor. O altă metodă de obținere a cristalelor este îndepărtarea treptată a apei dintr-o soluție saturată. Substanța „în plus” cristalizează. Și în acest caz, cu cât apa se evaporă mai încet, cu atât se obțin mai bine cristalele.

slide 4
A treia metodă este creșterea cristalelor din substanțele topite prin răcirea lentă a lichidului. Când se folosesc toate metodele, cele mai bune rezultate se obțin dacă se folosește o sămânță - un mic cristal de forma corectă, care este plasat într-o soluție sau topitură. În acest fel, de exemplu, se obțin cristale de rubin. Creșterea cristalelor de pietre prețioase se realizează foarte lent, uneori de ani de zile. Dacă, totuși, pentru a accelera cristalizarea, atunci în loc de un cristal, va apărea o masă de cristale mici. Această metodă poate fi efectuată numai în dispozitive speciale. În prezent, mai mult de jumătate din cristalele importante din punct de vedere tehnic sunt crescute din topitură. Una dintre cele mai utilizate metode industriale pentru obținerea semiconductorilor și a altor monocristale este metoda Czochralski. Proiectat în 1918. Materialul sursă (încărcarea) este încărcat într-un creuzet refractar și încălzit până la o stare topită. Apoi, cristalul de sămânță sub formă de tijă subțire cu un diametru de câțiva mm este plasat într-un suport de cristal răcit și scufundat în topitură.

slide 5
Jan Czochralski (1885 - 1953) - chimist polonez, inventatorul metodei, acum cunoscută pe scară largă, de creștere a monocristalelor dintr-o topitură prin tragerea lor de pe o suprafață liberă, ulterior numită după el. Potrivit unor relatări, Czochralski și-a descoperit faimoasa metodă în 1916, când și-a scăpat accidental stiloul într-un creuzet de staniu topit. Străgând stiloul din creuzet, a descoperit că un fir subțire de tablă solidificată stătea în spatele stiloului metalic. Prin înlocuirea penei stiloului cu o bucată de metal microscopică, Czochralski s-a convins că firul de metal astfel format are o structură monocristalină. În experimentele conduse de Czochralski, au fost obținute cristale simple cu o dimensiune de aproximativ un milimetru în diametru și până la 150 cm în lungime.

slide 6
Defectele cristalelor Descriind structura cristalelor, am folosit până acum modelele lor ideale. Diferența dintre cristalele reale și cele ideale este că cristalele reale nu au o rețea cristalină obișnuită. Ele conțin întotdeauna încălcări ale periodicității stricte în aranjarea atomilor. Aceste tulburări se numesc defecte ale cristalelor. Defectele se formează în timpul creșterii cristalelor sub influența mișcării termice a moleculelor, influențelor mecanice, iradierii cu fluxuri de particule, datorită prezenței impurităților etc. Orice încălcare a simetriei translaționale a unui cristal - periodicitatea ideală a cristalului. zăbrele - se numește defect de cristal. Există mai multe tipuri de defecte după dimensiune. Și anume, există defecte zero-dimensionale (punct), unidimensionale (liniare), bidimensionale (plate) și tridimensionale (volumerice).

Slide 7
Defectele cristalelor zero-dimensionale (sau punctiforme) includ toate defectele care sunt asociate cu deplasarea sau înlocuirea unui grup mic de atomi (defecte intrinseci ale punctului), precum și cu impuritățile. Ele apar în timpul încălzirii, alierei, în procesul de creștere a cristalelor și ca urmare a expunerii la radiații. Poate fi realizat și ca urmare a implantării. Proprietățile unor astfel de defecte și mecanismele formării lor sunt cele mai studiate, inclusiv mișcarea, interacțiunea, anihilarea și evaporarea. Defectele, numite defecte punctiforme, apar atunci când unul dintre atomii rețelei cristaline este înlocuit cu un atom de impuritate (a), introducerea unui atom între nodurile rețelei (b) sau ca urmare a formării de locuri vacante - absența. a unui atom într-unul dintre nodurile rețelei (c).

Slide 8
Impuritățile de substituție, care înlocuiesc particulele substanței principale la locurile rețelei, sunt introduse în rețea cu atât mai ușor, cu atât razele atomice (ionice) ale impurității și ale substanței principale sunt mai apropiate. Impuritățile interstițiale ocupă interstiții și, în plus, cu cât este mai ușor, cu atât volumul spațiului dintre atomi este mai mare. Încorporați pot fi atât atomi intrinseci, cât și de impurități sau ioni care diferă de atomii principali ca mărime sau valență. Dacă un atom străin se află într-un loc, atunci este un defect de substituție; dacă se află la un interstițiu, atunci este un atom interstițial. Pozițiile de echilibru ocupate de atomii interstițiali depind de materialul și tipul rețelei. Atomii vecini din nodurile rețelei cristaline sunt oarecum deplasați, provocând o ușoară deformare. Posturile vacante sunt cel mai important tip de defecte punctuale; accelerează toate procesele asociate mișcării atomilor: difuzia, sinterizarea pulberilor etc. În metalele pure comercial, defectele punctiforme cresc rezistența electrică, dar aproape că nu au niciun efect asupra proprietăților mecanice. Numai la concentrații mari de defecte ale metalelor iradiate plasticitatea scade și alte proprietăți se modifică vizibil.

Slide 9
Cum apar defectele spot? Conform principiilor de bază ale fizicii statistice, chiar și atunci când energia cinetică medie a atomilor este foarte mică, va exista întotdeauna un anumit număr de atomi cu o energie mai mare, suficientă pentru a muta un atom dintr-un loc de rețea. Mișcându-se prin cristal și dând o parte din energia acestuia altor atomi, un astfel de atom poate fi localizat în interstiții. Combinația dintre un atom într-un interstițiu și un loc vacant se numește defect Frenkel (sau pereche Frenkel). Locul liber și atomul interstițial sunt legați de forțe elastice semnificative.
Defectele Frenkel apar cu ușurință în cristale care conțin goluri interatomice semnificative. Substanțele cu structura de diamant sau sare gemă pot servi ca exemplu de astfel de cristale.

Slide 10
Defectele punctului Schottky se găsesc în principal în cristalele compacte, unde formarea atomilor interstițiali este dificilă sau nefavorabilă energetic. Unii atomi din stratul apropiat de suprafață, ca urmare a mișcării termice, pot părăsi cristalul la suprafață (Fig.). Locul liber de la locul eliberat poate migra apoi în cea mai mare parte a cristalului. Formarea defectelor Schottky reduce densitatea cristalului, deoarece volumul acestuia crește la o masă constantă, în timp ce în timpul formării defectelor Frenkel, densitatea rămâne neschimbată, deoarece volumul întregului corp nu se modifică.
Walter Hermann Schottky (1886 - 1976) - celebrul fizician german, a inventat în 1915 tubul vidat cu grilă de ecranare și în 1919 tetrodul. În 1938, Schottky a formulat o teorie care prezice efectul Schottky, folosită acum în diodele Schottky.

diapozitivul 11
Astfel, deși reprezintă o secvență departe de a fi perfectă, ordonată și oarecum monotonă de ioni pozitivi și negativi alternativi, cristalele reale conțin o gamă largă de defecte punctiforme interesante, care, după cum vom vedea, pot afecta foarte mult multe dintre proprietățile lor. După cum am spus deja, acestea sunt defecte intrinseci, a căror concentrație depinde de temperatură și, în plus, defecte neintrinsece, de impurități, care sunt fie prezente întâmplător, fie adăugate intenționat în timpul creșterii cristalelor. Toate aceste defecte pot fi considerate cvasiparticule. La fel ca particulele reale în vid, ele se pot mișca și interacționa între ele pe distanțe lungi pentru a forma structuri mai complexe.

slide 12
Procese de transfer în cristale Se presupune adesea în mod eronat că compușii halogenuri alcalini obișnuiți, cum ar fi clorura de sodiu și clorura de potasiu, sunt izolatori, dar de fapt sunt conductori relativ buni, acest lucru este valabil mai ales la temperaturi ridicate. Faptul existenței conductivității, precum și faptul că atât autodifuzia, cât și difuzia ionilor de impurități apar destul de ușor în solidele ionice, servesc drept dovezi de nerefuzat ale prezenței defectelor punctuale în acestea. Multe dintre aceste materiale nu au conductivitate electronică - măsurătorile arată că conductivitatea se datorează migrării ionilor. Totuși, fără existența unor locuri libere sau a atomilor interstițiali, mișcarea ionilor într-un conductor ionic atât de clasic este imposibilă: aceasta ar necesita prea multă energie. Datorită defectelor și mișcărilor acestora (Fig.), procesul de mișcare a ionilor se transformă într-un schimb de locuri între ion și defect; în timp ce cantitatea de energie necesară scade.

diapozitivul 13
Difuzia (în latină diffusio - răspândire, răspândire, dispersie, interacțiune) este procesul de pătrundere reciprocă a moleculelor unei substanțe între moleculele alteia, ducând la alinierea spontană a concentrațiilor acestora în volumul ocupat. În unele situații, una dintre substanțe are deja o concentrație egală și se vorbește despre difuzia unei substanțe în alta. În acest caz, transferul unei substanțe are loc dintr-o zonă cu o concentrație mare într-o zonă cu o concentrație scăzută (de-a lungul gradientului de concentrație). În cristale pot difuza atât atomii de rețea intrinseci (autodifuzie sau homodifuzie), cât și atomii altor elemente chimice dizolvați în substanță (impuritate sau heterodifuzie), precum și defecte punctuale ale structurii cristaline - atomi interstițiali și vacante.

Slide 14
Difuzia este un proces la nivel molecular și este determinat de natura aleatorie a mișcării moleculelor individuale. Viteza de difuzie este deci proporțională cu viteza medie a moleculelor. Dacă într-un amestec de gaze masa unei molecule este de patru ori mai mare decât a celeilalte, atunci o astfel de moleculă se mișcă de două ori mai încet în comparație cu mișcarea sa într-un gaz pur. În consecință, rata sa de difuzie este, de asemenea, mai mică. Această diferență în ratele de difuzie între moleculele ușoare și cele grele este utilizată pentru a separa substanțe cu greutăți moleculare diferite. Un exemplu este separarea izotopilor. Dacă un gaz care conține doi izotopi este trecut printr-o membrană poroasă, izotopii mai ușori pătrund în membrană mai repede decât cei mai grei. Pentru o mai bună separare, procesul se desfășoară în mai multe etape. Acest proces a fost utilizat pe scară largă pentru a separa izotopii de uraniu (separarea 235U de cea mai mare parte a 238U). (În prezent, pentru separarea izotopilor de uraniu se folosește o metodă de centrifugare, în care un gaz care conține uraniu este rotit foarte repede și, datorită diferenței de masă a moleculelor, izotopii sunt separați, care sunt apoi transferați înapoi în metal.)

diapozitivul 15
Difuzia respectă fenomenologic legile lui Fick. Prima lege a lui Fick stabilește proporționalitatea fluxului de difuzie al particulelor cu gradientul concentrației lor; A doua lege a lui Fick descrie modificarea concentrației datorată difuziei. Fenomenul de difuzie a fost studiat pentru prima dată de omul de știință de la Wurzburg A. Fick folosind soluții de sare ca exemplu. Fick, printr-o cercetare atentă, a arătat că difuzarea liberă a soluțiilor de sare are loc conform legilor care sunt complet analoge cu legile propagării căldurii în solide.

slide 16
Difuzia în cristale Unele caracteristici cristalografice generale ale procesului de difuzie sunt destul de evidente dacă luăm în considerare geometria cristalului. În primul rând, difuzia are loc aproape întotdeauna treptat, iar lungimea „trepților” elementare este de ordinul unui diametru atomic, adică mai mulți angstromi. Atomii se deplasează sărind dintr-o poziție în rețea. În concluzie, aceste salturi elementare asigură mișcarea atomilor pe distanțe mari. Să aflăm care este mecanismul salturilor atomice individuale. Există mai multe scheme posibile: mișcarea locurilor vacante, mișcarea atomilor interstițiali sau un fel de schimb reciproc de locuri între atomi (Fig.).
Deplasări atomice care duc la difuzie: a – deplasarea locurilor vacante; b – mișcarea atomilor interstițiali; c – schimbul de locuri a doi atomi; d - schimb inel de locuri a patru atomi

Slide 17
Pe baza conceptului de defecte punctiforme în cristale, Frenkel a propus două mecanisme principale de difuzie în solide: vacant (Fig. a: un atom se mișcă, schimbând locuri cu un vacant) și interstițial (Fig. b: un atom se mișcă de-a lungul interstițiilor). Atomii mici (ca mărime) de impurități se mișcă în al doilea mod, iar restul în primul mod: acesta este cel mai comun mecanism de difuzie.
Yakov Ilici Frenkel (1894 - 1952) - om de știință sovietic, fizician teoretician, unul dintre fondatorii fizicii solidelor. Din 1921 până la sfârșitul vieții, Frenkel a lucrat la Institutul de Fizică și Tehnologie din Leningrad. Începând cu 1922, Frenkel a publicat o carte nouă literalmente în fiecare an. A devenit autorul primului curs de fizică teoretică din URSS.

Slide 18
Dislocații O dislocare este un defect liniar în rețeaua cristalină a unui solid, care este prezența unui semiplan atomic „extra”. Cel mai simplu model vizual al unei dislocare a marginilor este o carte cu o parte ruptă dintr-una dintre paginile interioare. Apoi, dacă paginile cărții sunt asemănate cu planurile atomice, atunci marginea părții rupte a paginii modelează linia de dislocare. Se face o distincție între dislocarea șurubului și a muchiei.

Slide 19
Pentru ca o dislocare să se formeze într-un cristal ideal, este necesar să se producă o deplasare într-o anumită parte a planului de alunecare
Densitatea de dislocare variază într-un interval larg și depinde de starea materialului. După recoacere atentă, densitatea de dislocare este scăzută; în cristalele cu o rețea cristalină puternic deformată, densitatea de dislocare atinge valori foarte mari.

Slide 20
Densitatea de dislocare determină în mare măsură plasticitatea și rezistența materialului. Dacă densitatea este mai mică decât o anumită valoare, atunci rezistența la deformare crește brusc, iar rezistența se apropie de cea teoretică. Astfel, o creștere a rezistenței se realizează prin crearea unui metal cu o structură fără defecte și, pe de altă parte, prin creșterea densității luxațiilor, care împiedică mișcarea acestora.

diapozitivul 21
În timpul deformării plastice, o parte a cristalului se mișcă față de cealaltă sub acțiunea tensiunilor de forfecare. Când sarcinile sunt îndepărtate, schimbarea rămâne, adică. apare deformarea plastică. Aplicarea unei tensiuni de forfecare duce la deplasarea unei dislocari de margine, iar deplasarea axei acesteia printr-o translație înseamnă o modificare a semiplanului care formează în prezent dislocarea. Mișcarea unei dislocări de margine prin întregul cristal va duce la o deplasare a unei părți a cristalului cu o distanță interatomică. Rezultatul este deformarea plastică a cristalului (Fig.), adică părțile cristalului sunt deplasate una față de alta printr-o translație.
Un metal aflat în stare tensionată, sub orice tip de încărcare, suferă întotdeauna solicitări normale și tangenţiale. Creșterea tensiunilor normale și de forfecare duce la consecințe diferite. Creșterea tensiunilor normale duce la fracturi fragile. Deformarea plastică este cauzată de solicitări tangenţiale.

slide 22
O creștere a rezistenței se realizează prin crearea unui metal cu o structură fără defecte, precum și prin creșterea densității luxațiilor, care împiedică mișcarea acestora. In prezent s-au creat cristale fara defecte - mustati de pana la 2 mm lungime, 0,5 ... 20 μm grosime - " mustati " cu o rezistenta apropiata de cea teoretica. Dislocațiile afectează nu numai rezistența și plasticitatea, ci și alte proprietăți ale cristalelor. Odată cu creșterea densității dislocațiilor, proprietățile lor optice se schimbă, iar rezistența electrică a metalului crește. Dislocațiile cresc viteza medie de difuzie într-un cristal, accelerează îmbătrânirea și alte procese, reduc rezistența chimică, prin urmare, ca urmare a tratării suprafeței cristalului cu substanțe speciale, se formează gropi în punctele de ieșire ale dislocațiilor.

slide 23
Epitaxia este o creștere regulată a unui material cristalin pe altul (din greacă επι - on și ταξισ - ordin), adică creșterea orientată a unui cristal pe suprafața altuia (substrat). Energia minimă este cheltuită dacă cristalul crește de-a lungul unei dislocații de șurub.

slide 24
Multumesc pentru atentie!
Defecte ale structurii cristaline Metale reale care sunt folosite ca structural
materiale, constau dintr-un număr mare de cristale de formă neregulată. Aceste
cristale
numit
boabe
sau
cristale,
dar
structura
policristaline sau granulare. Tehnologii de producție existente
prin urmare, metalele nu permit obținerea purității lor chimice ideale
metalele reale conțin atomi de impurități. Atomii de impurităţi sunt
una dintre principalele surse de defecte ale structurii cristaline. ÎN
În funcție de puritatea chimică, metalele sunt împărțite în trei grupe:
chimic pur - conținut 99,9%;
de înaltă puritate - conținut 99,99%;
ultrapur - continut 99,999%.
Atomii oricăror impurități în dimensiunea și structura lor brusc
diferă de atomii componentei principale, deci câmpul de forță din jur
astfel de atomi sunt distorsionați. În jurul oricăror defecte apare o zonă elastică.
distorsiunea rețelei cristaline, care este echilibrată de volum
cristal adiacent unui defect al structurii cristaline.
comune tuturor metalelor. Aceste încălcări ale structurii ideale a solidelor
au un impact semnificativ asupra lor fizică, chimică,
proprietăți tehnologice și operaționale. Fara folosire
de idei despre defecte ale cristalelor reale, este imposibil de studiat fenomenele
deformare plastică, întărire și rupere a aliajelor etc. Defecte
structura cristalină este convenabil clasificată în funcție de geometria lor
forma si marime:
cele de suprafață (bidimensionale) sunt mici într-o singură direcție și au
o formă plată - acestea sunt granițele boabelor, blocurilor și gemenelor, granițele domeniilor;
punct (zero-dimensional) sunt mici în toate cele trei dimensiuni, dimensiunile lor nu sunt
mai mult de câteva diametre atomice - acestea sunt locuri libere, atomi interstițiali,
atomi de impurități;
liniare (unidimensionale) sunt mici în două direcții, iar în a treia
direcție, sunt proporționale cu lungimea cristalului - acestea sunt luxații, lanțuri
locuri libere și atomi interstițiali;
volumetrice (tridimensionale) au în toate cele trei dimensiuni relativ
dimensiunile mari sunt neomogenități mari, pori, fisuri etc.; Defectele de suprafață sunt interfețe
între boabe individuale sau subgranule dintr-un metal policristalin, la
include și defecte de „ambalare” în cristale.
O limită de cereale este o suprafață pe ambele părți ale căreia
rețelele cristaline diferă ca orientare spațială. Acest
Suprafața este un defect bidimensional cu dimensiuni semnificative în
două dimensiuni, iar în a treia - dimensiunea sa este proporțională cu atomul. limite de cereale
sunt zone cu densitate mare de dislocare și inconsecvență
structuri ale cristalelor învecinate. Atomii de la limita cerealelor au o creștere
energie în comparație cu atomii din interiorul boabelor și, în consecință, mai mult
tind să se angajeze în diverse interacțiuni și reacții. La limitele cerealelor
nu există o aranjare ordonată a atomilor. La limitele de cereale în procesul de cristalizare a metalului se acumulează
diverse impurități, defecte, incluziuni nemetalice,
filme de oxid. Ca urmare, legătura metalică dintre boabe este ruptă.
iar rezistența metalului este redusă. Ca urmare a structurii perturbate a frontierei
slăbi sau întări metalul, ceea ce duce, respectiv, la
intergranular (intergranular) sau transcristalin (de-a lungul corpului cerealelor)
distrugere. Sub influența temperaturilor ridicate, metalul tinde să se reducă
energia de suprafață a limitelor de cereale datorită creșterii și contracției boabelor
întinderea granițelor lor. Sub acţiunea chimică a graniţei
sunt mai active și, ca urmare, daune corozive
începe de-a lungul granițelor de cereale (această caracteristică stă la baza microanalizei
metale la fabricarea secțiunilor subțiri).
Există o altă sursă de distorsiune a suprafeței cristalinului
structuri metalice. Boabele de metal sunt reciproc dezorientate de mai mulți
grade, fragmentele sunt dezorientate de minute, iar blocurile care alcătuiesc
fragmente sunt dezorientate reciproc doar pentru câteva secunde. Dacă
luați în considerare boabele la mărire mare, se dovedește că în interiorul acestuia
există zone neorientate una față de alta la un unghi de 15 „...30”.
O astfel de structură se numește bloc sau mozaic, iar zonele sunt numite blocuri.
mozaicuri. Proprietățile metalelor vor depinde atât de dimensiunile blocurilor și ale granulelor, cât și
iar din orientarea lor reciprocă. Blocurile orientate sunt combinate în fragmente mai mari în
care orientarea generală rămâne arbitrară, astfel, toate boabele
dezorientați unul față de celălalt. Odată cu creșterea temperaturii
dezorientarea cerealelor crește. Proces termic care determină diviziunea cerealelor
în fragmente se numește poligonizare.
Diferența de proprietăți în funcție de direcția metalelor este
numele este anizotropie. Anizotropia este caracteristică tuturor substanțelor cu
structură cristalină. Boabele sunt dispuse aleator în volum, așadar
există aproximativ acelaşi număr de atomi în direcţii diferite şi
proprietățile rămân aceleași, acest fenomen se numește cvasi-anizotropie
(fals - anizotropie). Defectele punctuale sunt mici în trei dimensiuni și dimensiuni
apropiindu-se de punct. Unul dintre cele mai frecvente defecte este
locuri libere, adică un loc neocupat de un atom (defect Schottky). În locul unui vacant
nod, un atom nou se poate mișca și un loc liber - se formează de-a lungul unei „găuri”.
Cartier. Pe măsură ce temperatura crește, crește concentrația locurilor vacante. Asa de
precum atomii. situat aproape de suprafata. poate ieși la suprafață
cristal. iar atomii le vor lua locul. mai departe de suprafata.
Prezența locurilor libere în rețea conferă mobilitate atomilor. acestea. le permite
se deplasează în procesul de autodifuziune și difuzie. și astfel oferă
influența asupra unor procese precum îmbătrânirea, separarea fazelor secundare etc.
Alte defecte punctuale sunt atomii dislocați
(defectul Frenkel), i.e. atomi de sine de metal care ies dintr-un nod
zăbrele și având loc undeva în interstiții. În același timp, pe loc
atomul în mișcare, se formează un loc vacant. Concentrarea unor astfel de defecte
mic. deoarece formarea lor necesită o cheltuială semnificativă de energie. În orice metal există atomi străini de impurități. ÎN
În funcție de natura impurităților și de condițiile de intrare a acestora în metal, acestea pot
să fie dizolvate în metal sau să fie sub formă de incluziuni separate. Pe
proprietățile metalelor sunt cele mai afectate de străine dizolvate
impurități ai căror atomi pot fi localizați în golurile dintre atomi
metal de bază - atomi interstițiali sau la nodurile rețelei cristaline
metal de bază - atomi de substituție. Dacă atomii de impuritate sunt semnificativ
mai puțini atomi ai metalului de bază, atunci formează soluții interstițiale și dacă
mai mult - apoi formează soluții de substituție. În ambele cazuri, rețeaua devine
defect și deformarea acestuia afectează proprietățile metalului. Defectele liniare sunt mici în două dimensiuni, în a treia pot
ajunge la lungimea cristalului (granulelor). Defectele liniare includ lanțuri
posturi vacante. atomi interstițiali și dislocații. Luxațiile sunt speciale
fel de imperfecțiuni în rețeaua cristalină. Din punctul de vedere al teoriei luxaţiilor
se iau în considerare transformările de rezistență, fază și structurale. dislocare
numită imperfecțiune liniară care formează o zonă în interiorul cristalului
schimb. Teoria luxației a fost aplicată pentru prima dată la mijlocul anilor treizeci
al secolului al XX-lea de către fizicienii Orovan, Polyani și Taylor pentru a descrie procesul
deformarea plastică a corpurilor cristaline. Utilizarea lui este permisă
explicați natura rezistenței și ductilității metalelor. Teoria luxaţiilor a dat
oportunitatea de a explica diferența uriașă dintre teoretic și practic
rezistența metalelor.
Principalele tipuri de luxații sunt marginea și șurubul. Regional
Se formează o dislocare dacă apare o încărcătură suplimentară în interiorul cristalului.
semiplanul atomilor, care se numește extraplan. Marginea ei este 1-1
creează un defect de rețea liniar numit dislocare a muchiei.
În mod convențional, se presupune că o luxație este pozitivă dacă este în partea superioară
parte a cristalului și este indicată prin semnul ” ”, dacă dislocarea este în partea inferioară
părți - „T“ negativ. Luxațiile aceluiași semn resping, și
dimpotriva – sunt atrasi. Marginea tensionată
luxaţia se poate deplasa de-a lungul cristalului (de-a lungul planului de forfecare) până când
ajunge la limita de cereale (bloc). În acest caz, se formează un pas cu o valoare de
o distanță interatomică. Forfecarea plasticului este o consecință
deplasarea treptată a luxaţiilor în plan
schimb. Propagarea alunecării de-a lungul unui plan
alunecarea are loc secvenţial. Fiecare
act elementar de mutare a unei luxații din
o poziție la alta se realizează prin
ruperea unui singur atom vertical
avioane. Pentru a muta luxațiile, aveți nevoie
efort mult mai mic decât pentru rigid
deplasarea unei părți a cristalului față de alta în planul de forfecare. La
mișcarea de dislocare de-a lungul direcției de forfecare prin întregul cristal
are loc o deplasare a părților sale superioare și inferioare de un singur interatomic
distanţă. Ca urmare a deplasării, dislocarea iese la suprafață
cristal și dispare. O treaptă de alunecare rămâne la suprafață. Dislocarea șurubului. Este format dintr-o forfecare incompletă a unui cristal de-a lungul
densitatea Q. Spre deosebire de o dislocare a muchiei, o dislocare a șurubului
paralel cu vectorul de deplasare.
Dislocările se formează în timpul cristalizării metalelor în timpul
''prăbușirea'' a unui grup de posturi vacante, precum și în procesul de deformare plastică
și transformări de fază. O caracteristică importantă a structurii de dislocare
sunt densitatea de dislocare. Densitatea de dislocare este înțeleasă ca
lungimea totală a luxațiilor l (vezi), pe unitatea de volum V
cristal (cm3). În acest fel. dimensiunea densității de dislocare, cm-2. La
metale recoapte - 106...108 cm-2. Cu plastic rece
deformare, densitatea de dislocare crește la 1011...1012 cm-2. Mai mult
densitatea mare de dislocare duce la apariţia microfisurilor şi
distrugerea metalelor.
În apropierea liniei de dislocare, atomii sunt deplasați de la
locurile lor şi reţeaua cristalină este distorsionată, ceea ce
determină formarea unui câmp de stres (deasupra liniei
luxații, rețeaua este comprimată, iar dedesubt este întinsă).
Valoarea unei singure deplasări a planurilor
caracterizat prin vectorul Burger b, care
reflectă atât valoarea absolută a deplasării, cât și valoarea acesteia
direcţie. desfășurare mixtă. Dislocarea nu se poate termina în interior
cristal fără a se conecta la o altă luxație. Aceasta rezultă din faptul că
dislocarea este limita zonei de forfecare, iar zona de forfecare este întotdeauna acolo
linie închisă, iar o parte a acestei linii poate trece de-a lungul exteriorului
suprafata de cristal. Prin urmare, linia de dislocare trebuie să se închidă
în interiorul cristalului sau se termină pe suprafața acestuia.
Când se formează limita zonei de forfecare (linia de dislocare abcdf).
secțiuni drepte paralele și perpendiculare pe vectorul forfecare și
un caz mai general al unei linii curbilinii de dislocare gh. Pe secțiunile ab, cd și
ef este o dislocare a muchiei; Separa
secțiunile liniei curbilinii de dislocare au muchie sau elicoidal
orientare, dar o parte a acestei curbe nu este nici perpendiculară, nici paralelă
vector de forfecare, iar în aceste zone există o dislocare a mixtei
orientare. Deformarea plastică a corpurilor cristaline este legată de cantitate
luxații, lățimea lor, mobilitatea, gradul de interacțiune cu defectele
zăbrele etc. Natura legăturii dintre atomi afectează plasticitatea
cristale. Deci, în nemetale cu legăturile lor direcționale rigide
luxațiile sunt foarte înguste, necesită solicitări mari pentru a începe - în 103
ori mai mare decât pentru metale. Ca urmare, fractură fragilă în nemetale
vine înaintea turei.
Principalul motiv pentru rezistența scăzută a metalelor reale este
prezența dislocațiilor și a altor imperfecțiuni în structura materialului
structură cristalină. Obținerea de cristale fără luxații
duce la o creștere bruscă a rezistenței materialelor.
Ramura din stânga a curbei corespunde creației
comis
fără luxații
filiform
cristale (așa-numitele „muștați”), putere
care este aproape de teoretic. Cu limitat
densitatea de dislocare și alte distorsiuni
cristalin
grătare
proces
forfecare
cu cât este mai ușor, cu atât mai multe luxații
este în cea mai mare parte a metalului. Una dintre caracteristicile unei dislocari este vectorul deplasare - vectorul
Burgeri. Vectorul Burgers este un vector suplimentar care trebuie să fie
intra în conturul descris în jurul luxației pentru a se închide
conturul corespunzător acestuia în rețeaua unui cristal ideal, deschis
din cauza luxaţiei. Conturul trasat de-a lungul rețelei din jurul șantierului, în
acolo unde există o luxație se va dovedi a fi neînchis (conturul Burgers). Decalaj
conturul caracterizează suma tuturor deplasărilor rețelei elastice acumulate în
zona din jurul luxației este vectorul Burgers.
Pentru o dislocare a muchiei, vectorul Burgers este perpendicular, în timp ce pentru un șurub
luxații – paralel cu linia de dislocare. Vectorul Burgers este măsura
distorsiunea rețelei cristaline datorită prezenței în acesta
luxaţii. Dacă o dislocare este introdusă într-un cristal printr-o forfecare pură, atunci vectorul
shift și este vectorul Burgers. Conturul burgerilor poate fi schimbat
de-a lungul liniei de dislocare, întins sau comprimat într-o direcție perpendiculară pe
liniile de dislocare, în timp ce mărimea și direcția vectorului Burgers
ramane constant. Odată cu creșterea tensiunilor, numărul surselor de dislocare în
metal și densitatea lor crește. Pe lângă luxaţiile paralele
luxaţiile apar în planuri şi direcţii diferite. Locații
se afectează reciproc, se împiedică reciproc să se amestece, apar
anihilarea (distrugerea reciprocă) etc. (care a permis lui J. Gordon la figurat
numesc interacţiunea lor în procesul de deformare plastică „intimă
viața luxațiilor”). Pe măsură ce densitatea luxațiilor crește, mișcarea lor
devine din ce în ce mai dificil, ceea ce necesită o creștere a aplicației
sarcina pentru a continua deformarea. Ca urmare, metalul este întărit, ceea ce
corespunde ramurii din dreapta a curbei.
Luxațiile, împreună cu alte defecte, participă la fază
transformările, recristalizarea, servesc ca centre gata făcute în timpul precipitațiilor
a doua fază dintr-o soluție solidă. De-a lungul luxațiilor, viteza de difuzie este
cu câteva ordine de mărime mai mare decât printr-o rețea cristalină fără defecte.
Dislocațiile servesc ca loc de concentrare a atomilor de impurități, în special
impurități interstițiale, deoarece aceasta reduce distorsiunea rețelei. Dacă sub influența forțelor externe apar dislocații în metal,
atunci proprietățile elastice ale metalului se modifică și influența începe să afecteze
semnul deformarii initiale. Dacă metalul este supus unei slabe
deformare plastică printr-o sarcină de același semn, apoi când semnul se schimbă
sarcină, o scădere a rezistenței la plasticul inițial
deformatii (efect Bauschinger).
Luxațiile care au apărut în timpul deformării primare provoacă
apariția în metal a tensiunilor reziduale, care, însumându-se cu
tensiunile de funcționare atunci când semnul sarcinii se modifică, provoacă o scădere
puterea de curgere. Cu o creștere a deformațiilor plastice inițiale
cantitatea de reducere a caracteristicilor mecanice crește.
efectul
Bauschinger
clar
apare
la
nesemnificativ
primar
călirea prin muncă.
Mic de statura
concediu de odihna
nituit
materiale
elimină toate manifestările
efectul Bauschinger. efectul
slăbit semnificativ de
multiplu
ciclic
Se încarcă
material
din
prezența plasticului mic
deformări de diferite semne. Toate defectele enumerate în structura cristalului conduc la
apariția tensiunilor interne. După volum, unde
sunt echilibrate disting tensiuni de tip I, II și III.
Tensiunile interne de primul fel sunt tensiuni zonale,
apărute între secțiuni individuale ale secțiunii sau între individ
părți ale unui detaliu. Acestea includ tensiunile termice care apar
în timpul încălzirii și răcirii accelerate în timpul sudării, tratament termic.
Tensiuni interne de al doilea fel - apar în interiorul bobului sau între
boabele învecinate se datorează structurii de dislocare a metalului.
Tensiuni interne de tip III - apar în interiorul volumului comenzii
mai multe celule elementare; sursele punctuale sunt sursa principală
defecte.
Tensiunile reziduale interne sunt periculoase deoarece
se adună la tensiunile reale de funcționare și poate duce la
defectarea prematură a structurii.
Defecte ale cristalelor
Orice cristal real nu are o structură perfectă și are o serie de încălcări ale rețelei spațiale ideale, care sunt numite defecte ale cristalelor.
Defectele cristalelor sunt împărțite în zero-dimensionale, unidimensionale și bidimensionale. Defectele zero-dimensionale (punctuale) pot fi împărțite în energie, electronice și atomice.
Cele mai frecvente sunt defectele energetice - fononi - distorsiuni temporare ale regularității rețelei cristaline cauzate de mișcarea termică. Defectele energetice ale cristalelor includ și imperfecțiuni temporare ale rețelei (stări excitate) cauzate de expunerea la diferite radiații: lumină, raze X sau radiații γ, radiații α, flux de neutroni.
Defectele electronice includ electroni în exces, lipsa de electroni (legături de valență neumplute într-un cristal - găuri) și excitoni. Acestea din urmă sunt defecte de pereche formate dintr-un electron și o gaură, care sunt cuplate de forțele Coulomb.
Defectele atomice se manifestă sub forma unor locuri libere (defecte Schottky, Fig. 1.37), sub forma deplasării unui atom dintr-un situs într-un interstițiu (defecte Frenkel, Fig. 1.38), sub forma unei inserții a unui atom sau ion străin în rețea (Fig. 1.39). În cristalele ionice, pentru a menține neutralitatea electrică a cristalului, concentrațiile defectelor Schottky și Frenkel trebuie să fie aceleași atât pentru cationi, cât și pentru anioni.
Defectele liniare (unidimensionale) ale rețelei cristaline includ dislocații (tradus în rusă, cuvântul „dislocare” înseamnă „deplasare”). Cele mai simple tipuri de luxații sunt luxațiile de margine și șurub. Caracterul lor poate fi judecat din Fig. 1,40-1,42.
Pe fig. 1.40, a arată structura unui cristal ideal sub forma unei familii de planuri atomice paralele între ele. Dacă unul dintre aceste planuri se rupe în interiorul cristalului (Fig. 1.40, b), atunci locul ruperii sale formează o dislocare a muchiei. În cazul unei dislocari cu șurub (Fig. 1.40, c), natura deplasării planurilor atomice este diferită. Nu există nicio rupere în interiorul cristalului niciunuia dintre planurile atomice, dar planurile atomice în sine sunt un sistem similar cu o scară în spirală. În esență, acesta este un plan atomic răsucit de-a lungul unei spirale. Dacă ocolim acest plan în jurul axei dislocației șurubului (linia întreruptă în Fig. 1.40, c), atunci cu fiecare tură ne vom ridica sau vom coborî cu un pas de șurub egal cu distanța interplanară.
Un studiu detaliat al structurii cristalelor (folosind un microscop electronic și alte metode) a arătat că un singur cristal este format dintr-un număr mare de blocuri mici, ușor dezorientate unul față de celălalt. Rețeaua spațială din interiorul fiecărui bloc poate fi considerată destul de perfectă, dar dimensiunile acestor regiuni de ordine ideală în interiorul cristalului sunt foarte mici: se crede că dimensiunile liniare ale blocurilor se află în intervalul de la 10-6 la 10-4. cm.
Orice luxație specială poate fi reprezentată ca o combinație de dislocații de margine și șurub.
Defectele bidimensionale (plane) includ granițele dintre granulele de cristal și șirurile de dislocații liniare. Suprafața cristalului în sine poate fi, de asemenea, considerată un defect bidimensional.
Defecte punctuale, cum ar fi locurile libere, există în fiecare cristal, indiferent cât de atent este cultivat. Mai mult, într-un cristal adevărat, locurile libere apar și dispar în mod constant sub acțiunea fluctuațiilor termice. Conform formulei Boltzmann, concentrația de echilibru a locurilor vacante pv într-un cristal la o temperatură dată (T) se determină după cum urmează:
unde n este numărul de atomi pe unitatea de volum a cristalului, e este baza logaritmilor naturali, k este constanta Boltzmann, Ev este energia formării locurilor libere.
Pentru majoritatea cristalelor, energia de formare a golului este aproximativ egală cu 1 eV, la temperatura camerei kT » 0,025 eV,
Prin urmare,
Pe măsură ce temperatura crește, concentrația relativă a locurilor libere crește destul de rapid: la T = 600°K ajunge la 10–5, iar la 900°K–10–2.
Considerații similare pot fi făcute în ceea ce privește concentrația defectelor după Frenkel, ținând cont de faptul că energia de formare a implanturilor este mult mai mare (de ordinul a 3–5 eV).
Deși concentrația relativă a defectelor atomice poate fi mică, modificările proprietăților fizice ale cristalului cauzate de acestea pot fi enorme. Defectele atomice pot afecta proprietățile mecanice, electrice, magnetice și optice ale cristalelor. Ca o ilustrare, vom da doar un exemplu: miimi dintr-un procent atomic din unele impurități din cristalele semiconductoare pure își schimbă rezistența electrică de 105-106 ori.
Dislocațiile, fiind defecte extinse ale unui cristal, acoperă cu câmpul lor elastic al unei rețele distorsionate un număr mult mai mare de noduri decât defectele atomice. Lățimea miezului de dislocare este de doar câteva perioade de rețea, în timp ce lungimea sa atinge multe mii de perioade. Energia dislocațiilor este estimată a fi de ordinul a 4 10 -19 J la 1 m de lungime a dislocației. Energia de dislocare calculată pe o distanță interatomică de-a lungul lungimii de dislocare pentru diferite cristale se află în intervalul de la 3 la 30 eV. O energie atât de mare necesară pentru a crea dislocații este motivul pentru care numărul lor este practic independent de temperatură (atermicitatea dislocației). Spre deosebire de posturile vacante [cf. formula (1.1), probabilitatea de apariție a dislocărilor datorate fluctuațiilor mișcării termice este dispărut de mică pentru întregul interval de temperatură în care este posibilă starea cristalină.
Cea mai importantă proprietate a luxațiilor este mobilitatea lor ușoară și interacțiunea activă între ele și cu orice alte defecte ale rețelei. Fără a lua în considerare mecanismul mișcării de dislocare, subliniem că, pentru a provoca mișcarea de dislocare, este suficient să se creeze un mic efort de forfecare de ordinul a 0,1 kg/mm2 în cristal. Deja sub influența unui astfel de stres, dislocația se va deplasa în cristal până când va întâlni orice obstacol, care poate fi o limită de granule, o altă dislocare, un atom interstițial etc. Când întâlnește un obstacol, dislocația se îndoaie, ocolește. obstacolul, formând o buclă de dislocare în expansiune, care este apoi atașată și formează o buclă de dislocare separată, iar în zona unei bucle de dislocare separată rămâne un segment de dislocare liniară (între două obstacole), care, sub influența unui stres extern suficient, se va îndoi din nou și întregul proces se va repeta din nou. Astfel, se poate observa că interacțiunea luxațiilor în mișcare cu obstacole conduce la creșterea numărului de luxații (înmulțirea lor).
În cristalele metalice neformate, 106-108 luxații trec printr-o zonă de 1 cm2; în timpul deformării plastice, densitatea dislocației crește de mii și uneori de milioane de ori.
Să luăm în considerare efectul defectelor cristalului asupra rezistenței sale.
Puterea unui cristal ideal poate fi calculată ca forța necesară pentru a rupe atomi (ioni, molecule) unul de celălalt, sau pentru a le deplasa, depășind forțele de coeziune interatomică, adică, puterea ideală a unui cristal ar trebui determinată de produsul mărimii forțelor legăturii interatomice cu numărul de atomi pe unitatea de suprafață a secțiunii transversale corespunzătoare a cristalului. Rezistența la forfecare a cristalelor reale este de obicei cu trei până la patru ordine de mărime mai mică decât rezistența ideală calculată. O scădere atât de mare a rezistenței cristalului nu poate fi explicată printr-o scădere a ariei secțiunii transversale de lucru a probei din cauza porilor, cavităților și microfisurilor, deoarece dacă rezistența este slăbită cu un factor de 1000, cavitățile ar trebui să ocupe 99,9% din aria secțiunii transversale a cristalului.
Pe de altă parte, rezistența probelor monocristaline, în întregul volum al cărora se păstrează aproximativ aceeași orientare a axelor cristalografice, este semnificativ mai mică decât rezistența unui material policristalin. De asemenea, se știe că, într-un număr de cazuri, cristalele cu un număr mare de defecte au o rezistență mai mare decât cristalele cu un număr mai mic de defecte. Oțelul, de exemplu, care este fier „stricat” de impuritățile de carbon și alți aditivi, are proprietăți mecanice semnificativ mai mari decât fierul pur.
Imperfecțiunea cristalelor
Până acum, am considerat cristale ideale. Acest lucru ne-a permis să explicăm o serie de caracteristici ale cristalelor. De fapt, cristalele nu sunt perfecte. Ele pot conține un număr mare de defecte diverse. Unele proprietăți ale cristalelor, în special electrice și altele, depind și de gradul de perfecțiune al acestor cristale. Astfel de proprietăți se numesc proprietăți sensibile structural. Există 4 tipuri principale de imperfecțiuni într-un cristal și un număr de altele non-bazice.
Principalele imperfecțiuni includ:
1) defecte punctuale. Acestea includ locuri goale din rețea (locuri vacante), atomi interstițiali suplimentari și defecte de impurități (impurități substituționale și interstițiale).
2) Defecte liniare.(luxații).
3) defecte ale avionului. Acestea includ: suprafețe de tot felul de alte incluziuni, fisuri, suprafață exterioară.
4) Defecte de volum. Acestea includ incluziunile în sine, impurități străine.
Imperfecțiunile care nu sunt majore includ:
1) Electronii și găurile sunt defecte electronice.
2) Fononi, fotoni și alte cvasiparticule care există într-un cristal pentru un timp limitat
Electroni și găuri
De fapt, ele nu au afectat spectrul energetic al cristalului în starea neexcitată. Totuși, în condiții reale, la T¹0 (temperatura absolută), electronii și găurile pot fi excitați în rețea însăși, pe de o parte, iar pe de altă parte, pot fi injectați (introduși) în ea din exterior. Astfel de electroni și găuri pot duce, pe de o parte, la deformarea rețelei în sine și, pe de altă parte, datorită interacțiunii cu alte defecte, perturbă spectrul de energie al cristalului.
Fotonii
Ele nu pot fi considerate adevărate imperfecțiuni. Deși fotonii au o anumită energie și impuls, dacă această energie nu este suficientă pentru a genera perechi electron-gaură, atunci în acest caz cristalul va fi transparent pentru foton, adică va trece liber prin el, fără a interacționa cu materialul. Este inclus în clasificare deoarece pot afecta spectrul de energie al cristalului prin interacțiunea cu alte imperfecțiuni, în special cu electronii și găurile.
Imperfecțiuni punctuale (defect)
La T¹0, se poate dovedi că energia particulelor de la nodurile rețelei cristaline va fi suficientă pentru a transfera particula dintr-un nod într-un interstițiu. La care fiecare temperatură specifică va corespunde propriei concentrații specifice de astfel de defecte punctuale. O parte din defecte se vor forma din cauza transferului de particule de la noduri la interstiții, iar unele dintre ele se vor recombina (scăderea concentrației) datorită trecerii de la interstiții la noduri. Datorită egalității debitelor, fiecare temperatură va avea propria sa concentrație de defecte punctuale. Un astfel de defect, care este o combinație între un atom interstițial și site-ul liber rămas), cancia) este un defect Frenkel. O particulă din stratul apropiat de suprafață, din cauza temperaturii, poate ajunge la suprafață), suprafața este o chiuvetă nesfârșită a acestor particule). Apoi se formează un loc liber (loc liber) în stratul apropiat de suprafață. Acest site liber poate fi ocupat de un atom mai adânc, ceea ce este echivalent cu mișcarea locurilor vacante adânc în cristal. Astfel de defecte se numesc defecte Schottky. Ne putem imagina următorul mecanism de formare a defectelor. Particula de la suprafață se deplasează în adâncimea cristalului și în grosimea cristalului apar atomi interstițiali suplimentari fără locuri libere. Astfel de defecte se numesc defecte anti-Scotkian.
Formarea defectelor punctuale
Există trei mecanisme principale pentru formarea defectelor punctiforme într-un cristal.
întărire. Cristalul este încălzit la o temperatură semnificativă (ridicat), în timp ce fiecare temperatură corespunde unei concentrații bine definite de defecte punctiforme (concentrație de echilibru). La fiecare temperatură se stabilește o concentrație de echilibru a defectelor punctiforme. Cu cât temperatura este mai mare, cu atât concentrația de defecte punctiforme este mai mare. Dacă materialul încălzit în acest fel este răcit brusc, atunci acest exces de defecte punctiforme se va dovedi a fi înghețat, ceea ce nu corespunde acestei temperaturi scăzute. Astfel, se obține un exces față de concentrația de echilibru a defectelor punctiforme.
Impactul asupra cristalului de către forțe externe (câmpuri). În acest caz, cristalului este furnizată energie suficientă pentru formarea defectelor punctiforme.
Iradierea unui cristal cu particule de înaltă energie. Trei efecte principale sunt posibile datorită iradierii externe într-un cristal:
1) Interacțiunea elastică a particulelor cu o rețea.
2) Interacțiunea inelastică (ionizarea electronilor din rețea) a particulelor cu rețeaua.
3) Toate transmutările (transformațiile) nucleare posibile.
În al 2-lea și al 3-lea efect, primul efect este întotdeauna prezent. Aceste interacțiuni elastice au un dublu efect: pe de o parte, se manifestă sub formă de vibrații elastice ale rețelei, ducând la formarea de defecte structurale, pe de altă parte. În acest caz, energia radiației incidente trebuie să depășească energia de prag pentru formarea defectelor structurale. Această energie de prag este de obicei de 2-3 ori mai mare decât energia necesară pentru formarea unui astfel de defect structural în condiții adiabatice. În condiții adiabatice pentru siliciu (Si), energia de formare adiabatică este de 10 eV, energia de prag este de 25 eV. Pentru formarea unui gol în siliciu, este necesar ca energia radiației externe să fie de cel puțin 25 eV, și nu 10 eV ca în cazul procesului adiabatic. Este posibil ca la energii semnificative ale radiației incidente, o particulă (1 cuantă) să conducă la formarea nu a unuia, ci a mai multor defecte. Procesul poate fi în cascadă.
Concentrarea defectelor punctuale
Să găsim concentrația de defecte după Frenkel.
Să presupunem că există N particule la nodurile rețelei cristaline. Dintre acestea, n particule s-au mutat de la noduri la internod. Fie energia de formare a defectului Fresnel să fie Eph. Atunci probabilitatea ca încă o particulă să se deplaseze de la un nod la un internod va fi proporțională cu numărul de particule care se află încă în noduri (N-n) și cu factorul Boltzmann, adică ~. Și numărul total de particule care au trecut de la noduri la internod ~. Să găsim numărul de particule care trec de la interstiții la noduri (recombine). Acest număr este proporțional cu n și este proporțional cu numărul de locuri libere din noduri, sau mai degrabă cu probabilitatea ca particula să se împiedice de un nod gol, (adică ~). ~. Atunci modificarea totală a numărului de particule va fi egală cu diferența dintre aceste cantități:
În timp, fluxurile de particule de la noduri la interstiții și în direcția opusă vor deveni egale între ele, adică se stabilește o stare staționară. Deoarece numărul de particule din interstiții este mult mai mic decât numărul total de noduri, atunci n poate fi neglijat și. De aici găsim
este concentrația Frenkel de defecte, unde a și b sunt coeficienți necunoscuți. Folosind o abordare statistică a concentrației de defecte după Frenkel și ținând cont de faptul că N' este numărul de interstiții, putem găsi concentrația de defecte după Frenkel: , unde N este numărul de particule, N' este numărul a interstiţiilor.
Procesul de formare a defectelor conform lui Frenkel este un proces bimolecular (proces în două părți). În același timp, procesul de formare a defectelor conform Schottky este un proces monomolecular.
Un defect Schottky reprezintă un post vacant. După ce am efectuat raționament similar cu concentrația defectului Frenkel, obținem concentrația defectului Schottky în următoarea formă: , unde nsh este concentrația defectului Schottky, Esh este energia de formare a defectului Schottky. Deoarece procesul de formare Schottky este monomolecular, spre deosebire de defectele Frenkel, în numitorul exponentului nu există exponent 2. Procesul de formare, de exemplu, defectele Frenkel, este caracteristic cristalelor atomice. Pentru cristalele ionice, defectele, de exemplu, conform lui Schottky, pot fi formate doar în perechi. Acest lucru se datorează faptului că, pentru a menține neutralitatea electrică a cristalului ionic, este necesar ca perechi de ioni de semn opus să iasă simultan la suprafață. Adică concentrația unor astfel de defecte de pereche poate fi reprezentată ca un proces bimolecular: . Acum putem găsi raportul dintre concentrațiile de defecte după Frenkel și concentrația de defecte după Schottky: ~. Energia de formare a defectelor de pereche conform Schottky Er și energia de formare a defectelor conform Frenkel Ef au o valoare de aproximativ 1 eV și pot diferi unele de altele de ordinul a câteva zecimi de eV. KT pentru temperatura camerei are o valoare de ordinul a 0,03 eV. Apoi ~. Prin urmare, pentru un anumit cristal, va predomina un anumit tip de defecte punctiforme.
Viteza de mișcare a defectelor din cristal
Difuzia este procesul de mișcare a particulelor într-o rețea cristalină pe distanțe macroscopice din cauza fluctuațiilor (modificărilor) energiei termice. Dacă particulele în mișcare sunt particule ale rețelei în sine, atunci vorbim despre autodifuziune. Dacă particulele care sunt extraterestre participă la mișcare, atunci vorbim de heterodifuzie. Mișcarea acestor particule în rețea poate fi efectuată prin mai multe mecanisme:
Datorită mișcării atomilor interstițiali.
Datorită mișcării posturilor vacante.
Datorită schimbului reciproc de locuri de atomi interstițiali și de locuri libere.
Difuzia datorată mișcării atomilor interstițiali
De fapt, are două etape:
Un atom interstițial trebuie să se formeze în rețea.
Atomul interstițial trebuie să se miște în rețea.
Poziția la interstiții corespunde energiei potențiale minime
Exemplu: avem o rețea spațială. Particulă în interstiții.
Pentru ca o particulă să treacă de la un interstițiu la altul, trebuie să depășească o barieră potențială cu o înălțime Em. Frecvența salturilor de particule de la un interstițiu la altul va fi proporțională. Fie frecvența de oscilație a particulelor să corespundă interstițiilor v. Numărul de interstiții învecinate este egal cu Z. Atunci frecvența de sărituri este: .
Difuzia din cauza moțiunilor de posturi vacante
Procesul de difuzare din cauza posturilor vacante este, de asemenea, unul în 2 etape. Pe de o parte, locurile vacante trebuie formate, pe de altă parte, trebuie să se mute. Trebuie remarcat faptul că spațiul liber (loc liber) în care particula se poate mișca există, de asemenea, doar o anumită fracțiune de timp proporțional, unde Ev este energia formării locurilor libere. Și frecvența salturilor va arăta astfel: , unde Em este energia de mișcare a locurilor vacante, Q=Ev+Em este energia de activare a difuziei.
Mișcarea particulelor pe distanțe lungi
Luați în considerare un lanț de atomi identici.
Să presupunem că avem un lanț de atomi identici. Sunt situate la o distanta d una de alta. Particulele se pot deplasa spre stânga sau spre dreapta. Deplasarea medie a particulelor este 0. Datorită echiprobabilității mișcării particulelor în ambele direcții:
Să găsim deplasarea pătratică medie:
unde n este numărul de tranziții ale particulelor, poate fi exprimat. Apoi. Valoarea este determinată de parametrii materialului dat. Prin urmare, notăm: - coeficient de difuzie, ca urmare:
În cazul 3D:
Înlocuind aici valoarea lui q, obținem:
Unde D0 este factorul de frecvență de difuzie, Q este energia de activare a difuziei.
Difuziunea macroscopică
Luați în considerare o rețea cubică simplă:
Mental, între planurile 1 și 2, selectăm condiționat planul 3. și găsim numărul de particule care traversează acest semiplan de la stânga la dreapta și de la dreapta la stânga. Fie ca frecvența de salt a particulelor să fie egală cu q. Apoi, într-un timp egal cu semiplanul 3, particulele vor traversa din partea semiplanului 1. În mod similar, în același timp, particulele vor intersecta semiplanul selectat din partea semiplanului 2. Apoi, în timpul t, modificarea numărului de particule din semiplanul selectat poate fi reprezentată astfel: . Să găsim concentrația de particule - impurități în semiplanurile 1 și 2:
Diferența dintre concentrațiile de volum ale C1 și C2 poate fi exprimată astfel:
Luați în considerare un singur strat selectat (L2=1). Știm că este coeficientul de difuzie, atunci:
- Prima lege a difuziei a lui Fick.
În mod similar, formula pentru cazul tridimensional. Numai în locul coeficientului de difuzie unidimensional, înlocuim cazul tridimensional cu coeficientul de difuzie. Folosind această analogie de raționament pentru concentrație, și nu pentru numărul de purtători, ca în cazul precedent, se poate găsi a 2-a difuzie a lui Fick.
- A doua lege a lui Fick.
Legea a doua de difuzie a lui Fick este foarte convenabilă pentru calcule și pentru aplicații practice. În special pentru coeficientul de difuzie al diferitelor materiale. De exemplu, avem un material, pe suprafața căruia se aplică o impuritate, a cărui concentrație de suprafață este egală cu Q cm-2. Prin încălzirea acestui material, această impuritate este difuzată în volumul său. În acest caz, în funcție de timp, se stabilește o anumită distribuție a impurităților pe grosimea materialului pentru o anumită temperatură. Analitic, distribuția concentrației de impurități poate fi obținută prin rezolvarea ecuației de difuzie Fick sub următoarea formă:
Grafic, acesta este:
Pe baza acestui principiu, se pot găsi experimental parametrii de difuzie.
Metode experimentale pentru studiul difuziei
metoda de activare
O impuritate radioactivă este aplicată pe suprafața materialului, apoi această impuritate este difuzată în material. Apoi, o porțiune a materialului este îndepărtată strat cu strat și se examinează fie activitatea materialului rămas, fie a stratului gravat. Și astfel găsiți distribuția concentrației C pe suprafața X(C(x)). Apoi, folosind valoarea experimentală obținută și ultima formulă, se calculează coeficientul de difuzie.
Metode chimice
Ele se bazează pe faptul că în timpul difuzării unei impurități, ca urmare a interacțiunii sale cu materialul de bază, se formează noi compuși chimici cu proprietăți diferite ale rețelei.
metode de joncțiune p-n
Datorită difuzării impurităților în semiconductori, la o anumită adâncime a semiconductorului, se formează o regiune în care se modifică tipul conductivității acestuia. În continuare, se determină adâncimea joncțiunii p-n și se judecă din aceasta concentrația de impurități la această adâncime. Și apoi o fac prin analogie cu primul și al doilea caz.
Lista surselor utilizate
1. Kittel Ch. Introducere în fizica stării solide./ Per. din engleza; Ed. A. A. Guseva. – M.: Nauka, 1978.
2. Epifanov G.I. Fizica stării solide: Proc. indemnizație pentru universități. - M .: Mai sus. școli, 1977.
3. Zhdanov G.S., Khundzhua F.G., Prelegeri despre fizica stării solide - M: Editura Universității de Stat din Moscova, 1988.
4. Bushmanov B. N., Khromov Yu. A. Fizica stării solide: Proc. indemnizație pentru universități. - M .: Mai sus. școli, 1971.
5. Katsnelson A.A. Introducere în fizica stării solide - M: Editura Universității de Stat din Moscova, 1984.
Defecte în cristale Orice cristal real nu are o structură perfectă și are o serie de încălcări ale rețelei spațiale ideale, care sunt numite defecte în cristale. Defectele cristalelor sunt împărțite în zero-dimensionale, una Defecteîn cristale se numesc încălcări ale structurii cristaline ideale. O astfel de încălcare poate consta în înlocuirea unui atom al unei substanțe date cu un atom străin (atom de impuritate) (Fig. 1, a), în introducerea unui atom suplimentar într-un interstițiu (Fig. 1, b), în absența unui atom în situs (Fig. 1, c). Se numesc astfel de defecte repera cu precizie.Ele provoacă încălcări ale rețelei care se propagă pe distanțe de ordinul mai multor perioade.
Pe lângă defectele punctuale, există defecte concentrate în apropierea anumitor linii. Ei sunt numiti, cunoscuti defecte liniare sau luxaţii. Defectele de acest tip perturbă alternanța regulată a planurilor cristaline.
Cele mai simple tipuri de luxații sunt regionalȘi şurub luxaţii.

O dislocare a muchiei este cauzată de un semiplan extracristalin încorporat între două straturi atomice adiacente (Fig. 2). O dislocare a șurubului poate fi reprezentată ca urmare a tăierii unui cristal de-a lungul unui semiplan și a unei deplasări ulterioare a părților rețelei situate pe părțile opuse ale tăieturii una față de cealaltă cu valoarea unei perioade (Fig. 3).

Defectele au un efect puternic asupra proprietăților fizice ale cristalelor, inclusiv asupra rezistenței acestora.
Dislocația existentă inițial se deplasează de-a lungul cristalului sub influența tensiunilor create în cristal. Mișcarea dislocațiilor este împiedicată de prezența altor defecte în cristal, de exemplu, prezența atomilor de impurități. Luxațiile sunt, de asemenea, decelerate atunci când se încrucișează. O creștere a densității luxațiilor și o creștere a concentrației de impurități duce la o decelerare puternică a luxațiilor și la încetarea mișcării lor. Ca urmare, rezistența materialului crește. De exemplu, o creștere a rezistenței fierului se realizează prin dizolvarea atomilor de carbon din acesta (oțel).
Deformarea plastică este însoțită de distrugerea rețelei cristaline și de formarea unui număr mare de defecte care împiedică mișcarea luxațiilor. Aceasta explică întărirea materialelor în timpul prelucrării lor la rece.