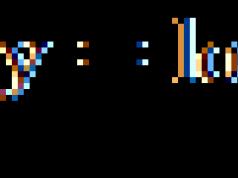Для получения кислорода , потребуются вещества, которые им богаты. Это пероксиды, селитры, хлораты. Мы будем использовать те, что можно достать без особого труда.
Для получения кислорода в домашних условиях есть несколько способов, разберём их по-порядку.
Самый простой и доступный способ получения кислорода – использовать марганцовку (или более правильное название – перманганат калия). Всем известно, что марганцовка – прекрасный антисептик, используется в качестве обеззараживающего вещества. Если её нет, то можно приобрести в аптеке.
Поступим так. В пробирку насыпаем немного марганцовки, закроем пробиркой с отверстием, в отверстие установим газоотводную трубку (по ней будет идти кислород). Другой конец трубки поместим в другую пробирку (она должна располагаться вверх дном, так как выделяющийся кислород легче воздуха и будет подниматься вверх. Такой же пробкой закром вторую пробирку.
В итоге у нас должно получиться две пробирки, соединённые между собой газоотводной трубкой через пробки. В одной (неперевёрнутой) пробирке - марганцовка.
Будем нагревать пробирку с марганцовкой. Тёмно-фиолетово-вишнёвый цвет кристалликов марганцовки исчезнет и превратится в тёмно-зелёные кристаллы манганата калия.
Реакция протекает так:
2KMnO 4 → MnO 2 + K 2 MnO 4 +O 2
Так из 10 грамм марганцовки можно получить почти 1 литр кислорода. Через пару минут можно извлечь колбу с марганцовкой из пламени. Мы получили кислород в перевёрнутой пробирке. Можем его проверить. Для этого аккуратно отсоединим вторую трубку (с кислородом) от газоотводной трубки, прикрыв отверстие пальцем. Теперь, если внести слабо горящую спичку в колбу с кислородом, то она ярко вспыхнет!
Получение кислорода
возможно также с помощью натриевой или калиевой селитры (соответствующие соли натрия и калия азотной кислоты).
(Нитраты калия и натрия – они же – селитры, продаются на магазинах для удобрений).
Итак, для получения кислорода из селитры возьмём пробирку из тугоплавкого стекла на штативе, поместим туда селитровый порошок (5 грамм будет достаточно).Потребуется под пробирку поставить керамическую чашечку с песком, та как стекло может расплавиться от температуры и потечь. Следовательно, горелку надо будет держать немного сбоку, а пробирку с селитрой – под наклоном.
При сильном нагреве селитры она начинает плавиться, при этом выделяется кислород. Реакция проходит так:
2KNO 3 → 2KNO 2 +O 2
Образующееся вещество – нитрит калия (или натрия, смотря, какая селитра использована) – соль азотистой кислоты.
Ещё один способ получения кислорода – использовать перекись водорода. Пероксид, гидроперит – всё одно и то же вещество. Перекись водорода продаётся в таблетках и в виде растворов (3%, 5%, 10%), которое можно приобрести в аптеке.
В отличии от предыдущих веществ, селитр или марганцовки, перекись водорода – неустойчивое вещество. Уже при наличии света она начинает распадаться на кислород и воду. Поэтому в аптеках перекись продаётся в пузырьках из тёмного стекла.
Кроме того, быстрому разложению перекиси водорода на воду и кислород способствуют катализаторы, например, оксид марганца, активированный уголь, стальной порошок (мелкая стружка) и даже слюна. Поэтому, перекись водорода нагревать не нужно, достаточно катализатора!
Здравствуйте.. Сегодня я расскажу Вам о кислороде и о способах его получения. Напоминаю, если у Вас будут ко мне вопросы, Вы можете писать их в комментариях к статье. Если же Вам понадобиться любая помощь по химии, . Буду рад Вам помочь.
Кислород распространён в природе в виде изотопов 16 О, 17 О, 18 О, которые имеют следующее процентное содержание на Земле – 99,76%, 0,048%, 0,192% соответственно.
В свободном состоянии кислород находится в виде трёх алло-тропных модификаций : атомарного кислорода - О о, дикислорода – О 2 и озона – О 3 . Причём, атомарный кислород может быть получен следующим образом:
КClO 3 = KCl + 3O 0
KNO 3 = KNO 2 + O 0
Кислород входит в состав более 1400 различных минералов и органических веществ, в атмосфере его содержание составляет 21% по объёму. А в человеческом теле содержится до 65% кислорода. Кислород газ без цвета и запаха, мало растворим в воде (в 100 объёмах воды при 20 о С растворяется 3 объёма кислорода).
В лаборатории кислород получают умеренным нагреванием некоторых веществ:
1) При разложении соединений марганца (+7) и (+4):
2KMnO 4 → K 2 MnO 4 + MnO 2 + O 2
перманганат манганат
калия калия
2MnO 2 → 2MnO + O 2
2) При разложении перхлоратов:
2KClO 4 → KClO 2 + KCl + 3O 2
перхлорат
калия
3) При разложении бертолетовой соли (хлората калия)
.
При этом образуется атомарный кислород:
2KClO 3 → 2 KCl + 6O 0
хлорат
калия
4) При разложении на свету солей хлорноватистой кислоты - гипохлоритов:
2NaClO → 2NaCl + O 2
Ca(ClO) 2 → CaCl 2 + O 2
5) При нагревании нитратов.
При этом образуется атомарный кислород. В зависимости от того, какое положение в ряду активности занимает металл нитрата, образуются различные продукты реакции:
2NaNO 3 → 2NaNO 2 + O 2
Ca(NO 3) 2 → CaO + 2NO 2 + O 2
2AgNO 3 → 2 Ag + 2NO 2 + O 2
6) При разложении пероксидов:
2H 2 O 2 ↔ 2H 2 O + O 2
7) При нагревании оксидов неактивных металлов:
2Аg 2 O ↔ 4Аg + O 2
Данный процесс имеет актуальное значение в быту. Дело в том, что посуда, изготовленная из меди или серебра, имея естественный слой оксидной плёнки, при нагревании образует активный кислород, что является антибактериальным эффектом. Растворение солей неактивных металлов, особенно нитратов, также приводит к образованию кислорода. Например, суммарный процесс растворения нитрата серебра можно представить по этапам:
AgNO 3 + H 2 O → AgOH + HNO 3
2AgOH → Ag 2 O + O 2
2Ag 2 O → 4Ag + O 2
или в суммарном виде:
4AgNO 3 + 2H 2 O → 4Ag + 4HNO 3 + 7O 2
8) При нагревании солей хрома высшей степени окисления:
4K 2 Cr 2 O 7 → 4K 2 CrO 4 + 2Cr 2 O 3 + 3 O 2
бихромат хромат
калия калия
В промышленности кислород получают:
1) Электролитическим разложением воды:
2Н 2 О → 2Н 2 + О 2
2) Взаимодействием углекислого газа с пероксидами:
СО 2 + К 2 О 2 →К 2 СО 3 + О 2
Данный способ представляет собой незаменимое техническое решение проблемы дыхания в изолированных системах: подводных лодках, шахтах, космических аппаратах.
3) При взаимодействии озона с восстановителями:
О 3 + 2КJ + H 2 O → J 2 + 2KOH + O 2
 Особое значение получение кислорода имеет место в процессе фотосинтеза
, происходящего в растениях. Кардинальным образом от этого процесса зависит вся жизнь на Земле. Фотосинтез – сложный многоступенчатый процесс. Начало ему даёт свет. Сам фотосинтез состоит из двух фаз: световой и темновой. В световую фазу пигмент хлорофилл, содержащийся в листьях растений, образует так называемый «светопоглощающий» комплекс», который отнимает электроны у воды, и тем самым расщепляет её на ионы водорода и кислород:
Особое значение получение кислорода имеет место в процессе фотосинтеза
, происходящего в растениях. Кардинальным образом от этого процесса зависит вся жизнь на Земле. Фотосинтез – сложный многоступенчатый процесс. Начало ему даёт свет. Сам фотосинтез состоит из двух фаз: световой и темновой. В световую фазу пигмент хлорофилл, содержащийся в листьях растений, образует так называемый «светопоглощающий» комплекс», который отнимает электроны у воды, и тем самым расщепляет её на ионы водорода и кислород:
2Н 2 О = 4е + 4Н + О 2
Накопившиеся протоны способствуют синтезу АТФ:
АДФ + Ф = АТФ
В темновую фазу происходит преобразование углекислого газа и воды в глюкозу. И побочно выделяется кислород:
6СО 2 + 6Н 2 О = С 6 Н 12 О 6 + О 2
blog.сайт, при полном или частичном копировании материала ссылка на первоисточник обязательна.
Кислород является одним из наиболее применяемых человечеством газов, он широко используется практически во всех областях нашей жизнедеятельности. Металлургия, химическая промышленность, медицина, народное хозяйство, авиация – вот лишь краткий перечень сфер, где без этого вещества не обойтись.
Получение кислорода осуществляется в соответствии с двумя технологиями: лабораторной и промышленной. Первые методики производства бесцветного газа базируются на химических реакциях. Кислород получают в результате разложения перманганата калия, бертолетовой соли или перекиси водорода в присутствии катализатора. Однако лабораторные методики не могут полностью удовлетворить потребности в этом уникальном химическом элементе.
Второй способ получения кислорода заключается в криогенной ректификации либо с использование адсорбционной или мембранной технологий. Первая методика обеспечивает высокую чистоту продуктов разделения, но имеет более длительный (по сравнению со вторыми методами) пусковой период.
Адсорбционные кислородные установки зарекомендовали себя одними из лучших среди высокопроизводительных систем по изготовлению обогащенного кислородом воздуха. Они дают возможность получать бесцветный газ чистотой до 95% (до 99 % с применением дополнительной ступени очистки). Их использование оправдано в экономическом плане, особенно в ситуациях, когда нет необходимости в кислороде высокой чистоты, за который пришлось бы переплачивать.
Основные характеристики криогенных систем
Вас интересует производство кислорода с чистотой до 99,9 %? Тогда обратите внимание на установки, работающие на основе криогенной технологии. Достоинства систем для производства кислорода высокой чистоты:
- длительный ресурс работы установки;
- высокая производительность;
- возможность получать кислород чистотой от 95 до 99,9 %.
Но из-за больших габаритов криогенных систем, невозможности быстрого запуска и остановки и др. факторов использование криогенного оборудования далеко не всегда является целесообразным.
Принцип действия адсорбционных установок
Схему работы кислородных систем с использованием адсорбционной технологии можно представить следующим образом:
- сжатый воздух движется в ресивер, в систему воздухоподготовки для избавления от механических примесей и фильтрации от капельной влаги;
- очищенный воздух направляется в адсорбционный воздухоразделительный блок, в состав которого входят адсорберы с адсорбентом;
- во время работы адсорберы находятся в двух состояниях - поглощения и регенерации; на стадии поглощения кислород поступает в кислородный ресивер, а азот на стадии генерации отводится в атмосферу; после чего кислород направляется потребителю;
- в случае необходимости давление газа может быть увеличено с помощью дожимного кислородного компрессора с последующей заправкой в баллоны.
Адсорбционные комплексы отличаются высоким уровнем надежности, полной автоматизацией, простотой в обслуживании, небольшими габаритами и весом.

Достоинства газоразделительных систем
Установки и станции с применением адсорбционной технологии для получения кислорода широко используются в самых разных сферах: при сварке и резке металлов, в строительстве, рыборазведении, выращивании мидий, креветок и т. д.
Преимущества газоразделительных систем:
- возможность автоматизации процесса получения кислорода;
- отсутствие особых требований к помещению;
- быстрый запуск и остановка;
- высокая надежность;
- низкая себестоимость получаемого кислорода.
Выгодные стороны адсорбционных установок НПК «Грасис»
Вас интересует производство кислорода используемым в промышленности способом? Вы хотели бы получать кислород при минимальных финансовых затратах? Научно-производственная компания «Грасис» поможет решить вашу задачу на самом высоком уровне. Мы предлагаем надежные и эффективные системы для получения кислорода из воздуха. Вот основные отличительные черты производимой нами продукции:
- полная автоматизация;
- продуманные до мелочей конструкции;
- современные системы контроля и управления.
Кислород, вырабатываемый нашими воздухоразделительными адсорбционными установками, имеет чистоту до 95 % (с опцией доочистки до 99%). Газ с такими характеристиками широко используется в металлургии при сварке и резке металлов, в народном хозяйстве. В производимом нами оборудовании применяются современные технологии, которые обеспечивают уникальные возможности в сфере газоразделения.
Особенности наших адсорбционных кислородных установок:
- высокая надежность;
- низкая себестоимость получаемого кислорода;
- инновационная высокоинтеллектуальная система контроля и управления;
- простота технического обслуживания;
- возможность производить кислород чистотой до 95 % (с опцией доочистки до 99%);
- производительность составляет до 6000 м³/ч.
Адсорбционные кислородные установки НПК «Грасис» – уникальное сочетание мирового конструкторского опыта производства газоразделительного оборудования и отечественных инновационных технологий.
Главные причины сотрудничества с НПК «Грасис»
Промышленный способ получения кислорода с применением установок, работающих на основе адсорбционной технологии, – один из наиболее перспективных на сегодняшний день. Он позволяет получать бесцветный газ с минимальными энергетическими затратами нужной чистоты. Вещество с данными параметрами востребовано в металлургии, машиностроении, химической отрасли, медицине.
Способ криогенной ректификации – оптимальное решение при необходимости производства кислорода высокой чистоты (до 99,9 %).
Ведущая отечественная компания «Грасис» предлагает высокоэффективные системы для производства кислорода по адсорбционной технологии на выгодных условиях. Мы обладаем большим опытом в реализации разнообразных проектов «под ключ», поэтому не боимся даже самых сложных задач.
Преимущества работы с ответственным поставщиком оборудования НПК «Грасис»:
- наша компания является непосредственным производителем, поэтому стоимость реализуемых установок не увеличивают дополнительные комиссии посредников;
- высокое качество продукции;
- полный спектр сервисных услуг по ремонту и техническому обслуживанию установок по производству кислорода;
- индивидуальный подход к каждому клиенту;
- многолетний опыт работы в сфере производства кислорода.
Звоните нашим менеджерам для уточнения нюансов сотрудничества.
Более подробно Вы можете ознакомиться с кислородным оборудованием (кислородные генераторы, кислородные установки, кислородные станции) на странице



В уроке 17 «Получение кислорода » из курса «Химия для чайников » выясним, как получают кислород в лабораторных условиях; узнаем, что такое катализатор, и как растения влияют на производство кислорода на нашей планете.
Наиболее важным для человека и других живых организмов веществом, входящим в состав воздуха, является кислород. Большие количества кислорода используются в промышленности, поэтому важно знать, как можно его получать.
В химической лаборатории кислород можно получать нагреванием некоторых сложных веществ, в состав которых входят атомы кислорода. К числу таких веществ относится вещество KMnO 4 , которое имеется в вашей домашней аптечке под названием «марганцовка».
Вы знакомы с простейшими приборами для получения газов. Если в один из таких приборов поместить немного порошка KMnO 4 и нагреть, то будет выделяться кислород (рис. 76):


Кислород можно также получить разложением пероксида водорода H 2 O 2 . Для этого в пробирку с H 2 O 2 следует добавить очень небольшое количество особого вещества - катализатора - и закрыть пробирку пробкой с газоотводной трубкой (рис. 77).

Для данной реакции катализатором является вещество, формула которого MnO 2 . При этом протекает следующая химическая реакция:

Обратите внимание на то, что ни в левой, ни в правой частях уравнения формулы катализатора нет. Его формулу принято записывать в уравнении реакции над знаком равенства. Для чего же добавляется катализатор? Процесс разложения H 2 O 2 при комнатных условиях протекает очень медленно. Поэтому для получения заметных количеств кислорода необходимо много времени. Однако эту реакцию можно резко ускорить путем прибавления катализатора.
Катализатор - это вещество, которое ускоряет химическую реакцию, но само в ней не расходуется.
Именно потому, что катализатор не расходуется в реакции, мы не записываем его формулу ни в одной из частей уравнения реакции.
Еще один способ получения кислорода - разложение воды под действием постоянного электрического тока. Этот процесс называется электролизом воды. Получить кислород можно в приборе, схематично изображенном на рисунке 78.

При этом протекает следующая химическая реакция:

Кислород в природе
Огромное количество газообразного кислорода содержится в атмосфере, растворено в водах морей и океанов. Кислород необходим всем живым организмам для дыхания. Без кислорода невозможно было бы получать энергию за счет сжигания различных видов топлива. На эти нужды ежегодно расходуется примерно 2% атмосферного кислорода.
Откуда берется кислород на Земле и почему его количество остается примерно постоянным, несмотря на такой расход? Единственным источником кислорода на нашей планете являются зеленые растения, производящие его под действием солнечного света в процессе фотосинтеза. Это очень сложный процесс, включающий много стадий. В результате фотосинтеза в зеленых частях растений углекислый газ и вода превращаются в глюкозу C 6 H 12 O 6 и кислород. Суммарное
уравнение реакций, протекающих в процессе фотосинтеза, можно представить следующим образом:
Установлено, что примерно одну десятую часть (11%) производимого зелеными растениями кислорода дают наземные растения, а остальные девять десятых (89%) - водные растения.
Получение кислорода и азота из воздуха
Огромные запасы кислорода в атмосфере позволяют получать и использовать его в различных производствах. В промышленных условиях кислород, азот и некоторые другие газы (аргон, неон) получают из воздуха.
Для этого воздух сначала превращают в жидкость (рис. 79) путем охлаждения до такой низкой температуры, при которой все его компоненты переходят в жидкое агрегатное состояние.

Затем эту жидкость медленно нагревают, в результате чего при разных температурах происходит последовательное выкипание (т. е. переход в газообразное состояние) веществ, которые содержатся в воздухе. Собирая выкипающие при разных температурах газы, по отдельности получают азот, кислород и другие вещества.
Краткие выводы урока:
- В лабораторных условиях кислород получают разложением некоторых сложных веществ, в состав которых входят атомы кислорода.
- Катализатор - вещество, которое ускоряет протекание химической реакции, но само при этом не расходуется.
- Источником кислорода на нашей планете являются зеленые растения, в которых протекает процесс фотосинтеза.
- В промышленности кислород получают из воздуха.
Надеюсь урок 17 «Получение кислорода » был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Данный урок посвящен изучению современных способов получения кислорода. Вы узнаете, с помощью каких методов и из каких веществ получают кислород в лаборатории и промышленности.
Тема: Вещества и их превращения
Урок: Получение кислорода
В промышленных целях кислород необходимо получать в больших объёмах и максимально дешёвым способом. Такой способ получения кислорода был предложен лауреатом Нобелевской премии Петром Леонидовичем Капицей. Он изобрёл установку для сжижения воздуха. Как известно, в воздухе находится около 21% по объему кислорода. Кислород можно выделить из жидкого воздуха методом перегонки, т.к. все вещества, входящие в состав воздуха имеют разные температуры кипения. Температура кипения кислорода - -183°С, а азота - -196°С. Значит, при перегонке сжиженного воздуха первым закипит и испарится азот, а затем – кислород.
В лаборатории кислород требуется не в таких больших количествах, как в промышленности. Обычно его привозят в голубых стальных баллонах, в которых он находится под давлением. В некоторых случаях всё же требуется получить кислород химическим путём. Для этого используют реакции разложения.
ОПЫТ 1. Нальем в чашку Петри раствор пероксида водорода. При комнатной температуре пероксид водорода разлагается медленно (признаков протекания реакции мы не видим), но этот процесс можно ускорить, если добавить в раствор несколько крупинок оксида марганца(IV). Вокруг крупинок черного оксида сразу начинают выделяться пузырьки газа. Это кислород. Как бы долго ни протекала реакция, крупинки оксида марганца(IV) в растворе не растворяются. То есть, оксид марганца(IV) участвует в реакции, ее ускоряет, но сам в ней не расходуется.
Вещества, которые ускоряют реакцию, но не расходуются в реакции, называют катализаторами .
Реакции, ускоряемые катализаторами, называют каталитическими .
Ускорение реакции катализатором называют катализом .
Таким образом, оксид марганца (IV) в реакции разложения пероксида водорода служит катализатором. В уравнении реакции формула катализатора записывается сверху над знаком равенства. Запишем уравнение проведенной реакции. При разложении пероксида водорода выделяется кислород и образуется вода. Выделение кислорода из раствора показывают стрелкой, направленной вверх:
2. Единая коллекция цифровых образовательных ресурсов ().
3. Электронная версия журнала «Химия и жизнь» ().
Домашнее задание
с. 66-67 №№ 2 – 5 из Рабочей тетради по химии: 8-й кл.: к учебнику П.А. Оржековского и др. «Химия. 8 класс» / О.В. Ушакова, П.И. Беспалов, П.А. Оржековский; под. ред. проф. П.А. Оржековского - М.: АСТ: Астрель: Профиздат, 2006.