Paskaita. 9. Specialios cheminės medžiagos
§ 1. Specialiųjų cheminių medžiagų rūšys ir pagrindinės jų savybės
Specialiosios cheminės medžiagos, atsižvelgiant į savybes, naudojimo sąlygas ir aptikimo būdus, sąlyginai gali būti skirstomos į šias grupes: dažančiosios, liuminescencinės (organinės kilmės – fosforai, neorganinės kilmės – šviesos kompozicijos), indikatorines ir kvapiąsias medžiagas.
Dažikliai - Tai yra cheminės medžiagos, kurios suteikia nuolatinį kontaktinių paviršių spalvą ir daugiausia naudojamos aktyviai aptikti ir atskleisti vagystę vykdančius asmenis.
Patekę į atviras žmogaus kūno vietas, jo drabužius, kitus daiktus, veikiami prakaito-riebalų išskyrų ar aplinkos drėgmės jie ištirpsta ir susidaro ryškiaspalvės dėmės. Taip sukuriami savotiški „ypatingi ženklai“. Tokias dėmes labai sunku pašalinti. Pavyzdžiui, kūno paviršiuje jie lieka po pakartotinio plovimo karštu vandeniu ir plovikliais, ypač po nagais ir odos raukšlėse. Beveik neįmanoma visiškai pašalinti dažančių medžiagų nuo drabužių ir kitų daiktų. Reikėtų nepamiršti, kad kai kurie iš jų turi galimybę švytintis ultravioletiniais spinduliais. Tai leidžia aptikti tokias medžiagas net ir tais atvejais, kai įprastu patikrinimu jos neaptinkamos dėl nedidelio kiekio arba užmaskavimo ant objekto dėl spalvos panašumo.
Dažai yra higroskopiški, tai yra, jie turi savybę sugerti drėgmę iš aplinkinio oro. Šis reiškinys itin nepageidautinas, nes miltelių pavidalo dažančios medžiagos, sugėrusios drėgmę, pirma, praranda savo savybes, o pakartotinai sudrėkintos nepakankamai stabiliai nudažo kontaktinį paviršių, antra, sudrėkintos gali nuspalvinti ir demaskuoti pažymėtą objektą. . Taigi, sudrėkinto, o paskui išdžiovinto rodamino C pėdsakai lengvai pašalinami nuo rankų paprastu nuplaunant muilu ir vandeniu. Todėl laikant ir naudojant dažus, siekiant išvengti gedimo ir pailginti pastarųjų galiojimo laiką, būtina vengti jų sąlyčio su drėgme ir drėgnu oru.
Įjungus spąstus, SHV pėdsakus galima aptikti pagal jiems būdingą spalvą, matomą plika akimi, ir pagal ultravioletinių spindulių liuminescenciją. Bazinių mišinių ekspertiniai tyrimai atliekami plonasluoksnės chromatografijos būdu ir dažų bei kitų komponentų identifikavimu, lyginant su standartais ir spalvinėmis reakcijomis, atliekamomis lašiniu būdu tiesiai ant plokštelės.
Įvairūs molekulinės spektroskopijos metodai, ypač spektrofotometrija, yra patogūs tiriant SSH raganą. Šių medžiagų spalvų spektrinės charakteristikos nustatomos registruojančiais spektrofotometrais.
ATS darbe naudojami dažai turi šias savybes:
Rodaminas C- tamsiai rudi milteliai su žalsvu atspalviu. Tirpalai vandenyje ir alkoholyje yra melsvai raudonos spalvos. Sudrėkintas kontaktinis paviršius nudažomas patvaria tamsiai raudona spalva. Ultravioletiniuose spinduliuose jis turi ryškiai raudoną liuminescenciją.
Rodaminas J- raudoni arba geltonai rudi milteliai. Tirpsta vandenyje ir alkoholyje. Gauti tirpalai turi ryškiai raudoną spalvą ir žalsvai geltoną liuminescenciją. Kontaktinis paviršius nudažytas rudai raudonai su ryškiai geltona liuminescencija ultravioletiniuose spinduliuose.
Rodaminas 4C - tamsiai raudonos spalvos kristalai. Tirpalas vandenyje yra tamsiai raudonos spalvos, etilo alkoholyje - rausvai tamsiai raudonas. Sudrėkintas kontaktinis paviršius nudažomas rausvai tamsiai raudona spalva, šviečiančia ta pačia spalva.
Pagrindinė ryškiai žalia- žalia pudra su auksiniu blizgesiu. Kontaktinis paviršius nudažytas nuolatine žalia spalva. Blogai tirpsta vandenyje, tirpsta alkoholyje.
metileno mėlynas- tamsiai žalia medžiaga. Kontaktinis paviršius nudažytas ryškiai mėlyna spalva. Jis blogai tirpsta vandenyje ir alkoholyje, tačiau kaitinant tirpumas pagerėja. Tirpalai yra mėlynos spalvos.
Chrizoidinas- raudonai rudi milteliai. Kontaktinis paviršius nudažytas geltonai oranžine spalva. Truputį ištirpinsime vandenyje ir gerai - etilo alkoholyje, dietilo eteryje, chloroforme. Tirpalai yra oranžinės rudos spalvos.
Safraninas T- rudai raudoni milteliai. Kontaktinį paviršių nudažo raudonai. Tirpsta vandenyje ir alkoholyje. Ultravioletiniuose spinduliuose, sudrėkintas etilo alkoholiu, jis šviečia raudonai.
metilo violetinė(metileno violetinė) - milteliai su žaliu metaliniu blizgesiu. Tirpalai vandenyje ir etanolyje yra purpuriniai.
Neutrali raudona- tamsiai žali kristaliniai milteliai. Vandeninis tirpalas yra raudonos spalvos. Tirpalas etanolyje yra raudonas, šiek tiek šviečiantis tamsiai raudonos spalvos.
Nilo mėlyna- žali kristaliniai milteliai su bronziniu blizgesiu. Blogai tirpsta šaltame vandenyje, kaitinant tirpumas didėja. Tirpsta etilo alkoholyje. Tirpalai yra mėlyni.
Fuksino pagrindinis- tamsiai žalios spalvos blizgūs kristalai. Kontaktinis paviršius nudažytas rožine spalva. Tirpiname vandenyje (geriau kaitinant), gerai ištirpsime etilo alkoholyje. Tirpalai yra rausvos spalvos.
Pagrindinė mėlyna K- mėlyni milteliai. Kontaktinis paviršius nudažytas mėlynai. Tirpsta vandenyje ir etilo alkoholyje. Tirpalai yra mėlynos spalvos.
Pagrindinis, rudas 2K- juodai rudi milteliai. Tirpalai vandenyje ir etanolyje yra rudos spalvos.
Azur 1 (metileneazūras)- tamsiai rudi kristalai su žalsvu blizgesiu. Tirpiname vandenyje, gerai ištirpsime metilo ir etilo alkoholyje. Tirpalai yra mėlynos spalvos. Alkoholiniai tirpalai turi melsvai raudoną liuminescenciją.
Briliantinė geltona- šviesiai rudi milteliai. Tirpalai vandenyje ir etanolyje yra geltonai oranžinės spalvos.
Eozinas- gelsvai oranžiniai kristaliniai milteliai. Netirpus vandenyje ir benzene; blogai tirpsta etilo alkoholyje, gerai - šarmuose. Gauti tirpalai yra rausvos spalvos.
Liuminescencinės medžiagos - chemikalai, kurie turi savybę švytinti (švyti) ultravioletiniuose spinduliuose.
Kai kurios medžiagos, apšviestos, gali ne tik atspindėti dalį ant jų krintančios šviesos, bet ir pačios pradeda švytėti, ypač veikiant ultravioletinę šviesą skleidžiantiems šaltiniams.
Tam tikrų cheminių medžiagų, turinčių griežtai apibrėžtą spalvą, šalto švytėjimo reiškinys, kai apšviečiamas ultravioletiniais spinduliais, vadinamas fotoliuminescencija (graikiško žodžio „nuotraukos“ – šviesa ir lotyniško „liuminescencija“ – švytėjimas) junginys. Pagal Stokso taisyklę liuminescencinė šviesa turi ilgesnį bangos ilgį nei sužadinimo šviesa. Todėl, kai medžiaga yra apšviesta, ji gali švytinti jai būdinga spalva.
Atkreiptinas dėmesys į tai, kad kai kurios medžiagos tam tikrą laiką išlaiko savybę švytėti, kai nutrūksta apšvietimas (liekamojo švytėjimo). Šis fotoliuminescencijos tipas vadinamas fosforescencija. Švytėjimas, kuris sustoja šviečiant, vadinamas fluorescencija. Tačiau tarp jų sunku nubrėžti aštrią ribą, o skirstymas tam tikru mastu yra sąlyginis.
Liuminescencijos reiškinys naudojamas liuminescencijos analizei. ATS darbe naudojamos liuminescencinės medžiagos, kaip taisyklė, yra bespalvės arba šiek tiek spalvotos. Be to, miltelių pavidalo liuminescencinės medžiagos yra smulkiai dispersinės ir turi geras sukibimo savybes. Dėl šios priežasties jie plačiai naudojami atliekant operatyvinės paieškos veiklą, siekiant paslėpti bet kokių objektų žymėjimą. Liuminescencijos reiškinys leidžia atskleisti nežymiai mažus liuminescencinių medžiagų kiekius. Pavyzdžiui, pakanka turėti milijonąją gramo šviečiančios medžiagos tirpalo pavidalu, kad ją būtų galima aptikti pagal būdingą liuminescenciją.
Pagrindiniai liuminescencinių medžiagų, naudojamų vidaus reikalų įstaigose, atstovai turi šias savybes:
Lengva BZS kompozicija- balti smulkiai kristaliniai milteliai. Jis netirpus vandenyje ir kituose tirpikliuose. Ultravioletiniuose spinduliuose BZS šviesos sudėtis turi ryškiai mėlyną liuminescenciją. Naudokite šią medžiagą, kad užteptumėte žymes ant audinio, verpalų, kailio.
Šviesos kompozicija FK-102- geltonai oranžiniai smulkūs kristaliniai milteliai. Netirpi vandenyje ir kituose tirpikliuose. Ultravioletiniuose spinduliuose jis šviečia oranžiškai raudonai. Jis naudojamas etiketėms klijuoti ant audinio, kailio, verpalų.
Lumogen geltonai žalia- yra amorfinė geltonai žalios spalvos medžiaga. Tirpsta organiniuose tirpikliuose, tokiuose kaip toluenas, dichloretanas, benzinas. Ultravioletiniuose spinduliuose jis turi geltonai žalią liuminescenciją.
Lumogen vandens mėlyna- šviesiai mėlynos spalvos milteliai. Jis gerai tirpsta toluene, benzine, dichloretane. Ultravioletiniuose spinduliuose jis turi mėlyną liuminescenciją.
Lumogen šviesiai žalia- šviesiai žalios spalvos smulkūs kristaliniai milteliai. Tirpsta toluene, benzine, dichloretane. Ultravioletiniuose spinduliuose jis šviečia žaliai.
tiesiai baltas- balta miltelių pavidalo medžiaga. Ultravioletiniuose spinduliuose jis turi mėlyną liuminescenciją.
Rivanolis- yra smulkiai kristaliniai geltonos spalvos milteliai. Jis blogai tirpsta vandenyje, bet gerai tirpsta alkoholyje. Ultravioletiniuose spinduliuose jis turi geltoną liuminescenciją.
Tetraciklinas- geltoni milteliai. Blogai tirpsta vandenyje. Ultravioletiniuose spinduliuose jis turi geltoną liuminescenciją.
Trifenilpirazolinas- Balti milteliai. Tirpsta alkoholyje. Ultravioletiniuose spinduliuose jis turi mėlyną liuminescenciją.
Pažymėtina, kad iš visų išvardytų liuminescencinių medžiagų rivanolis, tetraciklinas ir trifenilpirazolinas yra vaistai. Tai leidžia juos panaudoti maisto produktų ženklinimui, nes naudojamais kiekiais, net ir patekę į žmogaus organizmą, nekenkia sveikatai. Be to, šios medžiagos neturi įtakos paženklintų produktų skoniui ir maistinėms savybėms.
Rodikliai – Tai cheminės medžiagos, kurios, veikiamos tam tikrų cheminių reagentų, pakeičia spalvą. Jie naudojami objektams, kurie įprastomis sąlygomis yra nematomi, tačiau lengvai aptinkami dėl spalvos pasikeitimo, pažymėti.
Medicininiai preparatai naudojami kaip rodikliai Vidaus reikalų departamento darbe. Šios medžiagos yra nekenksmingos žmonėms ir aplinkai. Medicininiais vaistais pagrįstus indikatorius lengva gaminti ir patogu slaptam ženklinti bei vėliau aptikti (pasireikšti). Taip pat atsižvelgiama į tai, kad atsitiktinio farmacinių preparatų kontakto su pažymėto objekto paviršiumi tikimybė yra labai maža.
Vienas iš šios medžiagų grupės atstovų yra fenolftaleinas.
Fenolftaleinas- smulkiagrūdžiai balti milteliai. Jis blogai tirpsta vandenyje, bet gerai tirpsta alkoholyje. Fenolftaleino tirpalas yra bespalvis ir skaidrus. Kai į jį įpilamas šarminės reakcijos tirpalas (pavyzdžiui, amoniako, sodos ir kt. tirpalas), jis įgauna ryškiai tamsiai raudoną spalvą. Būtent ši jo savybė naudojama atliekant operatyvinę paiešką (įvykius.
Kiti farmaciniai preparatai taip pat gali būti naudojami kaip indikatoriai, pavyzdžiui, salicilo rūgštis, antipirinas, amidopirinas, rezercinas, kalcio gliukonatas, analginas, norint sukurti įrašus ir žymes, padarytus šių medžiagų tirpalais, 3% vandeninis geležies chlorido tirpalas ( Sh) naudojamas.
Salicilo rūgštis- smulkūs, adatos pavidalo kristalai, bekvapiai, balti, švelniai kaitinant pakylėti (pereina į dujinę būseną, apeinant skystą). Vandenyje salicilo rūgštis blogai tirpsta, lengvai tirpsta etilo alkoholyje, dietilo eteryje. Gauti tirpalai yra bespalviai. Sukurti su 3% FeCl 3 tirpalu, jie įgauna violetinę spalvą.
Antipirinas- bespalviai kristalai arba balti kristaliniai milteliai, bekvapiai, šiek tiek kartaus skonio. Lengvai tirpsta vandenyje ir etilo alkoholyje. Gauti tirpalai yra bespalviai. Veikiant FeCl 3 tirpalui, jie įgauna rudą spalvą.
Amidopirinas- balti kristalai arba balti milteliai, bekvapiai, šiek tiek kartaus skonio. Tirpsta vandenyje ir etilo alkoholyje. Gauti tirpalai yra bespalviai. Veikiant FeCl 3 tirpalui, jie įgauna rausvą spalvą su rudu atspalviu.
Rezorcinolis- balti arba balti su šiek tiek gelsvo atspalvio kristaliniai milteliai, turintys specifinį kvapą. Oro ir šviesos įtakoje jis palaipsniui tampa rausvas. Lengvai tirpsta vandenyje ir etilo alkoholyje. Gauti tirpalai yra bespalviai. Veikiant FeCl 3 tirpalui, jie įgauna rausvą spalvą su rudu atspalviu.
Kalcio gliukonatas- balti granuliuoti kristaliniai milteliai, bekvapiai ir beskoniai. Netirpus etilo alkoholyje. Tirpsta vandenyje. Gautas tirpalas yra bespalvis. Veikiamas FeCl 3 tirpalu įgauna žalsvai gelsvą spalvą.
Analgin- visiškai balti arba šiek tiek gelsvi kristaliniai milteliai, bekvapiai, kartaus skonio. Ištirpiname vandenyje. Gautas tirpalas yra bespalvis. Veikiant FeCl 3 tirpalui, jis pasidaro rausvas su avietiniu atspalviu. Kadangi analginas greitai suyra esant drėgmei, jo vandeninis tirpalas laikymo metu pagelsta. Objektams žymėti galima naudoti tik ką tik paruoštą tirpalą.
Išvardinti rodikliai – vaistai, o tai leidžia efektyviai juos naudoti ne tik įvairių prekių, bet ir maisto produktų ženklinimui.
Naudodami vaistus indikatoriniams tirpalams ruošti, galite vartoti paruoštas dozavimo formas, kuriose yra pradinių medžiagų, arba paruoštus siūlomų vaistų tirpalus,
Kvapiosios medžiagos – Tai specialios cheminės medžiagos, kurių pagrindinė savybė – būdingas patvarus kvapas, lengvai pagaunamas specialiai dresuoto šuns. Kadangi šios medžiagos, kaip taisyklė, naudojami ne įprasti natūralūs cheminiai junginiai, kurie turi specifinį poveikį šuns uoslei ir centrinei nervų sistemai. Kvapo preparatai palengvina paieškos šunų darbą įvairiose operatyvinėse veiklose.
Vidaus reikalų institucijose dirba šie kvapų preparatai: US (pėdsakų stipriklis) ir SP-80 ms.
JAV narkotikas yra specialiai paruošta miltelių pavidalo medžiaga. Jo kvapą gerai atpažįsta šunys, kai temperatūra yra nuo -20°C iki +30°C. Narkotikų pėdsakus ant drabužių, batų, namų apyvokos daiktų šuo lengvai aptinka per 3-7 dienas. Paprasti paieškos šunys, praėję trumpą specialų mokymą, yra tinkami objektų, kuriuose yra JAV pėdsakų, mėginiams imti. US gali būti naudojamas kartu su dažikliais ir liuminescencinėmis medžiagomis.
Paruošimas SP-80 ms- aliejinė klampi ruda medžiaga, turinti būdingą kvapą, mažai tirpi vandenyje, nekenksminga žmonėms ir gyvūnams. Vaistas susideda iš riebalų pagrindo ir specialios kvapiosios medžiagos. Į jį pridedama liuminescencinių medžiagų. Kai kuriais atvejais jis naudojamas nepridedant pastarojo. Ši jo atmaina vadinama SP-80.
Vaisto kvapas skirtingomis klimato sąlygomis ant pažymėtų objektų (zonoje) išlieka iki 10 dienų. Vaistas atsparus saulės spinduliams, lietui, vėjui, oro temperatūros svyravimams.
Jo pėdsakų buvimą gali suvokti bet kokios veislės šunys (paslaugų paieškos, medžioklės, dekoratyviniai), kurie sukūrė sąlyginių refleksų kompleksą šiam vaistui. Refleksui palaikyti reikia tik 2-3 treniruočių per mėnesį.
Naudojant kvapiąsias medžiagas, sudaromos sąlygos, kuriomis jos perkeliamos į pažeidėjo batus. Tai leidžia ne tik sėkmingai išsiaiškinti pėdsaką, bet ir atrinkti asmenis, įtariamus padarius nusikaltimą. Įvairių materialinių vertybių žymėjimas kvapnia medžiaga leidžia efektyviai jas aptikti ir atrinkti pažymėtus objektus iš daugybės vienarūšių. Kvapo medžiagų derinys su dažančiomis ir liuminescencinėmis medžiagomis abipusiškai padidina jų naudojimo efektyvumą, nes leidžia ilgą laiką atpažinti atitinkamus pėdsakus.
§ 2. Pagrindinės specialių cheminių medžiagų naudojimo kryptys
SHV naudojami tiek įvairių objektų ženklinimui eksploatacinės veiklos metu, tiek cheminių gaudyklių įrengimui objektuose, kuriuose galima arba vyksta vagystės.
Operatyvinėje-paieškos veikloje naudojami specialūs chemikalai miltelių, specialių tepalų, tirpalų, specialių pieštukų, aerozolių pavidalu.
SHV tipas, jo agregavimo būsena parenkami pagal esamą eksploatavimo situaciją.
Taip atsižvelgiama į daikto pobūdį, spalvą ir laikymo sąlygas. Prieš ženklinant objektus, pirmiausia būtina išbandyti chemines medžiagas su panašiais į naudojamą medžiagą mėginiais ir tik gavus teigiamus rezultatus, pereiti prie ženklinimo.
SHV milteliai naudojami tiek atskirai, tiek mišinyje vienas su kitu. Jie naudojami įvairiems objektams ženklinti švelniu ar grubiu paviršiumi, taip pat įrengti prietaisus, užtikrinančius jų purškimą. Paprastai tai yra dažančių ir liuminescencinių medžiagų mišiniai.
SHV pudra tepama teptuku arba pilant į objektus ar jų maketus. Daiktus, apdorotus miltelių pavidalo SHW, reikia keisti priklausomai nuo vietinių klimato sąlygų, bet ne rečiau kaip kartą per metus, kai mišinys yra sandarus, ir kartą per ketvirtį - jei nėra sandarinimo, nes SHW milteliai lengvai sugeria drėgmę iš oro, kuri suyra. jų savybes.
Specialūs tepalai yra riebalų bazė, į kurią įterpiami dažikliai, liuminescencinės medžiagos arba jų mišiniai. Pagrindas naudojamas vakuuminis tepalas, vazelinas, tepalas, konstaline ir kt.Ruošiant specialų tepalą, būtina atsižvelgti į riebalinio pagrindo savybes. Taigi, tepalą vazelino pagrindu galima naudoti nuo -3 ° C (toliau mažėjant temperatūrai, jis sukietėja) iki + 25 ° C (toliau kylant temperatūrai, tepalas lengvai suskystėja).
Specialūs tepalai konstantinio ir vakuuminio tepalo pagrindu yra atsparesni temperatūros ir drėgmės svyravimams. Specialus tepalas vakuuminio tepimo pagrindu pasižymi dideliu lipnumu ir ribotu tirpumu. Net ir pašalinus jį benzinu, liuminescencinių medžiagų pėdsakus galima aptikti pagal būdingą švytėjimą ultravioletiniuose spinduliuose.
Specialus tepalas, paruoštas vakuuminio tepalo ir vazelino aliejaus pagrindu (svorio santykiu 3:1), pasiteisino. Jis laikomas ant bet kokių lygių paviršių, nekeičia savo "konsistencijos temperatūros diapazone nuo -20 ° C iki + 30 ° C".
Specialiais tepalais tepami daiktai ar jų pakuotė. Skirtingai nuo miltelių pavidalo SHV, jie gerai laikosi ant įvairių lygių paviršių. Taip pat reikėtų atsižvelgti į tai, kad riebalų bazė izoliuoja SSH nuo sąlyčio su oro drėgme. Tai užtikrina žymių saugumą ilgesnį laiką net esant didelei drėgmei. Taigi, jei miltelių pavidalo SHV be sandarinimo apdorotų daiktų keitimas turėtų būti atliekamas bent kartą per ketvirtį, tai tepant specialiu tepalu - bent kartą per metus. Tepalo pavidalo paruoštus kvapus lengvai sugeria vilnoniai, medvilniniai ir kiti audiniai, gerai išsilaiko ant įvairių paviršių (medžio, metalo, plastiko, betono, gumos, odos, purvo ir asfaltuotų kelių). Be to, dažikliai ir liuminescenciniai priedai yra gerai saugomi nuo tiesioginės išorinių veiksnių, tokių kaip drėgmė ir temperatūra, įtakos.
Specialūs tepalai tepami šepetėliu arba vatos tamponu.
SPRENDIMAI ruošiami liuminescencinių medžiagų ar indikatorių pagrindu ir naudojami įvairiems objektams žymėti. Ruošiant tirpalus galima naudoti vandenį arba organinius tirpiklius, pavyzdžiui, alkoholį, eterį, tolueną, dichloretaną, acetoną. Jei reikia, SHV galima švirkšti tiesiai į skysčius, kuriuos reikia paženklinti. Pavyzdžiui, į įprastą mėlyną ar violetinį rašalą įdėjus liuminescencinių medžiagų, galite gauti vadinamąjį specialų rašalą. Jais tušinuku galima pažymėti įvairius dokumentus. Jei reikia gauti tirpalą, gerai fiksuojantį objekto paviršių, kaip tirpiklį galima naudoti dichloretaną, į kurį įterpiama organinio stiklo drožlių, kad išdžiūvus susidarytų sunkiai nusiplaunama plėvelė. SHV tirpalai ant objektų tepami teptuku, rašikliu, purškimo pistoletu.
Specialūs liuminescenciniai pieštukai naudojami įvairių objektų, dokumentų, banknotų žymėjimui. Išoriškai šie pieštukai, niekuo nesiskiriantys nuo įprastų, savo pagrindinėje masėje turi specialų priedą - liuminescencinę medžiagą. Pieštukai yra kelių spalvų.
Prieš žymint būtina įsitikinti, kad patys pažymėti objektai nešviečia ultravioletiniais spinduliais. Pieštuko spalva parenkama pagal daikto paviršiaus spalvą. Klijuojant etiketes ant plonų popieriaus lapų, dokumentų, popierinių prekių pakuočių, būtina užtikrinti, kad jos nepaliktų įbrėžtų žymių. Tokiais atvejais po pažymėtais objektais reikia padėti kieto lygaus paviršiaus objektą, pavyzdžiui, stiklą ar organinį stiklą.
Specialiais liuminescenciniais pieštukais užteptos žymės išsaugomos ilgą laiką.
Aerozolių balionėliai yra cilindras, užpildytas liuminescencinės medžiagos tirpalo arba indikatoriaus su freonais mišiniu. Naudojant purkštuvą, iš cilindro, veikiant freono garų slėgiui, išleidžiama mišinio srovė ir, suskaidžius į mažyčius lašelius, susidaro aerozolio debesis.
Naudodami aerozolinius purkštuvus galite greitai ir efektyviai apdoroti didelius objektų paviršius, išleisdami nedidelį kiekį SHV. Vidaus reikalų įstaigose dirba šie liuminescenciniai aerozoliai: Madizol-M, Madizol-PP, Madizol-SZh.
"Madizol-PP" naudojamas maisto produktų ženklinimui.
"Madizol-M" naudojamas kailių ir vilnos gaminių, medvilnės ir sintetinių audinių ženklinimui.
"Madizol-SJ" Skirta statybinių medžiagų, odos, stiklo, keramikos, plastiko, ūkinių gyvūnų vilnonių apdangalų žymėjimui.
Pagaminta fenolftaleino pagrindu "Fenozolis". Aerozolinė pakuotė "Phenozol" gali turėti dozavimo vožtuvą. Fenozolis naudojamas alkoholio turintiems skysčiams žymėti. Fenozolio buvimas nustatomas naudojant šarminį tirpalą.
Taigi policijos departamentas yra apginkluotas pakankamu skaičiumi specialių cheminių medžiagų, kurios gali būti efektyviai panaudotos kovojant su nusikalstamumu. Tačiau tai duoda teigiamą rezultatą tik tuo atveju, jei jų pėdsakai greitai aptinkami vykdant operatyvinę – paieškos veiklą.
§ 3. Cheminių spąstų samprata ir rūšys
Smulkių vagysčių problema egzistuoja nuo senų senovės ir, ko gero, egzistuos visada, nes materialinės būklės gerinimas lengvai prieinamu būdu yra daugiau ar mažiau būdingas kiekvienam žmogui. Šiandien techninės apsaugos, stebėjimo ir signalizacijos priemonės turi milžiniškas galimybes, tačiau jos negali apsaugoti piliečių asmeninės nuosavybės nuo nesąžiningų žmonių kėsinimosi. Kadangi neįmanoma sukurti visuomenės su visiško vaizdo valdymo ir stebėjimo tinklu, problemai spręsti naudojami kiti metodai.
Vienas iš būdų, prisidedančių prie nusikaltimų nuosavybei prevencijos ir greito atskleidimo, yra įvairių cheminių ir techninių priemonių panaudojimas. Tai apima specialias chemines kompozicijas, kurios praktikoje ir literatūroje dažnai vadinamos cheminiais spąstais arba žymenimis (kai kurie mokslininkai siūlo terminą „kriminalistikos žymekliai“). Tokios medžiagos, patekusios ant nusikaltėlio drabužių ar kūno, palieka sunkiai pašalinamus ir aiškiai matomus pėdsakus, leidžiančius nustatyti jo neteisėtą patekimą į patalpas, kontaktus su tam tikrais daiktais, vogtų medžiagų šaltinius ir jų platinimo kanalus. , kyšio davimas ir kt. Specialiųjų priemonių panaudojimą kovojant su nusikaltimais numato Policijos įstatymas (9 p., 11 str.), kuriame jos vadinamos „specialiosiomis dažikliais“2.
Rusijos Federacijos vidaus reikalų ministerijos 1993 m. rugsėjo 11 d. įsakymas Nr. 423 pateikia tokį cheminių spąstų sąvokos aiškinimą: Tai prietaisai arba prietaisai, aprūpinti (apdoroti) specialiomis cheminėmis medžiagomis (spalvomis ar kvapais), užmaskuoti įvairiais daiktais, kurių pagalba tokios medžiagos pernešamos ant žmogaus kūno ir drabužių.
Cheminiai spąstai yra viena iš nusikaltimų išaiškinimo priemonių. Jie atitinka visus techninėms priemonėms keliamus reikalavimus, todėl yra legalūs ir dėl jų naudojimo neturėtų kilti abejonių. Idėją sukurti spąstus paskatino pati praktika. Nusikaltimų tyrimo skyriaus darbuotojams puikiai žinomi faktai, kai vagysčių išaiškinimą labai palengvino tai, kad kaltininkas nusikaltimo metu netyčia aliejiniais dažais, balinimo ar kitais dažais ištepė rankas, batus ar drabužius. Tokie faktai buvo vertinami kaip didžiulė sėkmė, nes tai demaskavo nusikaltėlį tarp aplinkinių ir prisidėjo prie greito jo sulaikymo. Cheminių spąstų kūrimas ir naudojimas sėkmę paverčia dėsningumu, nes spąstų preparatai, patekę ant žmogaus kūno ir jo drabužių, sukelia ryškių spalvų ir sunkiai nuplaunamų, aplinkiniams lengvai pastebimų žymių atsiradimą, o tai padeda. sulaikyti nusikaltėlį. Tyrėjai patys cheminių spąstų nenaudoja, tačiau dažnai su jomis susiduria tirdami kyšininkavimą, taip pat vagystes iš prekybos vietų, komunalinių ir sandėliavimo patalpų, vaistinių, įstaigose esančių biuro stalų. Į įsibrovėlį bandant atidaryti ar paimti įrengtą objektą be leidimo, prietaisai mėtė medžiagas. Šiuo atveju atsirado gausus dažymas, o specifinė dažų savybė – prasiskverbti į kūno poras ar drabužių bei batų struktūrą – leido atpažinti įsibrovėlį labai ilgai. Net jei matomi dažų pėdsakai buvo nuplauti, jie labai ryškiai pasirodydavo ultravioletiniuose spinduliuose.
Į naudojamų medžiagų sudėtį įeina baziniai mišiniai su priedais. Juose sumontuoti kelių spalvų dažai arba jų derinys, leidžiantis jais žymėti tam tikros rūšies ar konkrečios teritorijos prekes. Sulaikius asmenį, susidūrusį su cheminėmis spąstais, galima neabejotinai nustatyti jo dalyvavimą konkrečiame nusikaltime, net jei pagrobėjas apie tai tyli ar net neigia. Dažnai spąstų pagalba pagrobėjas gali būti aptiktas anksčiau nei pati vagystė.
Cheminės gaudyklės, veikiančios autonomiškai, montuojant ir eksploatuojant nereikalauja maitinimo ir papildomos įrangos, o kartu su įsilaužimo signalizacija suteikia dar didesnį efektą, ypač kai vagis vagystę įvykdo „trūkčiodamas“.
Kartu su pagalba saugant materialines vertybes prekybos objektuose, bazėse, sandėliuose ir pagalbinėse patalpose dažnai atsiranda būtinybė apsaugoti konkretaus asmens asmeninę nuosavybę. Esant aukštam šiuolaikinio gyvenimo techniniam lygiui, labai mažai naudojama priemonių užkirsti kelią, dokumentuoti ir persekiojant atskleisti jau įvykdytas asmeninio turto vagystes, kurias dažnai įvykdo vienas šalia kito sėdintys darbuotojai. Priežastis ne ta, kad tokių priemonių nėra – racionalumo ir tikslingumo principas tiesiog įsigalioja dėl jų brangumo. Kartu tiek psichologinė trauma, tiek materialinė žala aukai nustumiama į antrą planą. Cheminiai spąstai veikia tik „vagis“ ar „smalsus“ darbuotojas.
Atsižvelgiant į tai, kad yra didelė asmeninio turto vagysčių įvairovė, cheminiai spąstai gaminami struktūriškai arti vagį dominančių objektų. Naudojamos medžiagos ir dangčiai, esantys cheminių gaudyklių įrengimo vietoje: valiutos keityklose, bankuose ir jų skyriuose, paštuose naudojamos bankų pakuotės su atitinkamais užrašais, parduotuvėse ir kioskuose - specialios dėžės, galinčios sukurti iliuzija, kad juose yra pinigų, darbo vietose – piniginės ir rankinės ir pan.
Cheminių spąstų kūrėjai ir gamintojai stengiasi išpildyti klientų pageidavimus ir pageidavimus. Padaugėjus vagysčių iš vasarnamių ir rūsių, sėkmingai naudojamas prietaisas vagiui išgąsdinti ašarinėmis dujomis. Įsiskverbęs į pastatą ir judėdamas juo, vagis tikrai užsikabins ant plonos nailoninės meškerės, kuri per spyruoklinį mechanizmą atidaro ašarinių dujų balionėlio vožtuvą. Net jei kambarys yra didelis, jame likti neįmanoma. Šis įrenginys veikia beveik bet kokiomis klimato sąlygomis, yra visiškai nepriklausomas nuo energijos, nereikalauja priežiūros, tačiau turi būti montuojamas uždarose, blogai vėdinamose patalpose.
Pastaruoju metu masiškai išplitus tokio pobūdžio nusikaltimams, kaip spalvotųjų metalų vagystės pramoniniuose įrenginiuose, buvo sėkmingai išbandytas cheminis gaudyklė su spyruokliniu dažų išmetimo mechanizmu. Jo veikimo principas – spyruoklinio mechanizmo įjungimas neteisėtai atidarius ar išėmus įrangą. Tokiu atveju dalis dažančių medžiagų užmetama ant pažeidėjo. Spąstai keletą metų išlaiko savo darbines savybes net esant ekstremalioms klimato sąlygoms, o tai yra pirmasis reikalavimas tokiems įrenginiams. Jis naudojamas siekiant užkirsti kelią, o vagystės iš užblokuoto objekto atveju – greičiausiam vagystės atskleidimui.
Spyruoklinė dažų gaudyklė montuojama elektros spintose ir ryšių dėžėse, gaisrinių hidrantų dėžėse ir ypač tinka apsaugoti taksofonų įrangą – aliuminiu dengtas telefonų būdeles ir naujus taksofonus, kuriuos dažnai puola spalvotųjų metalų medžiotojai. Gamybos procese atsižvelgiama į visas problemines problemas, kylančias eksploatuojant tokius įrenginius.
Kaip parodė praktika, po cheminių spąstų veikimo – nepaisant to, ar pagrobėjas yra atskleistas – informacija apie tokių prietaisų panaudojimo faktą ilgam žlugdo norą vogti.
Cheminiai spąstai pagal paskirtį skirstomi į dvi grupes:
1) ženklinimui;
2) blokuoti objektus materialinėmis vertybėmis.
Pinigų, vertybinių popierių, įvairių daiktų žymėjimui (pavyzdžiui, perleistams kaip kyšis) šiuo metu gaminami šie spąstai:
1. Reagentų ir prietaisų rinkinys "Rhododendron" -
Skirtas banknotų ženklinimui.
2. Specialus produktas aerozolio pakuotėje "Firefly" -
skirtas naudoti ant banknotų, dokumentų ir
kiti plono sluoksnio liuminescencinės medžiagos objektai su padidintu sukibimu (išvertus iš lotynų kalbos „limpa“) prie žmogaus odos ir nematomi normaliomis sąlygomis. At
pirštų, ant kurių yra vaisto, kontakto su įvairiais
paviršiai (durų rankena ir kt.) palieka pirštų atspaudus,
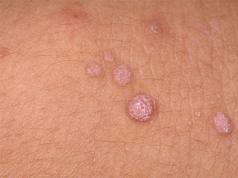
matomas ultravioletiniais spinduliais, kurių bangos ilgis yra 365 nm. Iš vienos aerozolio pakuotės apdoroto paviršiaus plotas yra 1,5 m 2 . Šiems tikslams taip pat naudojama dažanti kompozicija „Poddka“ (1 pav.), pagaminta maišant specialius dažus su tam tikrų rūšių lubrikantais. Susilietus su juo, ant rankų ir drabužių lieka sunkiai nusiplaunamos aviečių spalvos riebios dėmės.
3. Specialus įrankis „Diskoteka“; yra kosmetinis volelis, pripildytas permatomo gelio su specialiu liuminescenciniu žymekliu, nematomu esant normaliam apšvietimui, leidžiančiu patvirtinti viešų renginių lankytojo teisėtumą nepateikus leidimo (2 pav.). Atitinkamą nematomą ženklą inspektorius uždeda ant lankytojo rankos ridendamas dozatoriaus rutulį. Žymeklio buvimą galima aptikti pagal mėlyną liuminescencinį švytėjimą, kai jis apšvitinamas ultravioletiniais spinduliais, kurių bangos ilgis yra 365 nm.

4. Žymėjimo žymekliai "M" ir "K"; skirtas klijuoti etiketes, užrašus ant įvairių objektų ir dokumentų, siekiant juos identifikuoti arba išvengti klastojimo. „M“ ženklo žymekliai naudojami popierinėms medžiagoms žymėti, prekės ženklas „K“ - objektams, pagamintiems iš metalo, plastiko, odos, audinių ir tt žymėti. Ultravioletiniuose spinduliuose žymekliai „M“ suteikia mėlyną švytėjimą, „K“ “ – žalia.
5. Liuminescenciniai žymekliai vaško pieštukų pavidalu
(kreidelės); sukurtas naudoti žymes, kurios yra nematomos, kai
normalus apšvietimas (3 pav.). Jie žymi įvairius daiktus – pakavimo dėžes, dėžutes ir tt Autentifikavimas ir
pakuotės konservavimas atliekamas ultravioletiniu apšvietimu, kurio bangos ilgis yra 365 nm, atsižvelgiant į būdingą daugiaspalvį švytėjimą. Komplektą sudaro 5 skirtingo švytėjimo kreidelės: geltonos, žalios, geltonai žalios, mėlynos ir raudonos.
6. Liuminescencinis žymeklis "Lak-M"; skirta apsaugoti įvairius daiktus, siekiant nustatyti pakeitimo faktus arba
neleistinas atidarymas (4 pav.). Etiketė klijuojama ant švaraus, kieto paviršiaus. Tinkamos medžiagos yra dirbtinė ir natūrali oda, metalai, plastikai, mediena ir kt. Objekto autentiškumas vertinamas pagal būdingą geltonai žalią etiketės švytėjimą ultravioletiniuose spinduliuose, atsirandantį tirpikliui išdžiūvus.

Cheminiai spąstai, skirti blokuoti objektus, turinčius materialinių vertybių, skirstomi į aktyvius ir pasyvius.
Aktyvūs cheminiai spąstai turi įtaisą, skirtą dažams išmesti į erdvę ir taip užtikrinti, kad jie patektų ant drabužių ir atvirų šį įrenginį aktyvavusio asmens kūno dalių. Dažai gali būti išstumiami tiek mechaniniams įtaisams, pavyzdžiui, spyruokliniams, tiek suveikiant pirotechniniam purškimui (ri
DEVINTA KLASĖ
9-1 užduotis
Dvejetainio metalo A deguonies junginio mėginys, sveriantis 55 g, buvo apdorotas 1 litru vandens. Gautas tirpalas virinamas su grįžtamu šaldytuvu, kad gautų 998 ml tirpalo, kurio tankis 1,049 g/ml.
1. Išvardykite visas dvejetainių metalų junginių su deguonimi klases.
2. Nustatykite galimas junginio A formules ir pavadinkite jas.
3 Parašykite visas cheminių reakcijų lygtis, reikalingas uždaviniui išspręsti. 9-2 užduotis
Ant lentynos laboratorijoje jie rado dvi skardines su nutrintomis etiketėmis. Abiejuose stiklainiuose buvo juodų miltelių. Vieną iš jų ištirpinus koncentruotoje druskos rūgštyje, susidarė geltonai žalias tirpalas (1), kuris praskiedus vandeniu tapo mėlynas (2). Sąveikaujant su kitų miltelių koncentruota druskos rūgštimi, gautas mėlynas tirpalas (3), kuris praskiedus vandeniu tapo rausvas (4).
1. Pateikite pagrįstą išvadą, kokiose medžiagose gali būti
2. Parašykite šių medžiagų sąveikos su koncentruota druskos rūgštimi reakcijų lygtis (1, 3) ir reakcijų lygtis, kai susidarę tirpalai skiedžiami vandeniu (2, 4). Paaiškinkite atitinkamų sprendimų spalvų pasikeitimo priežastį.
9-3 užduotis
Kartą Karabasas-Barabasas, perskaitęs chemijos vadovėlį, pareikalavo, kad aktoriai ištirtų mangano sąveiką su įvairiomis rūgštimis. Kai kuriems veikėjams buvo duotas chemiškai grynas manganas, o likusiems – metalas, kuriame buvo geležies ir vario mišinio. Naudojome 3 M druskos ir azoto rūgštis, 1 M sieros rūgštį ir dūmuojančią (100 %) azoto rūgštį, kurių buvo paimta perteklius metalo atžvilgiu. Duremaras kiekvienam veikėjui suteikė po vieną metalo pavyzdį ir vieną buteliuką rūgšties. Veikėjai savo pastebėjimus fiksavo laboratoriniuose žurnaluose. Pažvelkime į šių žurnalų įrašus.
Pinokis. Reakcija vyksta energingai ir nereikalauja kaitinimo. Išsiskiria bespalvės dujos, kurios, pakėlus degtuką, su vata sprogsta. Metalas ištirpsta be likučių.
Malvina. Reakcija nevyksta taip stipriai kaip mėgintuvėlyje Pinokyje. Išsiskiria bespalvės, degios dujos, bekvapės ir beskonės. Visiškai ištirpus metalui, mėgintuvėlio apačioje lieka šiek tiek smulkių miltelių.
Pierrot. Reakcija nevyksta taip stipriai kaip mėgintuvėlyje Pinokyje. Metalas ištirpsta be likučių. Kai į tirpalą įpilama natrio sulfido, susidaro juodos nuosėdos. Iš mėgintuvėlio išsiskiriančios dujos turi vos pastebimą geltonai oranžinę spalvą, kuri išnyksta, kai dujos praleidžiamos per šarmą. Dujos, patekusios per šarmą, yra bespalvės, o pakėlus degtuką su vata sprogsta.
Lapė Alisa. Veikiant rūgščiai, metalo paviršius pasidengia balkšva danga, dujos neišsiskiria. Įpylus nedidelį kiekį vandens, prasideda energinga reakcija su rudų dujų išsiskyrimu. Gautas tirpalas yra žalsvai gelsvos spalvos, kuri neišnyksta verdant.
Katinas Bazilijus. Reakcija vyksta, kai išsiskiria bespalvės dujos ir yra tokia pat stipri kaip
adresu Pinokis. Sprendimas tampa gražusšviesiai rausvos spalvos. Visiškai ištirpus metalui, mėgintuvėlio apačioje lieka šiek tiek smulkių miltelių.
9-4 užduotis
Nuosėdos, gautos veikiant 400 g 8% vario (II) sulfato tirpalo su atskiestu amoniako tirpalu (kurio buvo paimta tiek, kad visiškai nusodintų nuosėdas) (1), filtruojamos, išdžiovinamos ir kalcinuojamos. stikliniame vamzdyje iki 300 °C inertinių dujų srovėje (2). Dujinės medžiagos vamzdžio išleidimo angoje buvo leidžiamos per 360 g sveriančią kieto šarmo kolonėlę, kurios masė padidėjo 5%.
Laikant tokį patį kiekį oru išdžiovintų nuosėdų eksikatoriuje virš koncentruotos sieros rūgšties, rūgšties masė padidėja 7,2 g (3).
1. Atlikę reikiamus skaičiavimus, nustatykite:
Dėl reakcijos (1) nusodintos medžiagos formulė; - nuosėdų deginimo metu susidariusios medžiagos formulė, ją apskaičiuokite
masę ir nurodykite jos pavadinimą.
2. Parašykite reakcijų lygtis (1 - 3);
3. Nurodykite, kuriai klasei priklauso nusodinta medžiaga, kuri nusėda dėl reakcijos (1).
9-5 užduotis
Chemike, atsiminkite, kaip odė: įpilkite rūgšties į vandenį.
Gerai žinoma, kad koncentruotai sieros rūgščiai reaguojant su vandeniu išsiskiria daug šilumos. Termodinamikos vadove galima rasti
šie duomenys apie sieros rūgšties susidarymo šilumą (Q f ).Q f , kJ mol−1
H2SO4 (l) 813,99
H2SO4 (ai) 909,27
Skliausteliuose esantys indeksai turi šias reikšmes: (l) skysta rūgštis, (ai) rūgštis, visiškai jonizuota vandenyje.
1. Kiek šilumos išsiskiria, kai 1 molis iš 100% sieros rūgšties vandens kiekyje, kurio pakaktų visiškai jonizuoti rūgštį?
2. Kokios masės vandens su tokiu šilumos kiekiu galima pašildyti nuo 25°C iki 100°C? Apsvarstykite, kad vandens šiluminė talpa C p lygus 75.3 J mol−1 K−1
Ir nepriklauso nuo temperatūros.
3. Kokios masės vandens galima pašildyti nuo 25°C iki 100°C ir su juo išgarinti
toks šilumos kiekis? Vandens garavimo šiluma 100°С temperatūroje yra 40,66 kJ mol−1.
4. Remdamiesi skaičiavimais, paaiškinkite, kodėl skiedžiant koncentruotą sieros rūgštį, ją reikia mažomis porcijomis pilti į vandenį, o ne atvirkščiai.
DEŠIMTA KLASĖ
10-1 užduotis
Į rūgšties tirpalus buvo pridėta baltos miltelių pavidalo medžiagos X. Eksperimentų rezultatai pateikti lentelėje.
Ir pridedant bario chlorido.
10-2 užduotis
Kalis yra svarbiausias biogeninis elementas, kuris yra gyvūnų ir augalų ląstelių dalis. Kai organizme trūksta kalio, išsivysto hipokalemija, sutrinka širdies ir skeleto raumenų darbas. Pagrindiniai kalio šaltiniai žmonėms yra kepenys, pienas, žuvis, džiovinti abrikosai, melionai, pupelės, kiviai, bulvės, avokadai, bananai, brokoliai, citrusiniai vaisiai, vynuogės. Dėl kalio trūkumo dirvožemyje stabdomas augalų augimas ir labai sumažėja derlius, todėl apie 90 % išgautų kalio druskų panaudojama cheminių trąšų gamybai.
Kalis metalas yra itin chemiškai aktyvus: jau kambario temperatūroje reaguoja su vandeniu, chloru, sieros vandeniliu, o kaitinamas – su amoniaku, vandeniliu, raudonuoju fosforu ir daugybe kitų medžiagų.
1. Parašykite reakcijų lygtis, kurio pagalba problemoje apibūdinamos kalio metalo cheminės savybės.
Dėl padidėjusio reaktyvumo laisvojo kalio gamtoje nerandama. Nepaisant to, kalio elemento mūsų planetoje yra gana daug: pagal paplitimą jis užima 7 vietą tarp visų elementų, sudaro nemažai savo mineralų ir yra jūros vandens dalis. Kalio kiekis žemės plutoje yra 2,4 masės. %, jūros vandenyje 0,0371 masės. %.
2. Išvardykite elementus, kurių masė žemės plutoje yra didesnė nei kalio.
3. Pateikite dviejų mineralų, kuriuose yra kalio, pavyzdžius (formulės, mineraloginiai ir cheminiai pavadinimai).
kalio koncentracija jūros vandenyje mol/l, jei vidutinis jūros vandens tankis
1,025 g/cm3.
Natūralus kalis susideda iš dviejų stabilių izotopų 39 K ir 41 K ir radioaktyvaus 40 K (pusėjimo laikas 1,251 109 metai). Kiekviename natūralaus kalio grame per sekundę suyra vidutiniškai 32 branduoliai 40 K, dėl ko, pavyzdžiui, 70 kg sveriančiame žmogaus kūne kas sekundę įvyksta apie 4000 radioaktyvių skilimų.
suiręs. Nepaisant to, kad jo skilimas vyksta iš karto dviem kryptimis (β – skilimas ir elektroninis, arba K-fiksavimas), bendras pusinės eliminacijos laikas yra gana didelis (1,248 109 metai). 40 K koncentracijos ir vieno iš jos produktų koncentracijos santykis
irimas izoliuotose uolienose naudojamas absoliučiam jų amžiui nustatyti; šis metodas yra vienas pagrindinių branduolinės geochronologijos metodų.
6. Parašykite 40 K izotopo branduolinio skilimo reakcijų lygtis Remdamiesi atominės masės dydžiu, įvertinkite stabilaus izotopo 41 K santykinį kiekį natūraliame mišinyje. Taip pat įvertinkite, prieš kiek metų 40 K kiekis natūraliame izotopų mišinyje buvo 0,0936%.
10-3 užduotis
Kartą Karabasas-Barabasas, perskaitęs chemijos vadovėlį, pareikalavo, kad aktoriai ištirtų mangano sąveiką su įvairiomis rūgštimis. Kai kuriems veikėjams buvo duotas chemiškai grynas manganas, o likusiems – metalas, kuriame buvo geležies ir vario mišinio. Naudojome 3 M druskos ir azoto rūgštis, 1 M sieros rūgštį ir dūmuojančią (100 %) azoto rūgštį, kurių buvo paimta perteklius metalo atžvilgiu. Duremaras kiekvienam veikėjui suteikė po vieną metalo pavyzdį ir vieną buteliuką rūgšties. Lėlės stebėjimai buvo įrašyti į laboratorinius žurnalus. Pažvelkime į šių žurnalų įrašus.
Pinokis. Reakcija vyksta energingai ir nereikalauja kaitinimo. Išsiskiria bespalvės dujos, kurios, pakėlus degtuką, su vata sprogsta. Metalas tirpsta be likučių.Malvina. Reakcija nevyksta taip stipriai kaip mėgintuvėlyje Pinokyje. Išsiskiria bespalvės, degios dujos, bekvapės ir beskonės. Visiškai ištirpus metalui, mėgintuvėlio apačioje lieka šiek tiek smulkių miltelių.
Pierrot. Reakcija nevyksta taip stipriai kaip mėgintuvėlyje Pinokyje. Metalas ištirpsta be likučių. Kai į tirpalą įpilama natrio sulfido, susidaro juodos nuosėdos. Iš mėgintuvėlio išsiskiriančios dujos turi vos pastebimą geltonai oranžinę spalvą, kuri išnyksta, kai dujos praleidžiamos per šarmą. Dujos, patekusios per šarmą, yra bespalvės, o pakėlus degtuką su vata sprogsta.
Lapė Alisa. Veikiant rūgščiai, metalo paviršius pasidengia balkšva danga, dujos neišsiskiria. Įpylus nedidelį kiekį vandens, prasideda energinga reakcija su rudų dujų išsiskyrimu. Gautas tirpalas yra žalsvai gelsvos spalvos, kuri neišnyksta verdant.
Katinas Bazilijus. Reakcija vyksta išskiriant bespalves dujas ir yra tokia pat energinga kaip ir Pinokio. Tirpalas įgauna gražią šviesiai rausvą spalvą. Visiškai ištirpus metalui, mėgintuvėlio apačioje lieka šiek tiek smulkių miltelių.
Darbo metu veikėjai pamiršo, kurį iš metalo pavyzdžių ir kokią rūgštį panaudojo. Už tai grėsė bausmė. Tačiau popiežius Carlo išgelbėjo situaciją ir nesunkiai atkūrė trūkstamą informaciją.
Tą patį padarykite ir jūs, lentelėje pateikdami galutinį atsakymą.
Pateikite metalų sąveikos su rūgštimis reakcijų lygtis ir koreliuokite jas su įrašais laboratoriniuose žurnaluose.
10-4 užduotis
Tam tikras kiekis izomerinių angliavandenilių A ir B mišinio buvo patalpintas į 10 litrų vakuuminį autoklavą, po kurio slėgiu buvo įpiltas 10 kartų (moliais) didesnis deguonies kiekis. Reakcijos mišinys kaitinamas iki 350 °C. Slėgis autoklave pasirodė 568,48 kPa. Per autoklavą buvo perleista elektros kibirkštis. Visiškai sudeginus angliavandenilius, slėgis vėl buvo matuojamas toje pačioje temperatūroje. Paaiškėjo, kad jis lygus 647,14 kPa. Gautas dujų mišinys praleidžiamas per kalkių vandens tirpalą; Susidarė 50,0 g nuosėdų.
1. Nustatykite angliavandenilių A ir B molekulinę formulę. Pagrįskite savo atsakymą skaičiavimais.
2. Nurodykite galimų izomerinių angliavandenilių, atitinkančių šią formulę ir nepanaikinančių vandeninio kalio permanganato tirpalo, skaičių.
Yra žinoma, kad angliavandeniliai A ir B yra hidrinami aukštesnėje temperatūroje ir slėgyje; šiuo atveju iš abiejų susidaro tie patys hidrinimo produktai C ir D. Yra žinoma, kad molekulėje A yra 4, o molekulėje B - 6 vandenilio atomų tipai.
3. A-D.
4. Parašykite A reakcijos su HBr produktus.
10-5 užduotis
Lentelėje pateikiamos standartinės ClF, BrF ir BrCl junginių susidarymo entalpijos dujų fazėje esant 298 K temperatūrai ir šių molekulių surišimo energija.
1. Remdamiesi šiais duomenimis, nustatykite jungimosi energijas fluoro, chloro ir bromo molekulėse. Nubraižykite įprastu masteliu (grafiką galima sudaryti ant užrašų knygelės lapo ir nenurodant kiekių verčių) Ebondo priklausomybę nuo halogeno atominės masės (F, Cl, Br ir I)
2. Dujinio chloro(III) fluorido susidarymo entalpija –158,9 kJ mol−1. Apskaičiuokite Cl-F surišimo energiją šioje molekulėje ir paaiškinkite, kodėl ji skiriasi nuo rišimosi energijos dviatominėje molekulėje.
3. Ryšio ilgiai ClF, BrF ir BrCl molekulėse yra atitinkamai 0,162, 0,176 ir 0,214 nm. Nustatykite fluoro, chloro ir bromo atomų kovalentinius spindulius. Raskite jungties ilgį Cl2 molekulėje.
Ryšio energija yra reakcijos ABg = Ag + Br entalpija

VIENUOTOKOJA KLASĖ
11-1 užduotis
Į rūgšties tirpalus buvo pridėta baltos miltelių pavidalo medžiagos X. Eksperimentų rezultatai pateikti lentelėje.
1. Nustatykite pridėtos medžiagos sudėtį (formulę). Parašykite jo pavadinimą.
2. Parašykite lygtis tų reakcijų, kurios vyksta tirpimo metu.
3. Kokių medžiagų gali būti galutiniame tirpale?
4. Dėl pridėtos medžiagos X parašykite reakcijas, kurios vyksta kaitinant
Ir pridedant bario chlorido.
11-2 užduotis
Chemijos laboratorijoje rasta kolba su pilkai juodais nežinomos X medžiagos kristalais, netirpiais vandenyje. Norėdamas nustatyti jų sudėtį, laborantas pasvėrė 14,22 g kristalų ir veikė juos dideliu praskiesto azoto rūgšties tirpalo pertekliumi. Kristalai visiškai ištirpo ir tirpalas pasidarė rudas (1 reakcija). Gautas tirpalas buvo padalintas į tris lygias dalis.
Antroji tirpalo dalis buvo apdorota kalio jodido tirpalu ir kaitinama iki virimo. Šiuo atveju išsiskyrė violetiniai garai, susidarė žalias tirpalas ir rudos nuosėdos (5–6 reakcijos). Nuosėdos atskirtos, plaunamos natrio tiosulfato tirpalu, dėl to jos pasidarė baltos (7 reakcija), po to išdžiovinamos ir pasvertos. Nuosėdų masė 2,865 g, jose yra 33,51 % (masės) metalo. Baltos nuosėdos visiškai ištirpusios natrio tiosulfato tirpalo perteklyje (8 reakcija)
KAM natrio bromidas buvo pridėtas į trečią rudo tirpalo dalį, tirpalas virinamas (9 reakcija). Tirpalui atvėsus, į jį pilamas koncentruotas amoniako tirpalas (reakcijos 10–12). Tirpalas pamėlynavo, iš jo iškrito pilkai žalios nuosėdos, kurias deginant (13 reakcija) gauta 2,28 g žalių miltelių, kuriuose buvo 68,42 % (masės) kito metalo. Aprašytos transformacijos gali būti pateiktos diagramos pavidalu:
juodi milteliai | |||||||||||
mėlynos nuosėdos + ryškiai geltonas tirpalas | |||||||||||
HNO3 | |||||||||||
Ruda | violetiniai garai + žalias tirpalas + rudos nuosėdos |
||||||||||
7 plovimas |
|||||||||||
NaBr, NH3 | Na2 S2 O3 |
||||||||||
baltos nuosėdos |
|||||||||||
pilkai žalios nuosėdos + mėlynas tirpalas |
|||||||||||
žalios spalvos milteliai | Na2 S2 O3 |
||||||||||
bespalvis |
|||||||||||

Nustatykite nežinomos medžiagos X formulę, užrašykite visų minėtų reakcijų lygtis (1–13).
11-3 užduotis
Automobilių dalių gamybai naudojami smūgiams ir dilimui atsparūs plastikai
Ir buitinė technika, plastikinės kortelės, medicininė įranga, baldai. Plačiai paplitęs ABS plastikai yra akrilnitrilo, butadieno kopolimeras
ir stireno.
1. Nubraižykite išvardytų monomerų struktūrines formules.
ABS mėginyje (pagal masę) yra 87,67 % anglies, 7,99 % vandenilio ir azoto.
2. Apskaičiuokite kiekvieno polimero monomero molinę ir masės dalį.
3. Užrašykite visas įmanomas polimero grandininių augimo reakcijų (radikalinės polimerizacijos) lygtis, dėl kurių į polimerą patenka butadieno vienetas.
4. Kiek skirtingų diadų (nuoseklių nuorodų porų) gali egzistuoti aprašytajame ABS plastikas: a) darant prielaidą, kad visos grandinės augimo reakcijos vyksta visiškai regio- ir stereoselektyvumu; b) darant prielaidą, kad grandininės sklidimo reakcijos su butadieno vienetu nėra selektyvios?
Yra žinoma, kad polistirenas ir stireno kopolimerai su akrilnitrilu yra stipri, bet gana trapi medžiaga (ji suyra esant mažoms deformacijoms), o polibutadienas yra guma, galinti be ardymo atlikti dideles grįžtamas deformacijas. ABS plastikas sujungia didelį stiprumą ir atsparumą deformacijai.
5. Kaip polimero grandinėje pasiskirsto komonomerų vienetai ABS plastikai (atsitiktinai, griežtai kaitaliojami, identiškų grandžių grupės)? Pagrįskite savo atsakymą.
Naudokite molines mases iki artimiausio visos atominės masės vieneto.
11-4 užduotis
Nustatyta, kad organinėms molekulėms ir tarpiniams junginiams yra maždaug eksponentinė C-C jungties ilgio (L , Å) priklausomybė nuo jo eilės (K ):
L = ae − bK
Angliavandenilyje I (ωC : ωH = 4)L I = 0,154 nm, o angliavandenilyje II L II = 0,120 nm.
1. Iššifruokite I ir II formules, jei M I/MII = 1,154. Nurodykite hibridizacijos tipą
C atomai I ir II molekulėse.
2. Apskaičiuokite koeficientų a ir b reikšmes. Benzeno molekulės K įvertinimas (L = 0,140 nm). Pastaba: atsakymuose nurodykite tris reikšmingus skaičius.
Gautą K reikšmę, naudojant Kekule terminologiją, galima paaiškinti „benzeno žiede esančių ryšių svyravimais“ (nors teisingiau sakyti, kad benzeno molekulė egzistuoja dviem mezomerinėmis formomis):
Tokio „svyravimo“ galimybę (egzistavimas dviejų mezomerinių formų pavidalu) rodė, pavyzdžiui, duomenys apie angliavandenilio III redukcinį ozonavimą, dėl kurio susidaro junginių X, Y ir Z mišinys molinėje masėje. santykis 1:2:3. III galima gauti iš II pagal schemą :
III+IV |
|||||||
Pd/BaSO4 | |||||||
Pb(OAc)2 | O2/Ag | 4H2 |
|||||
1) +C | |||||||
2) H3O+
3. Parašykite junginių struktūrines formules A–G, X–Z, III ir IV.
4. Nustatykite dehidrogenavimui naudojamo katalizatoriaus formulę
G, jei jame yra Al (29,51%), O (34,97%) ir elementas X.

11-5 užduotis
Chloracto rūgštis veikiant vandeniui paverčiama glikolio rūgštimi. Reakcija vyksta pagal lygtį
ClCH2COOH + H2O = HOCH2COOH + HCl.
Esant dideliam vandens pertekliui, reakcija chloracto rūgšties atžvilgiu yra pirmoji, o vandens atžvilgiu – nulis.
Reakcijos kinetika buvo tiriama titruojant. Tam iš reakcijos mišinio buvo paimti mėginiai ir titruojami NaOH tirpalu. Žemiau pateikiami šarmų tūriai, naudojami titruojant skirtingu reakcijos laiku.
1. Kokia yra reakcijos greičio konstanta?
2. Po kiek laiko po reakcijos pradžios visos trys rūgštys bus mišinyje vienodai?
3. Koks yra chloracto rūgšties pusinės eliminacijos laikas tokiomis sąlygomis?
4. Po kurio laiko mišinyje liks 25% pradinio chloracto rūgšties kiekio?
Nuoroda informacija:
Pirmos eilės reakcijoms k t = lnC C 0 , kur k yra reakcijos greičio konstanta, C 0 yra
pradinė medžiagos koncentracija, C – medžiagos koncentracija laiko momentu t.
Gyvybės ekologija.Atrodytų nieko paprasčiau, sumalti grūdus, štai tau miltai. Tačiau tokie miltai yra prastai laikomi. Todėl gamintojai jį išvalo iš labiausiai žmogui naudingų medžiagų.
Atrodytų, nieko nėra lengviau, sumalkite grūdus, štai jums miltai. Tačiau tokie miltai yra prastai laikomi. Todėl gamintojai jį išvalo iš labiausiai žmogui naudingų medžiagų. Didelis vitaminų, mikroelementų ir skaidulų kiekis, kurio mums taip daug reikia, visa tai nueina perniek. Lieka beveik vienas krakmolas. Bet tai dar ne viskas. Kad miltai būtų pakankamai balti, jie balinami medžiagomis, apie kurias pakalbėsime plačiau.
Atkreipkite dėmesį, kad tos pačios medžiagos naudojamos skalbimo milteliuose ir buitinėje chemijoje dezinfekcijai ir balinimui. Faktas, verčiantis susimąstyti, ar verta duoną pirkti parduotuvėse, ar geriau ją išsivirti patiems, namuose.
KALIO BROMATAS- šis neorganinis junginys, kalio druska, gerai tirpsta vandenyje. Maisto priedų klasifikacijoje jis žymimas E924.
Tyrimai su gyvūnais parodė skydliaukės ir inkstų vėžio galimybę žiurkėms ir pelėms. Esant aukštai temperatūrai, kuri susidaro kepant, kalio bromatas virsta kalio bromidu, kuris laikomas nekenksmingu. Duona iš „bromuotų miltų“ yra puri ir nenatūraliai balta.
Kalio bromatas draudžiamas maisto pramonėje Rusijoje, ES šalyse, Kinijoje, Brazilijoje, Kanadoje. Leidžiama JAV.
CHLORO DIOKSIDAS- dujinė medžiaga, turi būdingą kvapą, neorganinis chloro ir deguonies junginys, galinga antimikrobinė medžiaga. Sprogstamosios. Maisto priedų klasifikacijoje jis žymimas E926.
Miltus apdirbus chloro dioksidu, visiškai pašalinami tokoferoliai (vitaminas E), nepakeičiamos riebalų rūgštys. Tyrimai su pelėmis parodė, kad šeriant duona iš miltų, apdorotų chloro dioksidu, gyvūnai patyrė E-avitaminozę.
Priedas E926 leidžiamas Rusijoje, jis taip pat naudojamas dezinfekcijai ir geriamojo vandens valymui.
BENZOILO PEROKSIDAS- organinis aromatinės serijos junginys, balta miltelių pavidalo medžiaga. Maisto priedų klasifikacijoje jis žymimas E928.
Naudojamas miltams balinti, ir kaip kepimo geriklis. Benzoilo peroksidu apdoroti miltai yra puresni ir baltesni. E928 kremų ir tepalų pavidalu dažnai naudojamas dezodoruojančių aliejų ir sūrių gamyboje bei spuogų gydymui. Gryna forma yra stiprus kancerogenas (medžiaga, kuri provokuoja piktybinių navikų atsiradimą).
Patvirtintas Rusijoje naudoti kepimo pramonėje.
AMONIO PERSULFATAS- organiškai aktyvus junginys, amonio druska. Maisto priedų klasifikacijoje jis žymimas E923.
Turi trečią pavojingumo klasę. Įkvėptas gali sukelti sunkų astmos priepuolį, pavojingą odai ir akims.
Amonio persulfatas yra uždraustas maisto gamyboje visose pasaulio šalyse, įskaitant Rusiją. Bet kartais naudojamas kaip kepimo milteliai tešlai, miltų balinimui, gaiviųjų gėrimų ir konditerijos gaminių gamyboje, kaip glazūravimo priemonė.
ALOKSANAS- junginys, gaunamas oksiduojant šlapimo rūgštį.
Aloksanas slopina daugelio fermentų veikimą. Eksperimentiniams gyvūnams sukelia Langerhanso salelių nekrozę (specialių kasos ląstelių sankaupas), inkstų kanalėlių nekrozę ir kitus ne tokius ryškius hipofizės, užkrūčio liaukos, antinksčių ir skydliaukės pakitimus. Jis naudojamas eksperimentiniam diabetui su gyvūnais gauti ir toliau tiriant įvairius vaistus.
Manoma, kad aloksanas nėra toks toksiškas žmonėms kaip gyvūnams.
Pasirodo, balti miltai iš tikrųjų yra krakmolas, kuris geriausiu atveju bus nenaudingas žmogui, blogiausiu net pavojingas. Žinoma, geriausia naudoti viso grūdo miltus. Arba bent jau sumažinti produktų, pagamintų iš baltų miltų, naudojimą.
Prašau parodyti sveiką protą!
UŽDUOTYS
pirmajam (korespondenciniam) turui chemijoje
Kaspijos tarpregioninė moksleivių olimpiada
10-1 užduotis
balta miltelių pavidalo medžiaga X dedama į rūgščių tirpalus. Eksperimentų rezultatai pateikti lentelėje.
Klausimai:
1. Nustatykite pridėtos medžiagos sudėtį (formulę). Parašykite jo pavadinimą.
2. Parašykite reakcijų, vykstančių tirpimo metu, lygtį.
3. Kokių medžiagų gali būti galutiniame tirpale?
4. Dėl pridėtos medžiagos X Parašykite reakcijas, kurios vyksta kaitinant ir įpilant bario chlorido.
10-2 užduotis
Kalis yra svarbiausias biogeninis elementas, kuris yra gyvūnų ir augalų ląstelių dalis. Kai organizme trūksta kalio, išsivysto hipokalemija, sutrinka širdies ir skeleto raumenų darbas. Pagrindiniai kalio šaltiniai žmonėms yra kepenys, pienas, žuvis, džiovinti abrikosai, melionai, pupelės, kiviai, bulvės, avokadai, bananai, brokoliai, citrusiniai vaisiai, vynuogės. Dėl kalio trūkumo dirvožemyje stabdomi augalai ir smarkiai sumažėja derlius, todėl apie 90 % išgautų kalio druskų panaudojama cheminėms trąšoms gaminti.
Kalis metalas yra itin chemiškai aktyvus: jau kambario temperatūroje reaguoja su vandeniu, chloru, sieros vandeniliu, o kaitinamas – su amoniaku, vandeniliu, raudonuoju fosforu ir daugybe kitų medžiagų.
1. Parašykite reakcijų lygtis, kurių pagalba apibūdinamos metalinio kalio cheminės savybės uždavinyje.
Dėl padidėjusio reaktyvumo laisvojo kalio gamtoje nerandama. Nepaisant to, kalio elemento mūsų planetoje yra gana daug: pagal paplitimą jis užima 7 vietą tarp visų elementų, sudaro nemažai savo mineralų ir yra jūros vandens dalis. Kalio kiekis žemės plutoje yra 2,4 masės. %, jūros vandenyje 0,0371 masės. %.
2. Išvardykite elementus, kurių masė žemės plutoje yra didesnė nei kalio.
3. Pateikite dviejų mineralų, kuriuose yra kalio, pavyzdžius (formulės, mineraloginiai ir cheminiai pavadinimai).
4. Apskaičiuokite bendrą kalio kiekį žemės plutoje atomų vienetais, jei žinoma, kad žemės plutos masė yra 2,8 1019 tonų. Apskaičiuokite vidutinę kalio koncentraciją jūros vandenyje mol/l, jei vidutinis jūros vandens tankis yra 1,025 g/cm3.
Natūralų kalį sudaro du stabilūs izotopai 39K ir 41K ir radioaktyvusis 40K (pusėjimo laikas 1,251 109 metai). Kiekviename natūralaus kalio grame per sekundę suyra vidutiniškai 32 40K branduoliai, dėl ko, pavyzdžiui, 70 kg sveriančiame žmogaus kūne kas sekundę įvyksta apie 4000 radioaktyvių skilimų.
40K kiekis natūraliame izotopų mišinyje yra 0,0117%. Visi žemėje esantys 40 000 susidarė tuo pačiu metu, kai atsirado pati planeta, ir nuo to laiko palaipsniui nyko. Nepaisant to, kad jo skilimas vyksta iš karto dviem kryptimis (β-skilimas ir elektroninis, arba K-fiksavimas), bendras pusinės eliminacijos laikas yra gana ilgas (1,248 109 metai). Išskirtose uolienose absoliučiam jų amžiui nustatyti naudojamas 40K koncentracijos ir vieno iš jo skilimo produktų koncentracijos santykis; šis metodas yra vienas pagrindinių branduolinės geochronologijos metodų.
6. Parašykite 40K izotopo branduolinio skilimo reakcijų lygtis. Remdamiesi atominės masės verte, įvertinkite santykinį stabilaus izotopo 41K kiekį natūraliame mišinyje. Taip pat įvertinkite, prieš kiek metų 40K kiekis natūraliame izotopų mišinyje buvo 0,0936%.
10-3 užduotis
Kartą Karabasas-Barabasas, perskaitęs chemijos vadovėlį, pareikalavo, kad aktoriai ištirtų mangano sąveiką su įvairiomis rūgštimis. Kai kuriems veikėjams buvo duotas chemiškai grynas manganas, o likusiems – metalas, kuriame buvo geležies ir vario mišinio. Naudojome 3M druskos ir azoto rūgštis, 1M sieros rūgštį ir dūmingą (100%) azoto rūgštį, kurių buvo paimta per daug, palyginti su metalu. Duremaras kiekvienam veikėjui suteikė po vieną metalo pavyzdį ir vieną buteliuką rūgšties. Lėlės stebėjimai buvo įrašyti į laboratorinius žurnalus. Pažvelkime į šių žurnalų įrašus.
Pinokis. Reakcija vyksta energingai ir nereikalauja kaitinimo. Išsiskiria bespalvės dujos, kurios, pakėlus degtuką, su vata sprogsta. Metalas ištirpsta be likučių.
Malvina. Reakcija nevyksta taip stipriai kaip mėgintuvėlyje Pinokyje. Išsiskiria bespalvės, degios dujos, bekvapės ir beskonės. Visiškai ištirpus metalui, mėgintuvėlio apačioje lieka šiek tiek smulkių miltelių.
Pierrot. Reakcija nevyksta taip stipriai kaip mėgintuvėlyje Pinokyje. Metalas ištirpsta be likučių. Kai į tirpalą įpilama natrio sulfido, susidaro juodos nuosėdos. Iš mėgintuvėlio išsiskiriančios dujos turi vos pastebimą geltonai oranžinę spalvą, kuri išnyksta, kai dujos praleidžiamos per šarmą. Dujos, patekusios per šarmą, yra bespalvės, pakėlus degtuką su vata sprogsta.
Lapė Alisa. Veikiant rūgščiai, metalo paviršius pasidengia balta danga, dujos neišsiskiria. Įpylus nedidelį kiekį vandens, prasideda energinga reakcija su rudų dujų išsiskyrimu. Gautas tirpalas yra žalsvai gelsvos spalvos, kuri neišnyksta verdant.
Katinas Bazilijus. Reakcija vyksta išskiriant bespalves dujas ir yra tokia pat energinga kaip ir Pinokio. Tirpalas įgauna gražią šviesiai rausvą spalvą. Visiškai ištirpus metalui, mėgintuvėlio apačioje lieka šiek tiek smulkių miltelių.
Darbo metu veikėjai pamiršo, kurį iš metalo pavyzdžių ir kokią rūgštį panaudojo. Už tai grėsė bausmė. Tačiau popiežius Carlo išgelbėjo situaciją ir nesunkiai atkūrė trūkstamą informaciją.
Padarykite tai patys, lentelėje pateikdami galutinį atsakymą.
Pateikite metalų sąveikos su rūgštimis reakcijų lygtis ir koreliuokite jas su įrašais laboratoriniuose žurnaluose.
10-4 užduotis
Kažkoks izomerinių angliavandenilių mišinys BET Ir IN patalpintas į vakuuminį 10 l tūrio autoklavą, po to 10 kartų (moliais) slėgiu buvo įpiltas deguonies kiekis. Reakcijos mišinys kaitinamas iki 350 °C. Slėgis autoklave pasirodė 568,48 kPa. Per autoklavą buvo perleista elektros kibirkštis. Po to, kai angliavandeniliai visiškai sudeginami. Slėgis buvo matuojamas dar kartą toje pačioje temperatūroje. Paaiškėjo, kad jis lygus 647,14 kPa. Gautas dujų mišinys praleidžiamas per kalkių vandens tirpalą; Susidarė 50,0 g nuosėdų.
1. Nustatykite angliavandenilių molekulinę formulę BET Ir IN. Atsakymą pagrįskite skaičiavimais.
2. Nurodykite galimų izomerinių angliavandenilių, atitinkančių šią formulę ir nepanaikinančių vandeninio kalio permanganato tirpalo, skaičių.
3. Yra žinoma, kad angliavandeniliai BET Ir IN yra hidrinami aukštesnėje temperatūroje ir slėgyje; tuo pačiu metu iš abiejų susidaro tie patys hidrinimo produktai NUO Ir D . Yra žinoma, kad molekulėje BET yra 4, o molekulėje IN 6 tipų vandenilio atomai.
4. Parašykite junginių struktūrines formules BET- D .
5. Parašykite reakcijos produktus BET iš HBr .
10-5 užduotis
Lentelėje pateikiamos standartinės ClF, BrF ir BrCl junginių susidarymo entalpijos dujų fazėje esant 298 K temperatūrai ir šių molekulių surišimo energija.
Klausimai:
1. Remdamiesi šiais duomenimis, nustatykite surišimo energijas fluoro, chloro ir bromo molekulėse. Paveikslėlis sąlyginė skalė(grafiką galima sudaryti ant užrašų knygelės lapo nenurodant kiekių verčių) Ebondo priklausomybė nuo halogeno atominės masės ( F , Cl , Br , aš ).
2. Dujinio chloro fluorido susidarymo entalpija ( III ) yra lygus – 158,9 kJ mol-1. Apskaičiuokite surišimo energiją Cl - F šioje molekulėje ir paaiškinkite, kodėl ji skiriasi nuo surišimo energijos dviatominėje molekulėje.
3. Ryšių ilgiai molekulėse ClF , BrF Ir BrCl yra lygūs atitinkamai 0,162, 0,176 ir 0,214 nm. Nustatykite fluoro, chloro ir bromo atomų kovalentinius spindulius. Raskite jungties ilgį molekulėje Cl 2 .
Ryšio energija yra reakcijos ABr=Ar+Br entalpija.
Esame įpratę, kad soda visada „po ranka“. O kepimui jis reikalingas, ir išvalys virtuvėje visas dėmes, nublizgins sidabrą, naikins pelėsius. O kodėl jo nepanaudojus medicininiais tikslais: per karštą tirpalą kvėpuoti peršalus, gerti nuo rėmens, kai neišgydoma. Net kartais iš jo gaminame gazuotą gėrimą.
Civilizuotame Europos pasaulyje soda buvo žinoma nuo seno, ji buvo naudojama tiek muilo, stiklo gamybai, tiek įvairiems dažams ir net vaistams gaminti.
Nepastebimas popierinis baltas paketas stovi ant virtuvės lentynos ir gali padėti bet kurią akimirką. Sodos milteliai gali pakeisti daugybę cheminių junginių. Esame įpratę ir tiesiog nesusimąstome, iš kur ji atsiranda ir kaip atrodo sodos gamyba.
Kaip pradėjote gaminti soda?
Su šia medžiaga žmogus susidūrė senovėje. Jis buvo naudojamas išgaunant iš sodos ežerų ir nedidelių naudingųjų iškasenų telkinių. Europoje iš jo buvo gaminamas muilas, dažai, stiklas ir net vaistai. Šios baltos miltelių pavidalo medžiagos šaltinis buvo jūros dumblių pelenai. Tačiau pramonei šios sumos nepakako.
Gamtoje Užbaikalėje ir Vakarų Sibire yra sodos ežerų.
Natrono ežeras Tanzanijoje ir Searlso ežeras Kalifornijoje yra žinomi. Jungtinėms Valstijoms priklauso dideli šios natūralios medžiagos rezervai: jos savo reikmėms naudoja 40% natūralios sodos ir artimiausiais dešimtmečiais atsargų išeikvojimas nenumatomas. Rusija neturi didelių telkinių, todėl medžiaga gaunama tik cheminiais metodais.
Vienas pirmųjų buvo pritaikytas pramoninis metodas, kurį 1791 m. išrado prancūzų chemikas Leblanc. Metodas buvo pagrįstas natrio karbonato ekstrahavimu iš akmens druskos. Technologija nebuvo tobula: susidarė nemažas kiekis atliekų. Tačiau pradžia buvo padaryta: „baltosios medžiagos“ kaina sumažėjo, o įsigijimo poreikis išaugo.
Leblanc metodas buvo plačiai naudojamas, tačiau juo buvo gaminami tik sodos pelenai. Kitas išradėjas buvo prancūzas Augustinas Jeanas Fresnelis, kuris 1810 m. atliko reakciją, gaudamas sodos miltelius, perleisdamas akmens druską per amoniako tirpalą ir anglies dioksidą. Tačiau gamyboje ši plėtra buvo nuostolinga. Nebuvo žinoma, kaip atgauti cikliniame gamybos procese reikalingą amoniaką.
 Iki šiol išgrynintas natrio bikarbonatas gaminamas dviem būdais: „sausu“ ir „šlapiu“.
Iki šiol išgrynintas natrio bikarbonatas gaminamas dviem būdais: „sausu“ ir „šlapiu“. Ir tik 1861 m. belgas Ernestas Solvay, remdamasis Fresnelio darbais, atliko reakciją, siekdamas atkurti amoniaką, todėl gamyba tapo pigi ir pakeista Leblanc metodu. Metodo ypatumas buvo tas, kad jis leido be sodos pelenų gauti kepimo soda.
Rusijoje jie sužinojo apie „baltąją medžiagą“ Petro Didžiojo valdymo laikais. Iki 1860 m. jis buvo importuojamas ir vadinosi „zoda“ arba „niežulys“. O 1864 metais buvo įkurta sava šio gaminio gamyba.
Kepimo sodos sudėtis
„Baltosios medžiagos“ veislių nėra tiek mažai:
- yra sodos pelenų arba natrio karbonato: Na2CO3;
- taip pat yra bikarbonato soda (geriamoji soda) arba natrio bikarbonatas NaHCO3;
- kristalinė soda Na2CO3*10H2O;
- kaustinė soda, turinti labai tolimą ryšį su maistu, yra NaOH.
Remiantis sintezės metodu, jis skirstomas į Leblanc ir amoniaką, antrasis yra grynesnis.
„Baltoji medžiaga“ gamtoje yra reta, o ne gryna forma. Šios sumos nepakanka pasaulio poreikiams patenkinti. Sodos gamyba siekia kelis milijonus tonų per metus.
Kepimo soda turi cheminį pavadinimą – natrio bikarbonatas arba natrio bikarbonatas, kurio formulė NaHCO3. Jis yra ištirpusios medžiagos pavidalu druskos ežerų ir jūros vandens priemaišose, yra uolienų sudėtyje.
Druskos gamybos procesas
Sodos gamyba iki šiol pagrįsta Solvay metodu. Kitu būdu šis metodas vadinamas amoniako chloridu. Koncentruotas natrio chlorido tirpalas prisotinamas amoniaku ir veikiamas anglies dioksidu.
Gautas natrio bikarbonatas blogai tirpsta šaltame vandenyje ir gali būti lengvai išskiriamas filtruojant. Tada atlikite kalcinavimo procesą, sudarydami sodos miltelius.
 Sodos pelenai gaminami amoniako metodu, sąveikaujant sočiam vandeniniam natrio chlorido ir anglies dioksido tirpalui, esant amoniakui, susidarant natrio bikarbonatui ir vėliau jį kalcinuojant.
Sodos pelenai gaminami amoniako metodu, sąveikaujant sočiam vandeniniam natrio chlorido ir anglies dioksido tirpalui, esant amoniakui, susidarant natrio bikarbonatui ir vėliau jį kalcinuojant. Žingsnis po žingsnio procesas atrodo taip:
- NaCl + NH3 + CO2 + H2O \u003d NaHCO3 + NH4Cl (galutinio produkto susidarymas vyksta vandenyje esant t \u003d + 30 - + 40 laipsnių).
- 2NaHCO3 = Na2CO3 + CO2 + H2O (CO2 nepašalinamas iš ciklinio proceso). Tai sodos pelenų reakcija.
- 2NH4Cl + CaO = CaCl2 + H2O + 2NH3. Taip atkuriamas amoniakas. Jis ir toliau vėl ir vėl dalyvauja gamyboje, rasdamas panaudojimą tolimesnėje gamyboje.
Šiuo metodu gaunama ir soda, ir soda. Abi medžiagos yra paklausios gaminant įvairius produktus. Solvay metodas leidžia sintetinti dviejų rūšių sodos miltelius vienu metu. Dabar tampa aišku, iš ko gaminama soda ir kokie komponentai dalyvauja cheminėse reakcijose.
Rusijoje medžiaga gaminama dviejose įmonėse - Sodos gamykloje Sterlitamake (Baškirijos Respublika) ir Krymo sodos gamyklos įmonėje Krasnoperekopske (Krymo Respublika). Tai aukštos kokybės gaminiai, atitinkantys GOST reikalavimus.
Gamybos procesas iš natūralių mineralų
Kadangi yra šalių, kuriose gausu mineralų, į kurias įeina ir mus dominanti medžiaga (pavyzdžiui, JAV, Uganda, Turkija, Meksika), žinomas ir paprastesnis sodas gamybos būdas iš mineralų nahkolito ir sosto. Iš jų galite pasigaminti sodos pelenų miltelius, o tada paversti maistu.
Sostas išgaunamas įvairiais būdais:
- Iškerpamos požeminės patalpos, kurias palaiko specialūs įrenginiai. Mineralas paimamas ant kambarių sienų, o tada perkeliamas konvejeriu.
- Karštas vanduo pilamas po žeme, kad ištirptų mineralas. Siurbiamas skystis išgarinamas, o susidarę demineralizuoti kristalai apdorojami.
Kristalai susmulkinami, kaitinami, kad pašalintų nepageidaujamas dujas, o mineralas paverčiamas sodos milteliais. Tačiau jame vis dar yra daug priemaišų, kurios pašalinamos įpilant vandens ir vėliau filtruojant. Gauta medžiaga džiovinama, sijojama ir supakuojama į paruoštus konteinerius jau įmonėje.
Sodos pelenų miltelių panaudojimas gana platus. Jis reikalingas stiklo, muilo, popieriaus gamybai. Jis naudojamas vandens valymui. Natrio bikarbonatą būtina naudoti medicinoje ir maisto pramonėje.
Kaip ir bet kurios cheminės gamybos atveju, sodos miltelių gamyba nėra ekologiška. Tačiau destruktyvus poveikis gamtai būtų daug stipresnis, jei jie pradėtų gaminti tas sintetines medžiagas, kurias soda gali sėkmingai pakeisti.