समाधान का इलेक्ट्रोलिसिस
और पिघला हुआ नमक (2 घंटे)
वैकल्पिक पाठ्यक्रम "इलेक्ट्रोकेमिस्ट्री" की कक्षाएं
पाठ 1 उद्देश्य:
P l n e r in o g o u r o k a
1. धातुओं को प्राप्त करने की अध्ययन की गई विधियों की पुनरावृत्ति।
2. नई सामग्री की व्याख्या।
3. जीई रुडज़ाइटिस द्वारा पाठ्यपुस्तक से समस्याओं का समाधान, एफजी फेल्डमैन "रसायन विज्ञान-9" (मास्को: शिक्षा, 2002), पी। 120, संख्या 1, 2.
4. परीक्षण वस्तुओं पर ज्ञान के आत्मसात की जाँच करना।
5. इलेक्ट्रोलिसिस के उपयोग के बारे में संदेश।
पाठ 1 उद्देश्य:समाधान और पिघले हुए लवणों के लिए इलेक्ट्रोलिसिस योजनाएं लिखना सिखाएं और कम्प्यूटेशनल समस्याओं को हल करने के लिए प्राप्त ज्ञान को लागू करें; पाठ्यपुस्तक, परीक्षण सामग्री के साथ काम करने में कौशल विकसित करना जारी रखें; राष्ट्रीय अर्थव्यवस्था में इलेक्ट्रोलिसिस के उपयोग पर चर्चा करें।
पहले पाठ की प्रक्रिया
सीखी गई विधियों की पुनरावृत्ति धातु प्राप्त करनाकॉपर (II) ऑक्साइड से कॉपर प्राप्त करने के उदाहरण पर।
संबंधित प्रतिक्रियाओं के समीकरण लिखना:
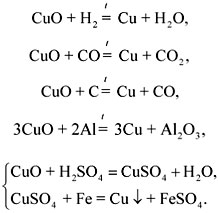
धातुओं को उनके लवणों के विलयनों और गलनों से प्राप्त करने का दूसरा तरीका है विद्युत, या इलेक्ट्रोलीज़.
इलेक्ट्रोलिसिस एक रेडॉक्स प्रक्रिया है जो इलेक्ट्रोड पर तब होती है जब एक विद्युत प्रवाह पिघल या इलेक्ट्रोलाइट समाधान के माध्यम से पारित किया जाता है.
सोडियम क्लोराइड पिघल इलेक्ट्रोलिसिस:
NaCl ना + + Cl -;
कैथोड (-) (ना +): ना + + इ= ना 0,
एनोड (-) (सीएल -): सीएल - - इ= सीएल 0, 2सीएल 0 = सीएल 2;
2NaCl = 2Na + Cl 2.
सोडियम क्लोराइड घोल का इलेक्ट्रोलिसिस:
NaCl Na + + Cl -,
एच 2 ओ एच + + ओएच -;
कैथोड (-) (ना +; एच +): एच + + इ= एच 0, 2 एच 0 = एच 2
(2एच 2 ओ + 2 इ= एच 2 + 2OH -),
एनोड (+) (सीएल -; ओएच -): सीएल - - इ= सीएल 0, 2सीएल 0 = सीएल 2;
2NaCl + 2H 2 O = 2NaOH + Cl 2 + H 2।
कॉपर (II) नाइट्रेट घोल का इलेक्ट्रोलिसिस:
घन (नं 3) 2 घन 2+ +
एच 2 ओ एच + + ओएच -;
कैथोड (-) (घन 2+; +): घन 2+ + 2 इ= घन 0,
एनोड (+) (ओएच -): ओह - - इ= ओह 0,
4 एच 0 = ओ 2 + 2 एच 2 ओ;
2Cu (NO 3) 2 + 2H 2 O = 2Cu + O 2 + 4HNO 3।
ये तीन उदाहरण बताते हैं कि धातु उत्पादन के अन्य तरीकों की तुलना में इलेक्ट्रोलिसिस अधिक लाभदायक क्यों है: धातु, हाइड्रॉक्साइड, एसिड, गैसें प्राप्त की जाती हैं।
हमने इलेक्ट्रोलिसिस योजनाएं लिखीं, और अब हम योजनाओं का जिक्र किए बिना, केवल आयन गतिविधि के पैमाने का उपयोग किए बिना, इलेक्ट्रोलिसिस समीकरणों को तुरंत लिखने का प्रयास करेंगे:
इलेक्ट्रोलिसिस समीकरणों के उदाहरण:
2HgSO 4 + 2H 2 O = 2Hg + O 2 + 2H 2 SO 4;
ना 2 SO 4 + 2H 2 O = Na 2 SO 4 + 2H 2 + O 2;
2LiCl + 2H 2 O = 2LiOH + H 2 + Cl 2।
समस्याओं को सुलझा रहाजीई रुडजाइटिस और एफजी फेल्डमैन (9वीं कक्षा, पृष्ठ 120, नंबर 1, 2) की पाठ्यपुस्तक से।
उद्देश्य 1.कॉपर (II) क्लोराइड के घोल के इलेक्ट्रोलिसिस के दौरान, कैथोड के द्रव्यमान में 8 ग्राम की वृद्धि हुई। कौन सी गैस निकली, इसका द्रव्यमान क्या है?
समाधान
CuCl 2 + H 2 O = Cu + Cl 2 + H 2 O,
(घन) = 8/64 = 0.125 मोल,
(Cu) = (Cl 2) = 0.125 mol,
एम(सीएल 2) = 0.125 71 = 8.875 ग्राम।
उत्तर... गैस - क्लोरीन वजन 8.875 ग्राम।
उद्देश्य 2.सिल्वर नाइट्रेट के जलीय घोल के इलेक्ट्रोलिसिस के दौरान 5.6 लीटर गैस निकली। कैथोड पर कितने ग्राम धातु जमा होती है?
समाधान
4AgNO 3 + 2H 2 O = 4Ag + O 2 + 4HNO 3,
(ओ 2) = 5.6 / 22.4 = 0.25 मोल,
(एजी) = 4 (ओ 2) = 4 25 = 1 मोल,
एम(एजी) = 1 107 = 107 ग्राम।
उत्तर... 107 ग्राम चांदी।
परिक्षण
विकल्प 1
1. कैथोड पर पोटेशियम हाइड्रॉक्साइड समाधान के इलेक्ट्रोलिसिस के दौरान, निम्नलिखित जारी किया जाता है:
ए) हाइड्रोजन; बी) ऑक्सीजन; ग) पोटेशियम।
2. समाधान में कॉपर (II) सल्फेट के घोल के इलेक्ट्रोलिसिस के दौरान, निम्नलिखित रूप होते हैं:
ए) तांबा (द्वितीय) हाइड्रॉक्साइड;
बी) सल्फ्यूरिक एसिड;
3. बेरियम क्लोराइड समाधान के इलेक्ट्रोलिसिस के दौरान, एनोड पर निम्नलिखित जारी किया जाता है:
ए) हाइड्रोजन; बी) क्लोरीन; ग) ऑक्सीजन।
4. पिघला हुआ एल्यूमीनियम क्लोराइड के इलेक्ट्रोलिसिस के दौरान, कैथोड पर निम्नलिखित छोड़ा जाता है:
ए) एल्यूमीनियम; बी) क्लोरीन;
c) इलेक्ट्रोलिसिस असंभव है।
5. सिल्वर नाइट्रेट विलयन का इलेक्ट्रोलिसिस निम्नलिखित योजना के अनुसार होता है:
ए) एग्नो 3 + एच 2 ओ एजी + एच 2 + एचएनओ 3;
बी) एग्नो 3 + एच 2 ओ एजी + ओ 2 + एचएनओ 3;
सी) एग्नो 3 + एच 2 ओ एग्नो 3 + एच 2 + ओ 2।
विकल्प 2
1. सोडियम हाइड्रॉक्साइड घोल के इलेक्ट्रोलिसिस के दौरान, एनोड पर निम्नलिखित छोड़ा जाता है:
ए) सोडियम; बी) ऑक्सीजन; ग) हाइड्रोजन।
2. घोल में सोडियम सल्फाइड के घोल के इलेक्ट्रोलिसिस के दौरान, निम्नलिखित रूप होते हैं:
ए) हाइड्रोजन सल्फाइड एसिड;
बी) सोडियम हाइड्रॉक्साइड;
3. पारा (II) क्लोराइड पिघलने के इलेक्ट्रोलिसिस के दौरान, कैथोड पर निम्नलिखित छोड़ा जाता है:
ए) पारा; बी) क्लोरीन; c) इलेक्ट्रोलिसिस असंभव है।
4.
5. पारा (II) नाइट्रेट के घोल का इलेक्ट्रोलिसिस निम्नलिखित योजना के अनुसार होता है:
ए) एचजी (एनओ 3) 2 + एच 2 ओ एचजी + एच 2 + एचएनओ 3;
बी) एचजी (एनओ 3) 2 + एच 2 ओ एचजी + ओ 2 + एचएनओ 3;
सी) एचजी (एनओ 3) 2 + एच 2 ओ एचजी (एनओ 3) 2 + एच 2 + ओ 2।
विकल्प 3
1. कॉपर (II) नाइट्रेट के घोल के इलेक्ट्रोलिसिस के दौरान, कैथोड पर निम्नलिखित छोड़ा जाता है:
ए) तांबा; बी) ऑक्सीजन; ग) हाइड्रोजन।
2. समाधान में लिथियम ब्रोमाइड के घोल के इलेक्ट्रोलिसिस के दौरान, निम्नलिखित रूप होते हैं:
बी) हाइड्रोब्रोमिक एसिड;
ग) लिथियम हाइड्रॉक्साइड।
3. सिल्वर क्लोराइड के पिघलने के इलेक्ट्रोलिसिस के दौरान, कैथोड पर निम्नलिखित छोड़ा जाता है:
ए) चांदी; बी) क्लोरीन; c) इलेक्ट्रोलिसिस असंभव है।
4. एल्यूमीनियम क्लोराइड समाधान के इलेक्ट्रोलिसिस के दौरान, एल्यूमीनियम को छोड़ा जाता है:
ए) कैथोड; बी) एनोड; c) विलयन में रहता है।
5. बेरियम ब्रोमाइड विलयन का इलेक्ट्रोलिसिस निम्नलिखित योजना के अनुसार होता है:
ए) बाबर 2 + एच 2 ओ बीआर 2 + एच 2 + बा (ओएच) 2;
बी) बाबर 2 + एच 2 ओ बीआर 2 + बा + एच 2 ओ;
सी) बाबर 2 + एच 2 ओ बीआर 2 + ओ 2 + बा (ओएच) 2.
विकल्प 4
1. बेरियम हाइड्रॉक्साइड घोल के इलेक्ट्रोलिसिस के दौरान, एनोड पर निम्नलिखित छोड़ा जाता है:
ए) हाइड्रोजन; बी) ऑक्सीजन; ग) बेरियम।
2. समाधान में पोटेशियम आयोडाइड के घोल के इलेक्ट्रोलिसिस के दौरान, निम्नलिखित रूप होते हैं:
ए) हाइड्रोयोडिक एसिड;
बी) पानी; ग) पोटेशियम हाइड्रॉक्साइड।
3. लेड (II) क्लोराइड के पिघलने के इलेक्ट्रोलिसिस के दौरान, कैथोड पर निम्नलिखित छोड़ा जाता है:
अगुवाई की; बी) क्लोरीन; c) इलेक्ट्रोलिसिस असंभव है।
4. कैथोड पर सिल्वर नाइट्रेट घोल के इलेक्ट्रोलिसिस के दौरान, निम्नलिखित जारी किया जाता है:
ए) चांदी; बी) हाइड्रोजन; ग) ऑक्सीजन।
5. सोडियम सल्फाइड के घोल का इलेक्ट्रोलिसिस निम्नलिखित योजना के अनुसार होता है:
ए) ना 2 एस + एच 2 ओ एस + एच 2 + नाओएच;
बी) ना 2 एस + एच 2 ओ एच 2 + ओ 2 + ना 2 एस;
सी) ना 2 एस + एच 2 ओ एच 2 + ना 2 एस + नाओएच।
जवाब
| विकल्प | प्रश्न 1 | प्रश्न 2 | प्रश्न 3 | प्रश्न 4 | प्रश्न 5 |
| 1 | ए | बी | बी | ए | बी |
| 2 | बी | बी | ए | ए | बी |
| 3 | ए | वी | ए | वी | ए |
| 4 | बी | वी | ए | ए | ए |
राष्ट्रीय अर्थव्यवस्था में इलेक्ट्रोलिसिस का उपयोग
1. धातु उत्पादों को जंग से बचाने के लिए, उनकी सतह पर एक और धातु की सबसे पतली परत लगाई जाती है: क्रोमियम, चांदी, सोना, निकल, आदि। कभी-कभी, महंगी धातुओं को बर्बाद न करने के लिए, वे एक बहुपरत कोटिंग का उत्पादन करते हैं। उदाहरण के लिए, कार के बाहरी हिस्से को पहले तांबे की एक पतली परत के साथ लेपित किया जाता है, तांबे पर निकल की एक पतली परत लगाई जाती है, और उस पर क्रोमियम की एक परत लगाई जाती है।
इलेक्ट्रोलिसिस द्वारा धातु पर कोटिंग करते समय, वे मोटाई और टिकाऊ में एक समान होते हैं। इस तरह, किसी भी आकार के उत्पादों को लेपित किया जा सकता है। अनुप्रयुक्त विद्युत रसायन की इस शाखा को कहा जाता है ELECTROPLATING.
2. संक्षारण संरक्षण के अलावा, गैल्वेनिक कोटिंग्स उत्पादों को एक सुंदर सजावटी रूप देती हैं।
3. इलेक्ट्रोकैमिस्ट्री की एक और शाखा, जो सैद्धांतिक रूप से इलेक्ट्रोप्लेटिंग के करीब है, इलेक्ट्रोफॉर्मिंग कहलाती है। यह विभिन्न वस्तुओं की सटीक प्रतिकृतियां बनाने की प्रक्रिया है। इसके लिए वस्तु पर मोम का लेप लगाया जाता है और एक मैट्रिक्स प्राप्त होता है। मैट्रिक्स पर कॉपी किए गए आइटम के सभी इंडेंटेशन बम्प्स होंगे। मोम मैट्रिक्स की सतह को ग्रेफाइट की एक पतली परत के साथ लेपित किया जाता है, जिससे यह प्रवाहकीय हो जाता है।
परिणामी ग्रेफाइट इलेक्ट्रोड को कॉपर सल्फेट के घोल से स्नान में डुबोया जाता है। एनोड कॉपर है। इलेक्ट्रोलिसिस के दौरान, कॉपर एनोड घुल जाता है और कॉपर ग्रेफाइट कैथोड पर जमा हो जाता है। इस प्रकार, एक सटीक तांबे की प्रति प्राप्त की जाती है।
इलेक्ट्रोप्लेटिंग की मदद से, छपाई के लिए क्लिच, ग्रामोफोन रिकॉर्ड बनाए जाते हैं, विभिन्न वस्तुओं को धातुकृत किया जाता है। इलेक्ट्रोफॉर्मिंग की खोज रूसी वैज्ञानिक बी.एस. जैकोबी (1838) ने की थी।
फोनोग्राफ रिकॉर्ड के लिए डाई बनाने में प्लास्टिक की प्लेट को विद्युत प्रवाहकीय बनाने के लिए बहुत पतली चांदी का लेप लगाना शामिल है। एक इलेक्ट्रोलाइटिक निकल चढ़ाना फिर प्लेट पर लगाया जाता है।
क्या प्लेट को इलेक्ट्रोलाइटिक बाथ में बनाया जाना चाहिए - एनोड या कैथोड?
(उत्तर। कैथोड।)
4. इलेक्ट्रोलिसिस का उपयोग कई धातुओं को प्राप्त करने के लिए किया जाता है: क्षार, क्षारीय पृथ्वी, एल्यूमीनियम, लैंथेनाइड्स, आदि।
5. कुछ धातुओं को अशुद्धियों से शुद्ध करने के लिए अशुद्धियों वाली धातु को एनोड से जोड़ा जाता है। धातु इलेक्ट्रोलिसिस के दौरान घुल जाती है और धातु कैथोड पर निकल जाती है, जबकि अशुद्धता घोल में रहती है।
6. इलेक्ट्रोलिसिस का व्यापक रूप से जटिल पदार्थ (क्षार, ऑक्सीजन युक्त एसिड), हैलोजन प्राप्त करने के लिए उपयोग किया जाता है।
व्यावहारिक कार्य(दूसरा पाठ)
पाठ मकसद।पानी के इलेक्ट्रोलिसिस का संचालन करें, अभ्यास में इलेक्ट्रोप्लेटिंग दिखाएं, पहले पाठ में प्राप्त ज्ञान को समेकित करें।
उपकरण।छात्रों की मेज पर: एक फ्लैट बैटरी, टर्मिनलों के साथ दो तार, दो ग्रेफाइट इलेक्ट्रोड, एक बीकर, टेस्ट ट्यूब, दो पैरों वाला एक तिपाई, एक 3% सोडियम सल्फेट समाधान, एक अल्कोहल लैंप, माचिस, एक मशाल।
शिक्षक की मेज पर: वही + कॉपर सल्फेट, पीतल की चाभी, कॉपर ट्यूब (तांबे का टुकड़ा) का घोल।
छात्रों को निर्देश देना
1. तारों को टर्मिनलों के साथ इलेक्ट्रोड में संलग्न करें।
2. इलेक्ट्रोड को एक गिलास में रखें ताकि वे स्पर्श न करें।
3. कांच में इलेक्ट्रोलाइट घोल (सोडियम सल्फेट) डालें।
4. परखनलियों में पानी डालें और उन्हें एक गिलास में ऊपर की ओर इलेक्ट्रोलाइट के साथ कम करके, उन्हें एक-एक करके ग्रेफाइट इलेक्ट्रोड पर डालें, टेस्ट ट्यूब के ऊपरी किनारे को ट्राइपॉड लेग में ठीक करें।
5. डिवाइस के माउंट होने के बाद, तारों के सिरों को बैटरी से जोड़ दें।
6. गैस के बुलबुले के निकलने का निरीक्षण करें: वे कैथोड से कम एनोड पर निकलते हैं। एक परखनली में लगभग सारा पानी बाहर निकलने वाली गैस से विस्थापित हो जाता है, और दूसरे में - आधे से, बैटरी से तारों को काट दें।
7. स्पिरिट लैंप जलाएं, टेस्ट ट्यूब को ध्यान से हटा दें, जहां पानी लगभग पूरी तरह से विस्थापित हो गया है, और इसे स्पिरिट लैंप में लाएं - गैस की एक विशेषता पॉप सुनाई देगी।
8. टॉर्च जलाएं। दूसरी परखनली निकालें, सुलगती मशाल से गैस की जांच करें।
छात्र असाइनमेंट
1. डिवाइस को स्केच करें।
2. जल विद्युत अपघटन का समीकरण लिखिए तथा समझाइए कि सोडियम सल्फेट विलयन में विद्युत अपघटन करना क्यों आवश्यक था।
3. इलेक्ट्रोड पर गैसों के विकास को दर्शाने वाले अभिक्रिया समीकरण लिखिए।
शिक्षक प्रदर्शन प्रयोग
(कक्षा के सर्वश्रेष्ठ छात्रों द्वारा किया जा सकता है
यदि उपयुक्त उपकरण उपलब्ध है)
1. वायर टर्मिनलों को कॉपर ट्यूब और ब्रास रिंच से कनेक्ट करें।
2. कॉपर (II) सल्फेट के घोल से ट्यूब और चाबी को गिलास में डालें।
3. तारों के दूसरे सिरों को बैटरी से कनेक्ट करें: बैटरी का "माइनस" कॉपर ट्यूब से, "प्लस" कुंजी से!
4. कुंजी की सतह पर तांबे के अवक्षेपण का निरीक्षण करें।
5. प्रयोग करने के बाद, पहले बैटरी से टर्मिनलों को डिस्कनेक्ट करें, फिर समाधान से कुंजी को हटा दें।
6. घुलनशील इलेक्ट्रोड के साथ इलेक्ट्रोलिसिस सर्किट को अलग करें:
CuSO 4 = Cu 2+ +
एनोड (+): u 0 - 2 इ= घन 2+,
कैथोड (-): Cu 2+ + 2 इ= क्यू 0.
घुलनशील एनोड के साथ इलेक्ट्रोलिसिस के लिए समग्र समीकरण नहीं लिखा जा सकता है।
इलेक्ट्रोलिसिस कॉपर (II) सल्फेट के घोल में किया गया था, क्योंकि:
a) विद्युत धारा प्रवाहित करने के लिए इलेक्ट्रोलाइट विलयन की आवश्यकता होती है, क्योंकि पानी एक कमजोर इलेक्ट्रोलाइट है;
बी) कोई प्रतिक्रिया उपोत्पाद जारी नहीं किया जाएगा, लेकिन कैथोड पर केवल तांबा।
7. उत्तीर्ण को समेकित करने के लिए कार्बन इलेक्ट्रोड के साथ जिंक क्लोराइड इलेक्ट्रोलिसिस का आरेख लिखें:
ZnCl 2 = Zn 2+ + 2Cl -,
कैथोड (-): Zn 2+ + 2 इ= जेडएन 0,
2एच 2 ओ + 2 इ= एच 2 + 2OH -,
एनोड (+): 2Cl - - 2 इ= सीएल 2.
इस मामले में, कुल प्रतिक्रिया समीकरण नहीं लिखा जा सकता है, क्योंकि यह ज्ञात नहीं है कि कुल बिजली का कितना हिस्सा पानी को पुनर्प्राप्त करने के लिए और कितना जस्ता आयनों को पुनर्प्राप्त करने के लिए उपयोग किया जाता है।
 |
डेमो प्रयोग लेआउट |
होम वर्क
1. अक्रिय इलेक्ट्रोड के साथ कॉपर (II) नाइट्रेट और सिल्वर नाइट्रेट के मिश्रण वाले विलयन के इलेक्ट्रोलिसिस का समीकरण लिखिए।
2. सोडियम हाइड्रॉक्साइड विलयन के विद्युत अपघटन का समीकरण लिखिए।
3. तांबे के सिक्के को साफ करने के लिए इसे बैटरी के नेगेटिव पोल से जुड़े तांबे के तार पर लटका दें और इसे 2.5% NaOH के घोल में डुबो दें, जहां बैटरी के पॉजिटिव पोल से जुड़ा ग्रेफाइट इलेक्ट्रोड भी डूब जाए। बताएं कि सिक्का कैसे साफ होता है। ( उत्तर... कैथोड पर, हाइड्रोजन आयनों को कम किया जा रहा है:
2एच + 2 इ= एच 2.
सिक्के की सतह पर हाइड्रोजन कॉपर ऑक्साइड के साथ प्रतिक्रिया करता है:
CuO + H 2 = Cu + H 2 O।
यह विधि पाउडर सफाई से बेहतर है क्योंकि सिक्का मिटता नहीं है।)
इलेक्ट्रोलिसिस क्या है? इस प्रश्न के उत्तर की सरल समझ के लिए, आइए किसी DC स्रोत की कल्पना करें। प्रत्येक डीसी शक्ति स्रोत के लिए, आप हमेशा एक सकारात्मक और नकारात्मक ध्रुव पा सकते हैं:
चलो दो रासायनिक प्रतिरोधी विद्युत प्रवाहकीय प्लेटों को इससे जोड़ते हैं, जिन्हें हम इलेक्ट्रोड कहेंगे। सकारात्मक ध्रुव से जुड़ी प्लेट को एनोड कहा जाता है, और नकारात्मक कैथोड को:
सोडियम क्लोराइड एक इलेक्ट्रोलाइट है; जब यह पिघलता है, तो यह सोडियम केशन और क्लोराइड आयनों में अलग हो जाता है:
NaCl = Na + + Cl -
जाहिर है, नकारात्मक चार्ज किए गए क्लोरीन आयन सकारात्मक चार्ज इलेक्ट्रोड - एनोड में जाएंगे, और सकारात्मक चार्ज ना + केशन नकारात्मक चार्ज इलेक्ट्रोड - कैथोड में जाएंगे। नतीजतन, Na + धनायन और Cl - आयनों दोनों का निर्वहन किया जाएगा, अर्थात वे तटस्थ परमाणु बन जाएंगे। Na + आयनों के मामले में इलेक्ट्रॉनों के अधिग्रहण और Cl - आयनों के मामले में इलेक्ट्रॉनों के नुकसान के माध्यम से निर्वहन होता है। अर्थात्, प्रक्रिया कैथोड पर होती है:
ना + + 1e - = ना 0,
और एनोड पर:
सीएल - - 1e - = क्ल
चूंकि प्रत्येक क्लोरीन परमाणु में एक अयुग्मित इलेक्ट्रॉन होता है, इसलिए उनका एकल अस्तित्व नुकसानदेह होता है और क्लोरीन परमाणु दो क्लोरीन परमाणुओं के अणु में संयोजित होते हैं:
l + ∙ सीएल = सीएल 2
इस प्रकार, कुल मिलाकर, एनोड पर होने वाली प्रक्रिया अधिक सही ढंग से निम्नानुसार लिखी गई है:
2Cl - - 2e - = Cl 2
यानी हमारे पास है:
कैथोड: ना + + 1e - = ना 0
एनोड: 2Cl - - 2e - = Cl 2
आइए इलेक्ट्रॉनिक बैलेंस का योग करें:
ना + + 1e - = ना 0 | 2
2Cl - - 2e - = Cl 2 | 1<
दोनों समीकरणों के बाएँ और दाएँ पक्षों को जोड़ें आधा प्रतिक्रियाओं, हम पाते हैं:
2Na + + 2e - + 2Cl - - 2e - = 2Na 0 + Cl 2
आइए हम दो इलेक्ट्रॉनों को उसी तरह से कम करें जैसे बीजगणित में किया जाता है, हमें इलेक्ट्रोलिसिस का आयनिक समीकरण प्राप्त होता है:
2NaCl (एल) => 2Na + Cl 2
ऊपर माना गया मामला सैद्धांतिक दृष्टिकोण से सबसे सरल है, क्योंकि सोडियम क्लोराइड पिघल में, सकारात्मक रूप से चार्ज किए गए आयनों में, केवल सोडियम आयन थे, और नकारात्मक वाले, केवल क्लोरीन आयन थे।
दूसरे शब्दों में, न तो Na + धनायन, और न ही Cl - आयनों में कैथोड और एनोड के लिए "प्रतियोगी" थे।
और, क्या होगा, उदाहरण के लिए, यदि सोडियम क्लोराइड को पिघलाने के बजाय, इसके जलीय घोल से करंट प्रवाहित किया जाता है? इस मामले में सोडियम क्लोराइड का वियोजन देखा जाता है, लेकिन जलीय घोल में धात्विक सोडियम का निर्माण असंभव हो जाता है। आखिरकार, हम जानते हैं कि क्षार धातुओं का प्रतिनिधि सोडियम एक अत्यंत सक्रिय धातु है जो पानी के साथ बहुत हिंसक प्रतिक्रिया करता है। यदि ऐसी परिस्थितियों में सोडियम को कम नहीं किया जा सकता है, तो कैथोड पर क्या कम हो जाएगा?
आइए पानी के अणु की संरचना को याद करें। यह एक द्विध्रुव है, अर्थात इसका एक ऋणात्मक और एक धनात्मक ध्रुव है:
यह इस संपत्ति के कारण है कि यह कैथोड सतह और एनोड सतह दोनों को "छड़ी" करने में सक्षम है:
इस मामले में, प्रक्रियाएं हो सकती हैं:
2H 2 O + 2e - = 2OH - + H 2
2H 2 O - 4e - = O 2 + 4H +
इस प्रकार, यह पता चला है कि यदि हम किसी इलेक्ट्रोलाइट के समाधान पर विचार करते हैं, तो हम देखेंगे कि इलेक्ट्रोलाइट के पृथक्करण के दौरान बनने वाले धनायन और आयन कैथोड पर कमी और एनोड पर ऑक्सीकरण के लिए पानी के अणुओं के साथ प्रतिस्पर्धा करते हैं।
तो कैथोड और एनोड पर कौन सी प्रक्रियाएँ होंगी? इलेक्ट्रोलाइट पृथक्करण या ऑक्सीकरण/पानी के अणुओं में कमी के दौरान बनने वाले आयनों का निर्वहन? या, शायद, ये सभी प्रक्रियाएं एक ही समय में होंगी?
इसके जलीय घोल के इलेक्ट्रोलिसिस के दौरान इलेक्ट्रोलाइट के प्रकार के आधार पर, कई तरह की स्थितियां संभव हैं। उदाहरण के लिए, क्षार, क्षारीय पृथ्वी धातु, एल्यूमीनियम और मैग्नीशियम के उद्धरण एक जलीय माध्यम में कम करने में सक्षम नहीं हैं, क्योंकि जब वे कम हो जाते हैं, तो क्रमशः क्षार, क्षारीय पृथ्वी धातु, एल्यूमीनियम या मैग्नीशियम प्राप्त किया जाना चाहिए, अर्थात। धातुएँ जो जल के साथ अभिक्रिया करती हैं।
इस मामले में, कैथोड पर केवल पानी के अणुओं की कमी संभव है।
आप निम्नलिखित सिद्धांतों का पालन करते हुए याद कर सकते हैं कि किसी भी इलेक्ट्रोलाइट के घोल के इलेक्ट्रोलिसिस के दौरान कैथोड पर कौन सी प्रक्रिया होगी:
1) यदि इलेक्ट्रोलाइट में एक धातु का धनायन होता है, जो सामान्य परिस्थितियों में मुक्त अवस्था में पानी के साथ प्रतिक्रिया करता है, तो प्रक्रिया कैथोड पर होती है:
2H 2 O + 2e - = 2OH - + H 2
यह अल समावेशी के लिए गतिविधि की सीमा की शुरुआत में धातुओं पर लागू होता है।
2) यदि इलेक्ट्रोलाइट में एक धातु का धनायन होता है, जो अपने मुक्त रूप में पानी के साथ प्रतिक्रिया नहीं करता है, लेकिन एसिड के साथ गैर-ऑक्सीडेंट के साथ प्रतिक्रिया करता है, तो दो प्रक्रियाएं एक साथ होती हैं, दोनों धातु के धनायनों और पानी के अणुओं की कमी:
मैं n + + ne = मैं 0
इन धातुओं में गतिविधि की श्रृंखला में अल और एच के बीच स्थित धातु शामिल हैं।
3) यदि इलेक्ट्रोलाइट में हाइड्रोजन केशन (एसिड) या धातु के धनायन होते हैं जो गैर-ऑक्सीकरण एजेंटों के साथ एसिड के साथ प्रतिक्रिया नहीं करते हैं, तो केवल इलेक्ट्रोलाइट केशन कम हो जाते हैं:
2Н + + 2е - = Н 2 - अम्ल के मामले में
Me n + + ne = Me 0 - नमक के मामले में
एनोड पर, इस बीच, स्थिति इस प्रकार है:
1) यदि इलेक्ट्रोलाइट में एनोक्सिक एसिड अवशेषों (एफ को छोड़कर) के आयन होते हैं, तो उनके ऑक्सीकरण की प्रक्रिया एनोड पर होती है, पानी के अणु ऑक्सीकृत नहीं होते हैं। उदाहरण के लिए:
2Сl - - 2e = Cl 2
एस 2- - 2ई = एस ओ
एनोड पर फ्लोराइड आयनों का ऑक्सीकरण नहीं होता है क्योंकि फ्लोरीन जलीय घोल में नहीं बन पाता है (पानी के साथ प्रतिक्रिया करता है)
2) यदि इलेक्ट्रोलाइट में हाइड्रॉक्साइड आयन (क्षार) होते हैं, तो वे पानी के अणुओं के बजाय ऑक्सीकृत हो जाते हैं:
4OH - - 4e - = 2H 2 O + O 2
3) यदि इलेक्ट्रोलाइट में ऑक्सीजन युक्त एसिड अवशेष (कार्बनिक एसिड अवशेषों को छोड़कर) या फ्लोराइड आयन (एफ -) होता है, तो पानी के अणुओं के ऑक्सीकरण की प्रक्रिया एनोड पर होती है:
2H 2 O - 4e - = O 2 + 4H +
4) एनोड पर एक कार्बोक्जिलिक एसिड के अम्लीय अवशेष के मामले में, प्रक्रिया आगे बढ़ती है:
2RCOO - - 2e - = R-R + 2CO 2
आइए विभिन्न स्थितियों के लिए इलेक्ट्रोलिसिस समीकरण लिखने का अभ्यास करें:
उदाहरण 1
जिंक क्लोराइड पिघलने के इलेक्ट्रोलिसिस के दौरान कैथोड और एनोड पर होने वाली प्रक्रियाओं के समीकरणों के साथ-साथ इलेक्ट्रोलिसिस के सामान्य समीकरण को भी लिखें।
समाधान
जब जिंक क्लोराइड पिघलता है, तो इसका पृथक्करण होता है:
ZnCl 2 = Zn 2+ + 2Cl -
इसके बाद, आपको इस तथ्य पर ध्यान देना चाहिए कि यह जस्ता क्लोराइड पिघला हुआ है जो इलेक्ट्रोलिसिस से गुजरता है, न कि जलीय घोल। दूसरे शब्दों में, विकल्पों के बिना, कैथोड पर केवल जिंक केशन की कमी हो सकती है, और एनोड पर क्लोराइड आयनों का ऑक्सीकरण हो सकता है। पानी के अणु नहीं:
कैथोड: Zn 2+ + 2e - = Zn 0 | 1
एनोड: 2Cl - - 2e - = Cl 2 | ∙ 1
ZnCl 2 = Zn + Cl 2
उदाहरण संख्या 2
जिंक क्लोराइड के जलीय घोल के इलेक्ट्रोलिसिस के दौरान कैथोड और एनोड पर होने वाली प्रक्रियाओं के समीकरणों के साथ-साथ इलेक्ट्रोलिसिस के सामान्य समीकरण को भी लिखें।
चूंकि इस मामले में, एक जलीय घोल इलेक्ट्रोलिसिस के अधीन होता है, इसलिए, सैद्धांतिक रूप से, पानी के अणु इलेक्ट्रोलिसिस में भाग ले सकते हैं। चूंकि जिंक अल और एच के बीच गतिविधि की रेखा में स्थित है, इसका मतलब है कि कैथोड पर जिंक केशन और पानी के अणु दोनों कम हो जाएंगे।
2H 2 O + 2e - = 2OH - + H 2
Zn 2+ + 2e - = Zn 0
क्लोराइड आयन एनोक्सिक एसिड एचसीएल का एक अम्लीय अवशेष है, इसलिए, एनोड पर ऑक्सीकरण के लिए प्रतिस्पर्धा में, क्लोराइड आयन पानी के अणुओं पर "जीत" करते हैं:
2Cl - - 2e - = Cl 2
इस विशेष मामले में, इलेक्ट्रोलिसिस के समग्र समीकरण को लिखना असंभव है, क्योंकि कैथोड पर जारी हाइड्रोजन और जस्ता के बीच का अनुपात अज्ञात है।
उदाहरण संख्या 3
कॉपर नाइट्रेट के जलीय घोल के इलेक्ट्रोलिसिस के दौरान कैथोड और एनोड पर होने वाली प्रक्रियाओं के समीकरणों के साथ-साथ इलेक्ट्रोलिसिस के सामान्य समीकरण को भी लिखें।
विलयन में कॉपर नाइट्रेट वियोजित अवस्था में होता है:
घन (नं 3) 2 = घन 2+ + 2नहीं 3 -
कॉपर हाइड्रोजन के दायीं ओर गतिविधि की पंक्ति में है, अर्थात कैथोड पर तांबे के धनायन कम हो जाएंगे:
घन 2+ + 2e - = घन 0
नाइट्रेट आयन नंबर 3 - एक ऑक्सीजन युक्त एसिड अवशेष है, जिसका अर्थ है कि नाइट्रेट आयन एनोड पर ऑक्सीकरण में पानी के अणुओं के साथ प्रतिस्पर्धा में "हार" जाते हैं:
2H 2 O - 4e - = O 2 + 4H +
इस प्रकार:
कैथोड: Cu 2+ + 2e - = Cu 0 | ∙ 2
2Cu 2+ + 2H 2 O = 2Cu 0 + O 2 + 4H +
परिणामी समीकरण इलेक्ट्रोलिसिस का आयनिक समीकरण है। इलेक्ट्रोलिसिस का पूरा आणविक समीकरण प्राप्त करने के लिए, आपको परिणामी आयनिक समीकरण के बाईं और दाईं ओर 4 नाइट्रेट आयनों को काउंटरों के रूप में जोड़ना होगा। तब हमें मिलता है:
2Cu (NO 3) 2 + 2H 2 O = 2Cu 0 + O 2 + 4HNO 3
उदाहरण संख्या 4
पोटेशियम एसीटेट के जलीय घोल के इलेक्ट्रोलिसिस के दौरान कैथोड और एनोड पर होने वाली प्रक्रियाओं के समीकरणों के साथ-साथ इलेक्ट्रोलिसिस के सामान्य समीकरण को भी लिखें।
समाधान:
जलीय घोल में पोटेशियम एसीटेट पोटेशियम केशन और एसीटेट आयनों में अलग हो जाता है:
सीएच 3 कुक = सीएच 3 सीओओ - + के +
पोटेशियम एक क्षार धातु है, अर्थात। बहुत शुरुआत में विद्युत रासायनिक वोल्टेज की श्रृंखला में है। इसका अर्थ है कि इसके धनायन कैथोड पर विसर्जित होने में सक्षम नहीं हैं। इसके बजाय, पानी के अणुओं को बहाल किया जाएगा:
2H 2 O + 2e - = 2OH - + H 2
जैसा कि ऊपर उल्लेख किया गया है, कार्बोक्जिलिक एसिड के अम्लीय अवशेष एनोड पर पानी के अणुओं से ऑक्सीकरण की प्रतियोगिता में "जीतते हैं":
2СН 3 - - 2e - = CH 3 −CH 3 + 2CO 2
इस प्रकार, इलेक्ट्रॉनिक संतुलन का योग और कैथोड और एनोड पर अर्ध-प्रतिक्रियाओं के दो समीकरणों को जोड़ने पर, हम प्राप्त करते हैं:
कैथोड: 2H 2 O + 2e - = 2OH - + H 2 | ∙ 1
एनोड: 2СН 3 - - 2e - = CH 3 -CH 3 + 2CO 2 | ∙ 1
2H 2 O + 2СН 3 СОО - = 2OH - + Н 2 + CH 3 -CH 3 + 2CO 2
हमने इलेक्ट्रोलिसिस का पूरा समीकरण आयनिक रूप में प्राप्त किया है। समीकरण के बाएँ और दाएँ पक्षों में दो पोटेशियम आयनों को जोड़ने और उन्हें काउंटरों के साथ जोड़ने पर, हमें आणविक रूप में पूर्ण इलेक्ट्रोलिसिस समीकरण मिलता है:
2H 2 O + 2СН 3 СООK = 2KOH + Н 2 + CH 3 -CH 3 + 2CO 2
उदाहरण संख्या 5
सल्फ्यूरिक एसिड के जलीय घोल के इलेक्ट्रोलिसिस के दौरान कैथोड और एनोड पर होने वाली प्रक्रियाओं के समीकरणों के साथ-साथ इलेक्ट्रोलिसिस के सामान्य समीकरण को भी लिखें।
सल्फ्यूरिक एसिड हाइड्रोजन केशन और सल्फेट आयनों में अलग हो जाता है:
एच 2 एसओ 4 = 2 एच + + एसओ 4 2-
हाइड्रोजन केशन एच + की कमी कैथोड पर होगी, और एनोड पर पानी के अणुओं का ऑक्सीकरण होगा, क्योंकि सल्फेट आयन ऑक्सीजन युक्त एसिड अवशेष होते हैं:
कैथोड: 2H + + 2e - = H 2 | 2
एनोड: 2H 2 O - 4e - = O 2 + 4H + | ∙ 1
4H + + 2H 2 O = 2H 2 + O 2 + 4H +
समीकरण के बाएँ और दाएँ और बाएँ पक्षों में हाइड्रोजन आयनों को कम करने से, हम सल्फ्यूरिक एसिड के जलीय घोल के इलेक्ट्रोलिसिस के लिए समीकरण प्राप्त करते हैं:
2एच 2 ओ = 2 एच 2 + ओ 2
जैसा कि आप देख सकते हैं, सल्फ्यूरिक एसिड के जलीय घोल का इलेक्ट्रोलिसिस पानी के इलेक्ट्रोलिसिस में कम हो जाता है।
उदाहरण संख्या 6
सोडियम हाइड्रॉक्साइड के जलीय घोल के इलेक्ट्रोलिसिस के दौरान कैथोड और एनोड पर होने वाली प्रक्रियाओं के समीकरणों के साथ-साथ इलेक्ट्रोलिसिस के सामान्य समीकरण को भी लिखिए।
सोडियम हाइड्रॉक्साइड का पृथक्करण:
NaOH = Na + + OH -
कैथोड पर केवल पानी के अणु कम हो जाएंगे, क्योंकि सोडियम एक अत्यधिक सक्रिय धातु है, एनोड पर केवल हाइड्रॉक्साइड आयन:
कैथोड: 2H 2 O + 2e - = 2OH - + H 2 | 2
एनोड: 4OH - - 4e - = O 2 + 2H 2 O | 1
4H 2 O + 4OH - = 4OH - + 2H 2 + O 2 + 2H 2 O
आइए हम बाएं और दाएं और 4 हाइड्रॉक्साइड आयनों पर दो पानी के अणुओं को कम करें और इस निष्कर्ष पर पहुंचे कि, सल्फ्यूरिक एसिड के मामले में, सोडियम हाइड्रॉक्साइड के जलीय घोल का इलेक्ट्रोलिसिस पानी के इलेक्ट्रोलिसिस में कम हो जाता है।
जलीय घोलों के इलेक्ट्रोलिसिस पर विचार करते समय, यह ध्यान में रखना चाहिए कि इलेक्ट्रोलाइट आयनों के अलावा, किसी भी जलीय घोल में ऐसे आयन भी होते हैं जो पानी H + और OH - के पृथक्करण के उत्पाद होते हैं।
एक विद्युत क्षेत्र में, हाइड्रोजन आयन कैथोड में चले जाते हैं, और OH आयन एनोड में चले जाते हैं। इस प्रकार, कैथोड पर इलेक्ट्रोलाइट केशन और हाइड्रोजन केशन दोनों को डिस्चार्ज किया जा सकता है। इसी तरह, एनोड पर इलेक्ट्रोलाइट आयनों और हाइड्रॉक्साइड आयनों दोनों का निर्वहन हो सकता है। इसके अलावा, पानी के अणु विद्युत रासायनिक ऑक्सीकरण या कमी से भी गुजर सकते हैं।
इलेक्ट्रोलिसिस के दौरान इलेक्ट्रोड पर किस तरह की इलेक्ट्रोकेमिकल प्रक्रियाएं होंगी, यह मुख्य रूप से संबंधित इलेक्ट्रोकेमिकल सिस्टम के इलेक्ट्रोड क्षमता के सापेक्ष मूल्यों पर निर्भर करेगा। कई संभावित प्रक्रियाओं में से एक आगे बढ़ेगी, जिसका कार्यान्वयन न्यूनतम ऊर्जा खपत से जुड़ा है। इसका मतलब यह है कि उच्चतम इलेक्ट्रोड क्षमता वाले इलेक्ट्रोकेमिकल सिस्टम के ऑक्सीकृत रूपों को कैथोड पर कम किया जाएगा, और सबसे कम इलेक्ट्रोड क्षमता वाले सिस्टम के कम रूपों को एनोड पर ऑक्सीकृत किया जाएगा। सामान्य स्थिति में, वे परमाणु, अणु और आयन एनोड पर अधिक आसानी से ऑक्सीकृत हो जाते हैं, जिनकी क्षमता इन परिस्थितियों में सबसे कम होती है, जबकि वे आयन, अणु और परमाणु जिनकी क्षमता सबसे अधिक होती है, कैथोड पर अधिक आसानी से कम हो जाते हैं। . आइए हम लवणों के जलीय विलयनों के इलेक्ट्रोलिसिस के दौरान होने वाली कैथोडिक प्रक्रियाओं पर विचार करें। यहां हाइड्रोजन आयन कमी प्रक्रिया के इलेक्ट्रोड क्षमता के मूल्य को ध्यान में रखना आवश्यक है, जो हाइड्रोजन आयनों की एकाग्रता पर निर्भर करता है। हम हाइड्रोजन इलेक्ट्रोड के लिए इलेक्ट्रोड क्षमता के सामान्य समीकरण को जानते हैं (खंड 2.3)।
उदासीन विलयनों (pH = 7) के मामले में, हाइड्रोजन आयनों के अपचयन के लिए इलेक्ट्रोड विभव का मान है
|
φ = –0,059 . 7 = -0.41 वी. |
1) धातु के पिंजरों वाले नमक के घोल के इलेक्ट्रोलिसिस के दौरान, जिसकी इलेक्ट्रोड क्षमता -0.41 V से बहुत अधिक सकारात्मक होती है, कैथोड पर ऐसे इलेक्ट्रोलाइट के तटस्थ समाधान से धातु कम हो जाएगी। ऐसी धातुएं हाइड्रोजन के निकट तनावों की श्रृंखला में पाई जाती हैं (लगभग टिन से और उसके बाद);
2) धातु के पिंजरों वाले नमक के घोल के इलेक्ट्रोलिसिस के दौरान, जिसकी इलेक्ट्रोड क्षमता - 0.41 V से बहुत अधिक नकारात्मक है, कैथोड पर धातु कम नहीं होगी, लेकिन हाइड्रोजन जारी किया जाएगा। ऐसी धातुओं में लगभग टाइटेनियम तक क्षार, क्षारीय पृथ्वी, मैग्नीशियम, एल्यूमीनियम शामिल हैं;
(वर्तमान घनत्व, तापमान, समाधान संरचना), धातु में कमी और हाइड्रोजन विकास दोनों संभव हैं; कभी-कभी धातु और हाइड्रोजन का संयुक्त विकास होता है।
अम्लीय विलयनों से हाइड्रोजन का विद्युत-रासायनिक विकास हाइड्रोजन आयनों के निस्सरण के कारण होता है:
2 एच + 2ē → 2H 0
2 एच 0 = एच 2 .
तटस्थ या क्षारीय मीडिया के मामले में, हाइड्रोजन का विकास पानी की विद्युत रासायनिक कमी के परिणामस्वरूप होता है:
गैर + ē → एन 0 + ओह –
एन 0 + एच 0 = एच 2 ,
|
फिर 2HON + 2ē → एच 2 + 2OH – |
इस प्रकार, जलीय विलयनों के इलेक्ट्रोलिसिस में कैथोडिक प्रक्रिया की प्रकृति मुख्य रूप से धातुओं के मानक इलेक्ट्रोड क्षमता की श्रृंखला में संबंधित धातु की स्थिति से निर्धारित होती है।
यदि विभिन्न धातुओं के धनायनों वाले एक जलीय घोल को इलेक्ट्रोलिसिस के अधीन किया जाता है, तो कैथोड पर उनकी रिहाई, एक नियम के रूप में, धातु इलेक्ट्रोड क्षमता के बीजीय मूल्य को कम करने के क्रम में आगे बढ़ेगी। उदाहरण के लिए, इलेक्ट्रोलाइज़र के टर्मिनलों पर पर्याप्त वोल्टेज के साथ एजी +, क्यू 2+ और जेडएन 2+ के मिश्रण से, चांदी के उद्धरण (φ 0 = +0.8 वी), फिर तांबे के उद्धरण (φ 0 = +0.34 वी) ) और अंत में, जस्ता (φ 0 = -0.76 वी)।
धनायनों के मिश्रण से धातुओं के विद्युत रासायनिक पृथक्करण का उपयोग इंजीनियरिंग और मात्रात्मक विश्लेषण में किया जाता है। सामान्य तौर पर, धातु आयनों के निर्वहन (इलेक्ट्रॉनों को जोड़ने) की क्षमता मानक इलेक्ट्रोड क्षमता की श्रृंखला में धातुओं की स्थिति से निर्धारित होती है। वोल्टेज की श्रृंखला में धातु जितनी बाईं ओर खड़ी होती है, उसकी नकारात्मक क्षमता उतनी ही अधिक होती है या सकारात्मक क्षमता कम होती है, उसके आयनों का निर्वहन उतना ही कठिन होता है। तो, वोल्टेज की एक श्रृंखला में खड़े धातु आयनों से, त्रिसंयोजक सोने के आयनों को सबसे आसानी से (सबसे कम विद्युत प्रवाह वोल्टेज पर), फिर चांदी के आयनों, आदि को छुट्टी दे दी जाती है। पोटेशियम आयनों को सबसे मुश्किल से डिस्चार्ज किया जाता है (विद्युत प्रवाह के उच्चतम वोल्टेज पर)। लेकिन धातु की क्षमता का परिमाण, जैसा कि ज्ञात है, समाधान में इसके आयनों की एकाग्रता के आधार पर बदलता है; इसी तरह, प्रत्येक धातु के आयनों के निर्वहन में आसानी उनकी एकाग्रता के आधार पर बदलती है: एकाग्रता में वृद्धि से आयनों के निर्वहन की सुविधा होती है, जबकि कमी से यह मुश्किल हो जाता है। इसलिए, कई धातुओं के आयनों वाले समाधान के इलेक्ट्रोलिसिस में, यह हो सकता है कि अधिक सक्रिय धातु की रिहाई कम सक्रिय धातु की रिहाई से पहले होगी (यदि पहली धातु के आयन की एकाग्रता महत्वपूर्ण है, और दूसरा बहुत कम है)।
आइए हम लवणों के जलीय विलयनों के इलेक्ट्रोलिसिस के दौरान होने वाली एनोडिक प्रक्रियाओं पर विचार करें। एनोड पर होने वाली प्रतिक्रियाओं की प्रकृति पानी के अणुओं की उपस्थिति और उस पदार्थ पर निर्भर करती है जिससे एनोड बनता है। यह ध्यान में रखा जाना चाहिए कि इलेक्ट्रोलिसिस के दौरान एनोड सामग्री ऑक्सीकरण कर सकती है। इस संबंध में, एक निष्क्रिय (अघुलनशील) एनोड के साथ इलेक्ट्रोलिसिस और एक सक्रिय (घुलनशील) एनोड के साथ इलेक्ट्रोलिसिस के बीच अंतर किया जाता है। अघुलनशील एनोड कोयले, ग्रेफाइट, प्लेटिनम, इरिडियम से बनाए जाते हैं; घुलनशील एनोड - तांबा, चांदी, जस्ता, कैडमियम, निकल और अन्य धातुओं से। अघुलनशील एनोड पर, इलेक्ट्रोलिसिस के दौरान आयनों या पानी के अणुओं का ऑक्सीकरण होता है। एनोक्सिक एसिड HI, HBr, HCl, H 2 S और उनके लवण (HF और फ्लोराइड को छोड़कर) के जलीय घोल के इलेक्ट्रोलिसिस के दौरान, आयनों को एनोड पर छुट्टी दे दी जाती है और संबंधित हैलोजन जारी किया जाता है। ध्यान दें कि एचसीएल और उसके लवणों के इलेक्ट्रोलिसिस के दौरान क्लोरीन की रिहाई सिस्टम की पारस्परिक स्थिति का खंडन करती है
2Cl – - 2ē →NS 2 (φ 0 = +1.36 वी)
2 एच 2 हे- 4ē →हे 2 + 4 एच + (φ 0 = +1.23 वी)
मानक इलेक्ट्रोड क्षमता की एक श्रृंखला में। यह विसंगति इन दो इलेक्ट्रोड प्रक्रियाओं में से दूसरे के एक महत्वपूर्ण ओवरवॉल्टेज से जुड़ी है - एनोड सामग्री का ऑक्सीजन विकास प्रक्रिया पर एक अवरोधक प्रभाव पड़ता है।
आयनों SO 4 2-, SO 3 2-, NO 3 -, PO 4 3-, आदि के साथ-साथ हाइड्रोजन फ्लोराइड और फ्लोराइड युक्त लवण के जलीय घोल के इलेक्ट्रोलिसिस के दौरान, पानी का विद्युत रासायनिक ऑक्सीकरण होता है। समाधान के पीएच के आधार पर, यह प्रक्रिया अलग-अलग तरीकों से आगे बढ़ती है और विभिन्न समीकरणों द्वारा लिखी जा सकती है। क्षारीय माध्यम में, समीकरण का रूप होता है
4ओएच – - 4ē → 2H 2 ओ + ओ 2 , (पीएच> 7)
और अम्लीय या तटस्थ मीडिया में हमारे पास है
Höh- 2ē →हे 0 + 2 एच + (पीएच 7)
2 हे 0 = हे 2 ,
|
फिर 2 एच 2 - 4ē → 4Н + + 2O 2 . |
विचाराधीन मामलों में, पानी का विद्युत रासायनिक ऑक्सीकरण ऊर्जावान रूप से सबसे लाभप्रद प्रक्रिया है। ऑक्सीजन युक्त आयनों का ऑक्सीकरण बहुत अधिक क्षमता पर होता है। उदाहरण के लिए, SO 4 2- - 2ē → S 2 O 8 2- आयन की मानक ऑक्सीकरण क्षमता 2.01 V है, जो 1.228 V के मानक जल ऑक्सीकरण क्षमता से काफी अधिक है।
2 एच 2 - 4ē → 2 + 4H + (φ 0 = 1.228 वी).
एफ-आयन का मानक ऑक्सीकरण क्षमता और भी महत्वपूर्ण है
2F – - 2ē →एफ 2 (φ 0 = 2 ,87 वी).
सामान्य तौर पर, लवण के जलीय घोलों के इलेक्ट्रोलिसिस के दौरान, धातु और हाइड्रोजन केशन एक साथ इलेक्ट्रोलाइज़र के कैथोड के पास आ रहे हैं, और उनमें से प्रत्येक कैथोड से आने वाले इलेक्ट्रॉनों द्वारा कम होने का "दावा" करता है। कैथोड पर कमी की प्रक्रिया वास्तव में कैसे आगे बढ़ेगी? उत्तर कई धातु तनावों से प्राप्त किया जा सकता है। इस मामले में, धातु के मानक इलेक्ट्रोड क्षमता का बीजगणितीय मूल्य जितना कम होगा, इलेक्ट्रॉन स्वीकर्ता उतने ही कमजोर होंगे और कैथोड पर उन्हें पुनर्स्थापित करना उतना ही कठिन होगा। इस संबंध में, विद्युत अपचयन के संबंध के अनुसार धनायनों के तीन समूहों को प्रतिष्ठित किया जाता है।
1. उच्च इलेक्ट्रॉन-निकासी गतिविधि (Cu 2+, Hg 2+, Ag +, Au 3+, Pt 2+, Pt 4+) द्वारा विशेषता वाले धनायन। इन धनायनों के लवणों के इलेक्ट्रोलिसिस के दौरान, धातु के धनायनों की लगभग पूर्ण कमी होती है; वर्तमान आउटपुट 100% या इसके करीब।
2. इलेक्ट्रॉन-निकासी क्षमता (एमएन 2+, जेडएन 2+, सीआर 3+, फे 2+, नी 2+, एसएन 2+, पीबी 2+) के औसत मूल्यों की विशेषता वाले उद्धरण। इलेक्ट्रोलिसिस के दौरान, धातु और पानी के अणुओं दोनों के धनायन एक साथ कैथोड पर कम हो जाते हैं, जिससे धातु की वर्तमान दक्षता में कमी आती है।
3. कम इलेक्ट्रॉन-निकासी क्षमता प्रदर्शित करने वाले धनायन (K +, Ca 2+, Mg 2+, Al 3+)। इस मामले में, कैथोड पर इलेक्ट्रॉन स्वीकर्ता माने गए समूह के धनायन नहीं हैं, बल्कि पानी के अणु हैं। इस मामले में, जलीय घोल में धनायन स्वयं अपरिवर्तित रहते हैं, और वर्तमान दक्षता शून्य के करीब पहुंच जाती है।
एनोड पर इलेक्ट्रोऑक्सीडेशन के लिए विभिन्न आयनों का अनुपात
एनोक्सिक एसिड और उनके लवण (Cl , Br ¯, J ¯, S 2-, CN¯, आदि) के आयन अपने इलेक्ट्रॉनों को पानी के अणु से कमजोर बनाए रखते हैं। इसलिए, इन आयनों वाले यौगिकों के जलीय समाधानों के इलेक्ट्रोलिसिस के दौरान, बाद वाले इलेक्ट्रॉन दाताओं की भूमिका निभाएंगे, वे अपने इलेक्ट्रॉनों को इलेक्ट्रोलाइज़र के बाहरी सर्किट में ऑक्सीकरण और स्थानांतरित करेंगे।
ऑक्सीजन एसिड आयन (NO 3 , SO 4 2-, PO 4 3-, आदि) पानी के अणुओं की तुलना में अपने इलेक्ट्रॉनों को अधिक मजबूती से धारण करने में सक्षम होते हैं। इस मामले में, पानी एनोड पर ऑक्सीकृत हो जाता है, जबकि आयन स्वयं अपरिवर्तित रहते हैं।
घुलनशील एनोड के मामले में, ऑक्सीडेटिव प्रक्रियाओं की संख्या बढ़कर तीन हो जाती है:
1) ऑक्सीजन के विकास के साथ पानी का विद्युत रासायनिक ऑक्सीकरण; 2) आयनों का निर्वहन (यानी इसका ऑक्सीकरण); 3) एनोड धातु का विद्युत रासायनिक ऑक्सीकरण (धातु का एनोडिक विघटन)।
संभावित प्रक्रियाओं में से, जो ऊर्जावान रूप से सबसे अधिक लाभकारी होगा, वह होगा। यदि एनोड धातु अन्य दोनों विद्युत रासायनिक प्रणालियों से पहले मानक क्षमता की श्रृंखला में स्थित है, तो धातु का एनोडिक विघटन देखा जाएगा। अन्यथा, ऑक्सीजन का विकास या आयनों का निर्वहन होगा। आयनों के निर्वहन के लिए कोई करीबी क्रम स्थापित नहीं किया गया है। इलेक्ट्रॉनों को दान करने की क्षमता को कम करके, सबसे आम आयनों को निम्नानुसार व्यवस्थित किया जाता है: S 2-, J , Br ¯, Cl , OH¯, H 2 O, SO 4 2-, NO 3 , CO 3 2- , पीओ 4 3- ...
आइए जलीय विलयनों के इलेक्ट्रोलिसिस के कई विशिष्ट मामलों पर विचार करें।
अघुलनशील एनोड के साथ CuCl 2 समाधान का इलेक्ट्रोलिसिस
वोल्टेज की श्रृंखला में, तांबा हाइड्रोजन के बाद स्थित होता है, इसलिए, Cu 2+ को कैथोड पर डिस्चार्ज किया जाएगा और धातु कॉपर को छोड़ा जाएगा, और एनोड पर क्लोराइड आयनों को आणविक क्लोरीन Cl 2 में ऑक्सीकृत किया जाएगा।
|
कैथोड (-) |
|
|
घन 2+ + 2ē → Cu 0 |
|
|
2Cl – - 2ē → क्ल 2 |
घन 2+ + 2 NS – → घन 0 + क्ल 2
CuCl 2 → घन 0 + क्ल 2
धातु वर्तमान उत्पादन (95-100%)।
NaNO 3 समाधान का इलेक्ट्रोलिसिस
चूंकि वोल्टेज की श्रृंखला में सोडियम हाइड्रोजन की तुलना में बहुत पहले होता है, इसलिए कैथोड पर पानी छोड़ा जाएगा। एनोड पर भी पानी छोड़ा जाएगा।
|
कैथोड (-) |
|
2 एच 2 हे+ 2ē →एच 2 + 2 ओह – |
|
2 एच 2 ओ - 4ē → 4H + + ओ 2 . |
इस प्रकार, कैथोड पर हाइड्रोजन मुक्त होता है और एक क्षारीय माध्यम बनाया जाता है, एनोड पर ऑक्सीजन छोड़ा जाता है और एनोड के पास एक अम्लीय माध्यम बनाया जाता है। यदि एनोड और कैथोड रिक्त स्थान एक दूसरे से अलग नहीं होते हैं, तो इसके सभी भागों में विलयन विद्युत रूप से तटस्थ रहेगा।
|
कैथोड (-) |
|
|
2 एच 2 हे+ 2ē →एच 2 + 2 ओह – |
|
|
2 एच 2 ओ - 4ē → 4H + + ओ 2 . |
6 2 हे → 2H 2 + 4ओएच – + 4H + + ओ 2
6 2 हे → 2H 2 + ओ 2 + 4H 2 हे
2 एच 2 हे → 2 एच 2 + हे 2
धातु का वर्तमान उत्पादन शून्य है।
नतीजतन, NaNO3 समाधान के इलेक्ट्रोलिसिस के दौरान, पानी का इलेक्ट्रोलिसिस होगा। NaNO 3 नमक की भूमिका विलयन की विद्युत चालकता को बढ़ाना है।
FeSO4 समाधान का इलेक्ट्रोलिसिस
कैथोड प्रतिक्रियाएं (-) (वसूली):
|
ए) फ़े 2+ + 2ē → फे 0 |
एक साथ प्रतिक्रियाएं |
|
बी) 2 एच 2 हे+ 2ē →एच 2 + 2 ओह – . |
एनोड (+) (ऑक्सीकरण) पर प्रतिक्रिया:
2 एच 2 ओ - 4ē → 4H + + ओ 2 .
धातु का वर्तमान उत्पादन औसत है।
अघुलनशील एनोड के साथ केजे समाधान का इलेक्ट्रोलिसिस
|
कैथोड (-) |
|
|
2 एच 2 हे+ 2ē →एच 2 + 2 ओह – |
|
|
2जे – - 2ē → जे 2 |
2 एच 2 हे + 2जे – → एच 2 + 2 ओह – + जू 2 .
केजे समाधान की इलेक्ट्रोलिसिस प्रतिक्रिया का अंतिम समीकरण:
2KJ + 2H 2 ओ → एच 2 + जू 2 + 2KOH.
कॉपर (घुलनशील) एनोड के साथ CuSO4 विलयन का इलेक्ट्रोलिसिस।
तांबे की मानक क्षमता +0.337 वी है, जो -0.41 वी से काफी अधिक है; इसलिए, CuSO 4 विलयन के इलेक्ट्रोलिसिस के दौरान, Cu 2+ आयनों का निर्वहन कैथोड पर होता है और धातु तांबा निकलता है। एनोड पर, विपरीत प्रक्रिया होती है - धातु ऑक्सीकरण, क्योंकि तांबे की क्षमता पानी की ऑक्सीकरण क्षमता (+1.228 वी) से बहुत कम है, और इससे भी ज्यादा - एसओ 4 2- आयन (+) की ऑक्सीकरण क्षमता 2.01 वी)। नतीजतन, इस मामले में, इलेक्ट्रोलिसिस एनोड के धातु (तांबे) के विघटन और कैथोड पर इसकी रिहाई के लिए कम हो जाता है।
कॉपर सल्फेट घोल के लिए इलेक्ट्रोलिसिस योजना:
|
कैथोड (-) |
|
घन 2+ + 2ē → Cu 0 |
|
घन 0 - 2ē → Cu 2+ . |
इस प्रक्रिया का उपयोग धातुओं के विद्युत शोधन (तथाकथित इलेक्ट्रोलाइटिक शोधन) के लिए किया जाता है।
क्लोरीनीकरण
सोडियम हाइपोक्लोराइट (NaClO) का उपयोग कई हानिकारक सूक्ष्मजीवों को बेअसर करने की इसकी रासायनिक क्षमता के कारण होता है। इसके जीवाणुनाशक गुणों का उद्देश्य कई खतरनाक कवक और बैक्टीरिया को नष्ट करना है।
सोडियम हाइपोक्लोराइट प्राप्त करने के लिए आणविक क्लोरीन (Cl) का उपयोग करके सोडियम हाइड्रॉक्साइड (NaOH) का क्लोरीनीकरण करना आवश्यक है।
सोडियम हाइपोक्लोराइट (NaClO) की क्रिया का सिद्धांत काफी सरल है, क्योंकि इस पदार्थ में उच्च जैव रासायनिक (बायोसाइड - हानिकारक या रोगजनक सूक्ष्मजीवों का मुकाबला करने के लिए डिज़ाइन किए गए रासायनिक एजेंट) गुण होते हैं। जब सोडियम हाइपोक्लोराइट (NaClO) पानी में प्रवेश करता है, तो यह सक्रिय रूप से विघटित होने लगता है, जिससे रेडिकल और ऑक्सीजन के रूप में सक्रिय कण बनते हैं। सोडियम हाइपोक्लोराइट (NaClO) रेडिकल हानिकारक सूक्ष्मजीवों के खिलाफ निर्देशित होते हैं। सोडियम हाइपोक्लोराइट (NaClO) के सक्रिय कण सूक्ष्मजीव की बाहरी झिल्ली या बायोफिल्म को नष्ट करना शुरू कर देते हैं, इस प्रकार, यह विभिन्न रोगजनक कवक, वायरस और बैक्टीरिया की अंतिम मृत्यु की ओर जाता है। सोडियम हाइपोक्लोराइट की रासायनिक संरचना का उद्देश्य पानी कीटाणुरहित और कीटाणुरहित करना है। . इसलिए, यह पदार्थ मानव जीवन के कई क्षेत्रों में एक महत्वपूर्ण स्थान रखता है। विश्व अध्ययनों से पता चलता है कि सोडियम हाइपोक्लोराइट (NaClO) का उपयोग 91% मामलों में कीटाणुशोधन के लिए किया जाता है, शेष 9% में पोटेशियम या लिथियम हाइपोक्लोराइट शामिल होता है। लेकिन इस पदार्थ के लिए दैनिक जीवन में परिणाम और लाभ देने के लिए, समाधान की एकाग्रता की सावधानीपूर्वक निगरानी करना आवश्यक है।
क्लोरीनीकरण पानी कीटाणुरहित करने का सबसे आसान और सस्ता तरीका निकला, इसलिए यह जल्दी से पूरी दुनिया में फैल गया। अब हम कह सकते हैं कि पीने के पानी को कीटाणुरहित करने का पारंपरिक तरीका, जिसे दुनिया भर में अपनाया गया है (100 में से 99 मामलों में), क्लोरीनीकरण है, और आज पानी को क्लोरीनेट करने के लिए सालाना सैकड़ों हजारों टन क्लोरीन की खपत होती है। उदाहरण के लिए, में रूस में, 99% से अधिक पानी क्लोरीनयुक्त है और इन उद्देश्यों के लिए औसतन सालाना लगभग 100 हजार टन क्लोरीन का उपयोग किया जाता है।
पीने के पानी को कीटाणुरहित करने की वर्तमान प्रथा में, क्लोरीनीकरण का उपयोग अक्सर किसी भी अन्य ज्ञात तरीकों की तुलना में सबसे किफायती और प्रभावी तरीके के रूप में किया जाता है, क्योंकि यह एकमात्र तरीका है जो वितरण नेटवर्क में किसी भी बिंदु पर पानी की सूक्ष्मजीवविज्ञानी सुरक्षा सुनिश्चित करता है। किसी भी समय क्लोरीन के प्रभाव के कारण।
यह सर्वविदित है कि क्लोरीन (Cl), पानी के साथ प्रतिक्रिया करके, "क्लोरीन पानी" (जैसा कि पहले सोचा गया था) नहीं बनाता है, लेकिन हाइपोक्लोरस एसिड ( एचसीएलओ) - रसायनज्ञों द्वारा प्राप्त पहला पदार्थ जिसमें सक्रिय क्लोरीन होता है।
प्रतिक्रिया समीकरण से: एचसीएलओ + एचसीएल ↔ सीएल 2 + एच 2 ओ,यह इस प्रकार है कि सैद्धांतिक रूप से नेट के 52.5 ग्राम से एचसीएलओआप 71 ग्राम प्राप्त कर सकते हैं सीएल 2यानी हाइपोक्लोरस एसिड में 135.2% सक्रिय क्लोरीन होता है। लेकिन यह एसिड अस्थिर है: समाधान में इसकी अधिकतम संभव एकाग्रता 30% से अधिक नहीं है।
क्लोरीन पानी में आसानी से घुल जाता है, जिससे उसमें मौजूद सभी जीव मर जाते हैं। जैसा कि पाया गया, जलीय घोल में गैसीय क्लोरीन को पानी के साथ मिलाने पर संतुलन स्थापित होता है:
सीएल 2 + एच 2 ओ ↔ एचसीएलओ + एचसीएल
इसके अलावा, पृथक्करण होता है (वियोजन एक कण (अणु, कट्टरपंथी, आयन) का कई सरल कणों में क्षय होता है) गठित हाइपोक्लोरस एसिड एचओसीएल एच + + ओसीएल –
क्लोरीन के जलीय घोल में हाइपोक्लोरस एसिड की उपस्थिति और इसके पृथक्करण के परिणामस्वरूप होने वाले आयन ओएसएल -मजबूत जीवाणुनाशक गुण हैं (यह सूक्ष्मजीवों को नष्ट करने की क्षमता है)। उसी समय, यह पता चला कि मुक्त हाइपोक्लोरस एसिड हाइपोक्लोराइट आयनों की तुलना में लगभग 300 गुना अधिक सक्रिय है क्लो -... यह अद्वितीय क्षमता द्वारा समझाया गया है एचसीएलओअपनी झिल्लियों के माध्यम से बैक्टीरिया में प्रवेश करते हैं। इसके अलावा, जैसा कि हमने पहले ही संकेत दिया है, हाइपोक्लोरस एसिड प्रकाश में अपघटन के लिए अतिसंवेदनशील है:
2HClO → 2 1O 2 + 2HCl → О 2 + HCl
हाइड्रोक्लोरिक एसिड और परमाणु (एकल) ऑक्सीजन (एक मध्यवर्ती के रूप में) के गठन के साथ, जो सबसे मजबूत ऑक्सीकरण एजेंट है।
क्लोरीनीकरण प्रक्रिया।
जल उपचार संयंत्र में, विभिन्न क्षमताओं, छोटे और मध्यम आकार के सिलेंडरों के विशेष कंटेनरों में तरलीकृत अवस्था में क्लोरीन की आपूर्ति की जाती है। लेकिन गैसीय अवस्था में क्लोरीन का उपयोग पानी कीटाणुरहित करने के लिए किया जाता है। गैसीय क्लोरीन तरल क्लोरीन से कॉइल बाष्पीकरणकर्ताओं में वाष्पीकरण द्वारा प्राप्त किया जाता है, जो ऊर्ध्वाधर बेलनाकार उपकरण होते हैं जिनके अंदर कॉइल होते हैं, जिसके माध्यम से तरल क्लोरीन गुजरता है। पानी में प्राप्त गैसीय क्लोरीन की खुराक विशेष उपकरणों - वैक्यूम क्लोरीनेटर के माध्यम से की जाती है।
उपचारित पानी में क्लोरीन की शुरूआत के बाद, इसे पानी के साथ अच्छी तरह मिलाया जाना चाहिए और उपभोक्ता को पानी की आपूर्ति से पहले पानी के साथ इसके संपर्क की पर्याप्त अवधि (कम से कम 30 मिनट) होनी चाहिए। यह ध्यान दिया जाना चाहिए कि क्लोरीनीकरण से पहले पानी पहले से ही तैयार किया जाना चाहिए और, एक नियम के रूप में, क्लोरीनीकरण आमतौर पर साफ पानी के साफ पानी की टंकी में प्रवेश करने से पहले किया जाता है, जहां आवश्यक संपर्क समय सुनिश्चित किया जाता है।
पानी कीटाणुशोधन के लिए क्लोरीन गैस का उपयोग करने के मुख्य लाभ
हैं:
- पानी कीटाणुशोधन प्रक्रिया की कम लागत;
- क्लोरीनीकरण प्रक्रिया की सादगी;
- गैसीय क्लोरीन की उच्च कीटाणुशोधन क्षमता;
- क्लोरीन न केवल सूक्ष्मजीवों को प्रभावित करता है, बल्कि कार्बनिक और अकार्बनिक पदार्थों का ऑक्सीकरण भी करता है;
- क्लोरीन पानी के स्वाद और गंध को समाप्त करता है, इसका रंग, मैलापन में वृद्धि में योगदान नहीं करता है।
हालांकि, क्लोरीन खतरे के दूसरे वर्ग से संबंधित एक अत्यधिक सक्रिय जहरीला पदार्थ है। गैसीय क्लोरीन एक मजबूत ऑक्सीकरण एजेंट है, कई कार्बनिक पदार्थों के दहन का समर्थन करता है, और ज्वलनशील पदार्थों के संपर्क में आग खतरनाक है। क्लोरीन वातावरण में तारपीन, टाइटेनियम और धातु के पाउडर कमरे के तापमान पर अनायास प्रज्वलित हो सकते हैं। क्लोरीन हाइड्रोजन के साथ विस्फोटक मिश्रण बनाती है।
कई बार, क्लोरीनीकरण में सुरक्षा सुनिश्चित करने की लागत पानी के वास्तविक क्लोरीनीकरण की लागत से अधिक हो जाती है।
इस संबंध में, पानी के क्लोरीनीकरण में क्लोरीन एजेंट के रूप में सोडियम हाइपोक्लोराइट का उपयोग गैसीय क्लोरीन का एक अच्छा विकल्प है।
इलेक्ट्रोलीज़
सबसे सस्ता, सरल और सुरक्षित तरीका सोडियम क्लोराइड (NaCl) के जलीय घोल के इलेक्ट्रोलिसिस द्वारा सोडियम हाइपोक्लोराइट के कीटाणुनाशक घोल को प्राप्त करना और उसी उपकरण में क्षार के साथ इसकी बातचीत - एक इलेक्ट्रोलाइजर है। 
तस्वीरें इलेक्ट्रोलाइजर दिखाती हैं। सोडियम हाइपोक्लोराइट डोजिंग के लिए सेको डोजिंग पंप और NaCl ब्राइन पंप करने के लिए अर्गल हर्मेटिक पंप
तरल क्लोरीन का उपयोग करके क्लोरीनीकरण विधि के सभी लाभों को बरकरार रखते हुए, इलेक्ट्रोलाइटिक सोडियम हाइपोक्लोराइट के साथ कीटाणुशोधन विषाक्त गैस के परिवहन और भंडारण की मुख्य कठिनाइयों से बचा जाता है।
कम सांद्रता वाले सोडियम हाइपोक्लोराइट घोल के उपयोग से तरल क्लोरीन और अत्यधिक केंद्रित सोडियम हाइपोक्लोराइट घोल की तुलना में पानी कीटाणुशोधन की उत्पादन प्रक्रिया की सुरक्षा बढ़ जाती है।
सोडियम हाइपोक्लोराइट के उत्पादन के लिए कच्चा माल टेबल सॉल्ट है। चूंकि अभिकर्मक का उपयोग सीधे उत्पादन स्थल पर किया जाता है, इसलिए परिवहन की कोई आवश्यकता नहीं होती है।
सोडियम हाइपोक्लोराइट के उत्पादन की तकनीकी प्रक्रिया में निम्नलिखित ऑपरेशन शामिल हैं:
- सोडियम क्लोराइड का संतृप्त घोल तैयार करना।
- इलेक्ट्रोलिसिस द्वारा सोडियम हाइपोक्लोराइट प्राप्त करने की मुख्य प्रक्रिया।
सोडियम क्लोराइड घोल के इलेक्ट्रोलिसिस के दौरान, निम्नलिखित प्रतिक्रियाएँ होती हैं:
कैथोड पर: 2Na + + 2e → 2Na;
2Na + 2H2O → 2NaOH (सोडियम हाइड्रॉक्साइड) + H 2;
एनोड पर: 2Cl - - 2e → Cl 2;
Cl 2 + 2H 2 O → 2HClO (हाइपोक्लोरस अम्ल) + HCl।
समग्र प्रतिक्रिया के रूप में प्रतिनिधित्व किया जा सकता है:
NaCl + H 2 O → NaClO + H 2।
चूंकि क्लोराइट्स और क्लोरेट्स के बाद के गठन के साथ सोडियम हाइपोक्लोराइट का ऑक्सीकरण घटते तापमान के साथ धीमा हो जाता है, इलेक्ट्रोलिसिस काम कर रहे नमक समाधान (20-25 डिग्री सेल्सियस) के अपेक्षाकृत कम तापमान पर किया जाता है।
नमक को विशेष कंटेनरों में डाला जाता है - लोडिंग डिवाइस के माध्यम से संतृप्त। कम सांद्रता वाले सोडियम हाइपोक्लोराइट घोल के उत्पादन के लिए कच्चा माल उच्च श्रेणी का भोजन तालिका नमक या "अतिरिक्त" है। डाला गया पानी, नमक की परत से गुजरते हुए, सोडियम क्लोराइड का एक संतृप्त घोल बनाता है।
केंद्रित नमक के घोल को शुद्ध करने के लिए मोटे फिल्टर और बदले जाने योग्य पॉलीप्रोपाइलीन कार्ट्रिज फाइन फिल्टर का उपयोग 5 माइक्रोन के थ्रूपुट के साथ किया जाता है।
सोडियम क्लोराइड के संतृप्त घोल को मिक्सर में पंप किया जाता है, जहाँ इसे नल के पानी से काम की सांद्रता (SanPiN 2.1.4.1074-01 के अनुसार) और फिर इलेक्ट्रोलाइज़र में पतला किया जाता है।
इलेक्ट्रोलिसिस द्वारा सोडियम हाइपोक्लोराइट प्राप्त करने की मुख्य प्रक्रिया इलेक्ट्रोलिसिस बाथ और हीट एक्सचेंजर से युक्त प्रतिष्ठानों में की जाती है। हीट एक्सचेंजर्स में, इलेक्ट्रोलाइट को गर्मियों में (नल के पानी से) ठंडा किया जाता है, और सर्दियों में, काम कर रहे नमक के घोल को पहले से गरम किया जाता है।
इलेक्ट्रोलिसिस स्नान में, टाइटेनियम इलेक्ट्रोड रूथेनियम और इरिडियम डाइऑक्साइड के साथ लेपित होते हैं। इलेक्ट्रोलिसिस की प्रक्रिया में, कैल्शियम और मैग्नीशियम इलेक्ट्रोड पर जमा होते हैं, इसलिए, समय-समय पर, इन जमाओं के रूप में, कोशिकाओं को 4% हाइड्रोक्लोरिक एसिड (एचसीएल) समाधान के साथ एक बंद सर्किट में फ्लश किया जाता है।
इलेक्ट्रोलिसिस सेल में, काम कर रहे नमक के घोल का निरंतर इलेक्ट्रोलिसिस होता है, जिसके परिणामस्वरूप सोडियम हाइपोक्लोराइट प्राप्त होता है। 2.5 m3 / h के निरंतर आयतन प्रवाह के साथ 3% NaCl समाधान इलेक्ट्रोलिसिस इकाई के माध्यम से तब तक बहता है जब तक वांछित NaClO एकाग्रता (0.8%) तक नहीं पहुंच जाता है। इलेक्ट्रोलाइजर्स में बनने वाले सोडियम हाइपोक्लोराइट को उपचार सुविधाओं की जरूरतों के लिए आपूर्ति प्रदान करने के लिए विशेष टैंकों में संग्रहित किया जाता है।
सक्रिय क्लोरीन के संदर्भ में कम से कम 8 ग्राम / एल की एकाग्रता के साथ सोडियम हाइपोक्लोराइट भंडारण टैंक में प्रवेश करता है, जहां से इसे अभिकर्मक इंजेक्शन बिंदुओं के पास स्थित खुराक इकाइयों में पंप किया जाता है। टैंकों से, सोडियम हाइपोक्लोराइट की आपूर्ति पाइपलाइन प्रणाली के माध्यम से डोजिंग पंपों के माध्यम से एक स्वचालित डोजिंग स्टेशन को उपचारित पानी में की जाती है।
उत्पादन
सोडियम हाइपोक्लोराइट के कम-केंद्रित समाधानों के उपयोग से वाटरवर्क्स में जल शोधन के लिए तकनीकी प्रक्रियाओं की सुरक्षा बढ़ाना संभव हो जाता है।
शहर के जल आपूर्ति नेटवर्क (द्वितीय चरण) को खिलाए जाने से पहले पराबैंगनी विकिरण के साथ कम सांद्रता वाले सोडियम हाइपोक्लोराइट (प्रथम चरण) के साथ उपचारित पानी के कीटाणुशोधन का संयोजन वर्तमान मानकों के साथ सूक्ष्मजीवविज्ञानी संकेतकों के संदर्भ में पानी की गुणवत्ता के पूर्ण अनुपालन की गारंटी देता है। उच्च महामारी विज्ञान सुरक्षा।
इलेक्ट्रोलीज़
पिघला देता है और इलेक्ट्रोलाइट समाधान
इलेक्ट्रोलीज़ पारित होने के दौरान होने वाली रासायनिक प्रतिक्रियाओं का एक सेट कहा जाता है एकदिश धारा एक विद्युत रासायनिक प्रणाली के माध्यम से जिसमें दो इलेक्ट्रोड और एक पिघल या इलेक्ट्रोलाइट समाधान होता है।
इलेक्ट्रोलिसिस का रासायनिक सार यह है कि यह एक निरंतर विद्युत प्रवाह के प्रभाव में होने वाली एक रेडॉक्स प्रतिक्रिया है, और ऑक्सीकरण और कमी की प्रक्रियाएं स्थानिक रूप से अलग हो जाती हैं।
कैथोड - एक इलेक्ट्रोड जिस पर धनायन या पानी कम किया जाता है। यह नकारात्मक चार्ज है।
एनोड - एक इलेक्ट्रोड जिस पर आयनों या पानी का ऑक्सीकरण होता है। यह सकारात्मक रूप से चार्ज किया जाता है।
1. पिघले हुए लवणों, क्षारों का इलेक्ट्रोलिसिस।
पिघलने के इलेक्ट्रोलिसिस के दौरान, कैथोड पर धातु के धनायन हमेशा कम हो जाते हैं।
(-): еn + + nē → Me0
एनोडिक प्रक्रिया आयनों की संरचना द्वारा निर्धारित की जाती है:
a) यदि एनोक्सिक एसिड (Cl-, Br-, I-, S2-) का आयन, तो यह आयन एनोडिक ऑक्सीकरण से गुजरता है और एक साधारण पदार्थ बनता है:
ए (+): 2Cl - - 2ē → Cl2 या A (+): S2- - 2ē → S0
बी) यदि एक ऑक्सीजन युक्त आयन (SO42-, SiO32-, HO-, आदि) एनोडिक ऑक्सीकरण से गुजरता है, तो अधातु एक ऑक्साइड (अपनी ऑक्सीकरण अवस्था को बदले बिना) बनाती है और ऑक्सीजन निकलती है।
ए (+): 2SiO32-- 4ē → 2SiO2 + O2
ए (+): 2SO32-- 4ē → 2SO2 + O2
ए (+): 4PO43-- 12ē → 2P2O5 + 3O2
ए (+): 4NO3-- 4ē → 2N2O5 + О2
ए (+): 4HO-- 4ē → 2H2O + O2
उदाहरण 1.1. ZnCl2 नमक पिघला
ZnCl2 Zn2 + + 2Cl-
एस: ZnCl2 इलेक्ट्रोलिसिस Zn + Cl2
उदाहरण 1.2. NaOH क्षार पिघल
NaOH ना + + OH-
कुल इलेक्ट्रोलिसिस समीकरण समीकरणों के दाएं और बाएं पक्षों को जोड़कर प्राप्त किया जाता है, बशर्ते कि कैथोडिक और एनोडिक प्रक्रियाओं में भाग लेने वाले इलेक्ट्रॉन बराबर हों।
https://pandia.ru/text/80/299/images/image006_58.gif "चौड़ाई =" 70 "ऊंचाई =" 12 "> 4 Na + + 4 ē + 4 OH - - 4 इलेक्ट्रोलिसिस 4 Na0 + O2 + 2H2O
4 Na + + 4 OH - इलेक्ट्रोलिसिस 4 Na0 + O2 + 2H2O - आयनिक समीकरण
4NaOH इलेक्ट्रोलिसिस 4Na + 2H2O + O2 - आणविक समीकरण
उदाहरण 1.3। नमक पिघला हुआ Na2SO4
Na2SO4 Û 2Na + + SO42-
के (-): ना + + 1 नाव * 4
ए (+): 2SO42- - 4 O2 + 2SO3
4Na + + 2SO42- Þ 2Nao + O2 + 2SO3 - आयनिक इलेक्ट्रोलिसिस समीकरण
2Na2SO4 इलेक्ट्रोलिसिस 4Nao + O2 + 2SO3 - आणविक समीकरण
टू ए
उदाहरण 1.4. AgNO3 नमक पिघला
AgNO3 Ag + + NO3-
(-): एजी + + 1 पहले * 4
ए (+): 4NO3- - 4 ē Þ 2N2O5 + 2O2 * 1
4Ag + + 4NO3- इलेक्ट्रोलिसिस 4Ag + 2N2O5 + 2O2
4AgNO3 इलेक्ट्रोलिसिस 4Ag + 2N2O5 + 2O2
टू ए
स्व-अध्ययन कार्य ... निम्नलिखित लवणों के गलनांक के लिए इलेक्ट्रोलिसिस समीकरण बनाएं: AlCl3, Cr2 (SO4) 3, Na2SiO3, K2CO3।
2. लवण, हाइड्रॉक्साइड और अम्ल के विलयन का इलेक्ट्रोलिसिस।
जलीय विलयनों का इलेक्ट्रोलिसिस इस तथ्य से जटिल है कि पानी ऑक्सीकरण और कमी प्रक्रियाओं में भाग ले सकता है।
कैथोडिक प्रक्रियाएं नमक धनायन की विद्युत रासायनिक गतिविधि द्वारा निर्धारित किया जाता है। वोल्टेज श्रृंखला में धातु जितनी बाईं ओर होगी, कैथोड पर इसके उद्धरण उतने ही कठिन होंगे:
![]() ली
क
सीए
ना
मिलीग्राम
अली
एम.एन.
Zn
करोड़
ते
नी
एस.एन.
पंजाब
एच 2
घन
एचजी
एजी
पीटी
औ
ली
क
सीए
ना
मिलीग्राम
अली
एम.एन.
Zn
करोड़
ते
नी
एस.एन.
पंजाब
एच 2
घन
एचजी
एजी
पीटी
औ
मैं समूहद्वितीयसमूहतृतीयसमूह
अल (समूह I) तक और सहित धातु के पिंजरों के लिए, कैथोडिक प्रक्रिया पानी से हाइड्रोजन की कमी है:
(-) के: 2H2O + 2ē → H2 + 2HO-
हाइड्रोजन (समूह III) के बाद धातु के पिंजरों के लिए, कैथोडिक प्रक्रिया धातु में उनकी कमी है:
(-) : еn + + nē → Me0
Mn से H2 (समूह II) तक वोल्टेज की श्रृंखला में धातु के पिंजरों के लिए, पानी से धातु और हाइड्रोजन के धनायनों की कमी की समानांतर प्रतिस्पर्धी प्रक्रियाएं हैं:
(-) : еn + + nē → Me0
2H2O + 2ē → H2 + 2HO-
इनमें से कौन सी प्रक्रिया प्रबल होगी यह कई कारकों पर निर्भर करता है: मी गतिविधि, समाधान पीएच, नमक एकाग्रता, लागू वोल्टेज, और इलेक्ट्रोलिसिस की स्थिति।
एनोडिक प्रक्रियाएं नमक आयनों की संरचना द्वारा निर्धारित:
ए) यदि एनोक्सिक एसिड (Cl-, Br-, I-, S2-, आदि) का आयन, तो इसे सरल पदार्थों (F- के अपवाद के साथ) में ऑक्सीकृत किया जाता है:
ए (+): S2- - 2ē → S0
बी) ऑक्सीजन युक्त आयन (SO42-, CO32-, आदि, या OH-) की उपस्थिति में, केवल पानी एनोडिक ऑक्सीकरण से गुजरता है:
ए (+): 2H2O - 4ē → O2 + 4H +
आइए उन उदाहरणों पर विचार करें जो सभी संभावित विकल्पों को स्पष्ट करते हैं:
उदाहरण 2.1 ... KCl नमक घोल
(-): 2H2O + 2e - Þ H2 + 2OH-
ए (+): 2Cl - - 2e - Cl2
ई: 2H2O + 2Cl - इलेक्ट्रोलिसिस H2 + 2OH - + Cl2 - इलेक्ट्रोलिसिस का आयनिक समीकरण
2KCl + 2H2O इलेक्ट्रोलिसिस H2 + 2KOH + Cl2 - इलेक्ट्रोलिसिस का आणविक समीकरण
टू ए
उदाहरण 2.2 ... CuCl2 नमक का घोल
CuCl2 Cu2 + + 2Cl-
(-): Cu2 + + 2e - Cuo
ए (+): 2Cl- -2e - Cl2
ई: CuCl2 इलेक्ट्रोलिसिस Cu + Cl2
उदाहरण 2.3। FeCl2 नमक का घोल
FeCl2 Fe2 + + 2Cl-
लोहा समूह II की धातुओं से संबंधित है, इसलिए कैथोड पर दो समानांतर प्रक्रियाएं होंगी:
पहली प्रक्रिया:
(-) के: Fe2 + + 2ē → Fe0
(+) ए: 2Cl - - 2ē → Cl2
Fe2 + + 2Cl - el-s Fe0 + Cl2 - प्रक्रिया का आयनिक समीकरण
FeCl2 el-s Fe0 + Cl2 - प्रक्रिया का आणविक समीकरण
दूसरी प्रक्रिया:
(-) के: 2H2O + 2ē → H2 + 2OH-
(+) ए: 2Cl - - 2ē → Cl2
2Н2О + 2Cl - → Н2 + 2ОН - + Cl2 - प्रक्रिया का आयनिक समीकरण
2Н2О + FeCl2 इलेक्ट्रोलिसिस Н2 + Fe (ОН) 2 + Cl2 - आणविक समीकरण।
इस प्रकार, कैथोड स्पेस मेंइलेक्ट्रोलिसिस की स्थितियों के आधार पर Fe, H2 और Fe (OH) 2 अलग-अलग अनुपात में बनेंगे।
उदाहरण 2.4 ... Na2SO4 नमक का घोल।
Na2SO4 Û 2Na + + SO42-
के (-) 2H2O + 2e - Þ H2 + 2OH - * 2
ए (+) 2H2O - 4e - Þ O2 + 4H +
ई: 6H2O इलेक्ट्रोलिसिस 2H2 + 4OH - + O2 + 4H +
ई: 6H2O + 2Na2SO4 इलेक्ट्रोलिसिस 2H2 + 4 NaOH + O2 + 2H2SO4
एनोड स्पेस में कैथोड स्पेस में
जब विद्युत प्रवाह को बंद कर दिया जाता है और कैथोड और एनोड रिक्त स्थान की सामग्री को मिलाया जाता है, तो इलेक्ट्रोलिसिस के अंतिम परिणाम को आरेख द्वारा दर्शाया जा सकता है:
2H2O एल-एस 2H2 + O2,
चूँकि क्षार अम्ल के साथ क्रिया करके 2 mol नमक और 4 mol पानी बनाता है।
उदाहरण 2.5 ... CuSO4 समाधान का इलेक्ट्रोलिसिस।
CuSO4 Cu2 + + SO42-
के (-): Cu2 + + 2e - Þ Cuo
ए (+): 2H2O - 4e - Þ O2 + 4H +
ई: 2Cu2 + + 2H2O इलेक्ट्रोलिसिस 2Cuo + O2 + 4H +
ई: CuSO4 + 2H2O इलेक्ट्रोलिसिस 2Cuo + O2 + 2H2SO4
उदाहरण 2.6। FeSO4 समाधान का इलेक्ट्रोलिसिस
चूंकि लोहा धातुओं के II समूह से संबंधित है, इसलिए कैथोड पर समानांतर में दो प्रतिस्पर्धी प्रक्रियाएं होंगी (उदाहरण 2.3 देखें), और पानी एनोड पर ऑक्सीकृत हो जाएगा (उदाहरण 2.4 देखें):
पहली प्रक्रिया:
https://pandia.ru/text/80/299/images/image043_10.gif "चौड़ाई =" 41 "ऊंचाई =" 12 "> 2Fе2 + + 2Н2О el-З 2 Fe + O2 + 4H + - का आयनिक समीकरण प्रक्रिया
2FeSO4 + 2Н2О el-З 2 Fe + O2 + 2Н2SO4- आणविक समीकरण
दूसरी प्रक्रिया:
(+): 2Н2О + 2ē → Н2 + 2ОН - * 2
ए (-): 2H2O - 4ē → O2 + 4H +
6H2O इलेक्ट्रोलिसिस 2H2 + 4OH - + O2 + 4H +
6H2O + 2FeSO4 इलेक्ट्रोलिसिस 2H2 + 2Fe (OH) 2 + O2 + 2H2SO4 - आणविक
https://pandia.ru/text/80/299/images/image051_9.gif "चौड़ाई =" 21 "ऊंचाई =" 50 "> और केवल अगर पानी से धातु और हाइड्रोजन के कैथोडिक कमी की प्रक्रियाएं समान अनुपात में हैं , आप कुल अंतिम प्रतिक्रिया समीकरण लिख सकते हैं:
(-) के: Fe2 + + 2ē → Fe0
2H2O + 2ē → H2 + 2HO - केवल 4 इलेक्ट्रॉन
(+) ए: 2H2O - 4ē → O2 + 4H +
Fe2 + + 2H2O + 2H2O → Fe + H2 + 2HO - + O2 + 4H +
2FeSO4 + 4Н2О el-s Fe + Н2 + Fe (OH) 2 + O2 + 2Н2SO4
कैथोड एनोड
करंट को बंद करने और विलयनों को मिलाने के बाद, अंतिम समीकरण इस प्रकार होगा:
· समाधान K2CO3, ZnSO4, AgNO3, NiI2, CoCl2 के इलेक्ट्रोलिसिस के समीकरण बनाएं।
· कार्य को हल करने के लिए। तकनीकी NaOH में NaCl अशुद्धता की सामग्री का विश्लेषण करने के लिए, 40 ग्राम तैयारी को पानी में भंग कर दिया गया था और क्लोरीन आयनों के पूरी तरह से ऑक्सीकरण होने तक इलेक्ट्रोलिसिस के अधीन किया गया था। उसी समय, 200C के तापमान और सामान्य दबाव पर एनोड पर 601 मिली Cl2 छोड़ा गया। NaOH में NaCl अशुद्धता के द्रव्यमान अंश की गणना करें।
3. घुलनशील इलेक्ट्रोलिसिस एन एस एम एनोड
ऊपर, एक निष्क्रिय एनोड के साथ लवण के जलीय घोल के इलेक्ट्रोलिसिस के उदाहरणों पर विचार किया गया था, जो कि एनोड प्रक्रिया में भाग नहीं लेता है। ऐसे इलेक्ट्रोड निष्क्रिय उत्कृष्ट धातुओं से बने होते हैं, उदाहरण के लिए, Pt, Ir, या कार्बन इलेक्ट्रोड का उपयोग किया जाता है। यदि घुलनशील एनोड का उपयोग किया जाता है, उदाहरण के लिए, क्यू-एनोड, जेडएन-एनोड, तो एनोड प्रक्रिया को काफी संशोधित किया जाता है, क्योंकि एनोड स्वयं ऑक्सीकरण होता है। 2 प्रतिस्पर्धी के एनोड पर, कम क्षमता वाली एक प्रक्रिया चल रही है: तांबे के ऑक्सीकरण के लिए E0 = - 0.34 V, जिंक E0 के ऑक्सीकरण के लिए = - 0.76 V और Cl-आयन के ऑक्सीकरण के लिए E0 = + 1.36 वी.
उदाहरण 3.1। घुलनशील एनोड के साथ CuCl2 नमक के जलीय घोल का इलेक्ट्रोलिसिस:
कैथोड (-): Cu-एनोड (+):
u2 + + 2ē → Cu0 u0 - 2ē → Cu2 +
इस प्रकार, कॉपर एनोड का एक प्रकार का शोधन होता है: यह घुल जाता है, अशुद्धियाँ एनोड स्थान में रहती हैं, और शुद्ध तांबा कैथोड पर जमा हो जाता है। इस मामले में, क्लोरीन आयन ऑक्सीकरण नहीं होता है, लेकिन एनोड स्थान में जमा हो जाता है।
उदाहरण 3.2. Cu-एनोड के साथ KCl नमक के जलीय घोल का इलेक्ट्रोलिसिस:
Cu-एनोड (+): u0 - 2ē → Cu2 +
प्रारंभिक क्षण में, हाइड्रोजन कैथोड पर पानी से पुनर्प्राप्त करना शुरू कर देता है, लेकिन समाधान में Cu2 + की उपस्थिति दो कैथोडिक कमी प्रतिक्रियाओं को प्रतिस्पर्धी बनाती है:
के (-): 2H2O + 2ē → H2 + 2NO - E0 = - 0.828 V
Cu2 + + 2ē → Cu0 E0 = + 0.34 V
नतीजतन, जो एक उच्च संभावित आय की विशेषता है, मुख्य रूप से, यानी Cu2 + से Cu0 की कमी।
इस प्रकार, इस मामले में, Cu-एनोड का विघटन होगा: Cu0 - 2ē → Cu2 +, और कैथोड पर गठित तांबे के धनायन कम हो जाएंगे: Cu2 + + 2ē → Cu0। KCl नमक की आवश्यकता केवल विलयन की विद्युत चालकता को बढ़ाने के लिए होती है, और यह सीधे रेडॉक्स प्रक्रियाओं में भाग नहीं लेता है।
स्वतंत्र कार्य के लिए असाइनमेंट।एक Cu एनोड के साथ CuSO4 के इलेक्ट्रोलिसिस पर विचार करें, Na2SO4 एक Cu एनोड के साथ।