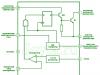
निर्धारित करें कि जमीनी अवस्था में श्रृंखला में दर्शाए गए तत्वों में से किस परमाणु में एक अयुग्मित इलेक्ट्रॉन होता है।
उत्तर क्षेत्र में चयनित तत्वों की संख्या लिखिए।
उत्तर:
उत्तर: 23
व्याख्या:
आइए प्रत्येक संकेतित रासायनिक तत्वों के लिए इलेक्ट्रॉनिक सूत्र लिखें और अंतिम इलेक्ट्रॉनिक स्तर का इलेक्ट्रॉन-ग्राफिक सूत्र बनाएं:
1) एस: 1एस 2 2एस 2 2पी 6 3एस 2 3पी 4
2) ना: 1s 2 2s 2 2p 6 3s 1
3) अल: 1s 2 2s 2 2p 6 3s 2 3p 1
4) सी: 1s 2 2s 2 2p 6 3s 2 3p 2
5) मिलीग्राम: 1s 2 2s 2 2p 6 3s 2
पंक्ति में दर्शाए गए रासायनिक तत्वों में से तीन धातु तत्वों का चयन करें। चयनित तत्वों को पुनर्स्थापनात्मक गुणों के आरोही क्रम में व्यवस्थित करें।
उत्तर क्षेत्र में चयनित तत्वों की संख्या को वांछित क्रम में लिखें।
उत्तर: 352
व्याख्या:
आवर्त सारणी के मुख्य उपसमूहों में, धातुएँ बोरॉन-एस्टेटिन विकर्ण के साथ-साथ द्वितीयक उपसमूहों में स्थित होती हैं। इस प्रकार, इस सूची की धातुओं में Na, Al और Mg शामिल हैं।
आवर्त में बायीं ओर तथा उपसमूह में नीचे की ओर जाने पर तत्वों के धात्विक और इसलिए अपचायक गुण बढ़ जाते हैं।
इस प्रकार, ऊपर सूचीबद्ध धातुओं के धात्विक गुण श्रृंखला Al, Mg, Na . में वृद्धि करते हैं
पंक्ति में इंगित तत्वों में से, दो तत्वों का चयन करें, जो ऑक्सीजन के संयोजन में +4 की ऑक्सीकरण अवस्था प्रदर्शित करते हैं।
उत्तर क्षेत्र में चयनित तत्वों की संख्या लिखिए।
उत्तर: 14
व्याख्या:
जटिल पदार्थों में प्रस्तुत सूची से तत्वों का मुख्य ऑक्सीकरण राज्य:
सल्फर - "-2", "+4" और "+6"
सोडियम ना - "+1" (एकल)
एल्यूमिनियम अल - "+3" (केवल एक)
सिलिकॉन सी - "-4", "+4"
मैग्नीशियम Mg - "+2" (एकल)
पदार्थों की प्रस्तावित सूची में से दो ऐसे पदार्थों का चयन कीजिए जिनमें एक आयनिक रासायनिक बंध मौजूद हो।
उत्तर: 12
व्याख्या:
अधिकांश मामलों में, एक यौगिक में एक आयनिक प्रकार के बंधन की उपस्थिति इस तथ्य से निर्धारित की जा सकती है कि इसकी संरचनात्मक इकाइयों में एक साथ एक विशिष्ट धातु और गैर-धातु परमाणुओं के परमाणु शामिल होते हैं।
इस मानदंड के आधार पर, आयनिक प्रकार का बंधन यौगिकों KCl और KNO 3 में होता है।
उपरोक्त विशेषता के अलावा, एक यौगिक में एक आयनिक बंधन की उपस्थिति कहा जा सकता है यदि इसकी संरचनात्मक इकाई में अमोनियम धनायन (NH) है 4 + ) या इसके कार्बनिक एनालॉग - एल्केलामोनियम केशन RNH 3 + , डायलकेलामोनियम आर 2NH2+ , ट्रायलकिलमोनियम आर 3एनएच+ और टेट्राएल्किलमोनियम R 4एन+ , जहां R कुछ हाइड्रोकार्बन मूलक है। उदाहरण के लिए, यौगिक में एक आयनिक प्रकार का बंधन होता है (CH .) 3 ) 4 धनायन के बीच NCl (CH .) 3) 4+ और क्लोराइड आयन Cl -।
किसी पदार्थ के सूत्र और उस वर्ग / समूह के बीच एक पत्राचार स्थापित करें जिससे यह पदार्थ संबंधित है: एक अक्षर द्वारा इंगित प्रत्येक स्थिति के लिए, एक संख्या द्वारा इंगित संबंधित स्थिति का चयन करें।
उत्तर: 241
व्याख्या:
एन 2 ओ 3 - गैर-धातु ऑक्साइड। N 2 O, NO, SiO और CO को छोड़कर सभी अधातु ऑक्साइड अम्लीय हैं।
अल 2 ओ 3 - ऑक्सीकरण अवस्था +3 में धातु ऑक्साइड। ऑक्सीकरण अवस्था में धातु ऑक्साइड +3, +4, साथ ही BeO, ZnO, SnO और PbO, उभयधर्मी हैं।
एचसीएलओ 4 एसिड का एक विशिष्ट प्रतिनिधि है, क्योंकि। एक जलीय घोल में वियोजन के दौरान, धनायनों से केवल H + धनायन बनते हैं:
एचसीएलओ 4 \u003d एच + + क्लो 4 -
पदार्थों की प्रस्तावित सूची से, दो पदार्थों का चयन करें, जिनमें से प्रत्येक के साथ जस्ता परस्पर क्रिया करता है।
1) नाइट्रिक एसिड (समाधान)
2) लोहा (द्वितीय) हाइड्रॉक्साइड
3) मैग्नीशियम सल्फेट (समाधान)
4) सोडियम हाइड्रॉक्साइड (समाधान)
5) एल्यूमीनियम क्लोराइड (समाधान)
उत्तर क्षेत्र में चयनित पदार्थों की संख्या लिखिए।
उत्तर: 14
व्याख्या:
1) नाइट्रिक एसिड एक मजबूत ऑक्सीकरण एजेंट है और प्लैटिनम और सोने को छोड़कर सभी धातुओं के साथ प्रतिक्रिया करता है।
2) आयरन हाइड्रॉक्साइड (ll) एक अघुलनशील क्षार है। धातुएँ अघुलनशील हाइड्रॉक्साइड के साथ बिल्कुल भी प्रतिक्रिया नहीं करती हैं, और केवल तीन धातुएँ घुलनशील (क्षार) के साथ प्रतिक्रिया करती हैं - Be, Zn, Al।
3) मैग्नीशियम सल्फेट जिंक की तुलना में अधिक सक्रिय धातु का नमक है, और इसलिए प्रतिक्रिया आगे नहीं बढ़ती है।
4) सोडियम हाइड्रॉक्साइड - क्षार (घुलनशील धातु हाइड्रॉक्साइड)। केवल Be, Zn, Al धातु क्षार के साथ कार्य करते हैं।
5) AlCl 3 - जिंक की तुलना में अधिक सक्रिय धातु का नमक, अर्थात। प्रतिक्रिया संभव नहीं है।
पदार्थों की प्रस्तावित सूची में से दो ऑक्साइड चुनें जो पानी के साथ प्रतिक्रिया करते हैं।
उत्तर क्षेत्र में चयनित पदार्थों की संख्या लिखिए।
उत्तर: 14
व्याख्या:
ऑक्साइड में से, केवल क्षार और क्षारीय पृथ्वी धातुओं के ऑक्साइड, साथ ही SiO2 को छोड़कर सभी एसिड ऑक्साइड, पानी के साथ प्रतिक्रिया करते हैं।
इस प्रकार, उत्तर विकल्प 1 और 4 उपयुक्त हैं:
बाओ + एच 2 ओ \u003d बा (ओएच) 2
एसओ 3 + एच 2 ओ \u003d एच 2 एसओ 4
1) हाइड्रोजन ब्रोमाइड
3) सोडियम नाइट्रेट
4) सल्फर ऑक्साइड (IV)
5) एल्यूमीनियम क्लोराइड
तालिका में चयनित संख्याओं को संबंधित अक्षरों के नीचे लिखें।
उत्तर: 52
व्याख्या:
इन पदार्थों में लवण केवल सोडियम नाइट्रेट और एल्युमिनियम क्लोराइड हैं। सभी नाइट्रेट, जैसे सोडियम लवण, घुलनशील होते हैं, और इसलिए सोडियम नाइट्रेट सिद्धांत रूप में किसी भी अभिकर्मक के साथ अवक्षेपित नहीं हो सकता है। इसलिए, नमक X केवल एल्यूमीनियम क्लोराइड हो सकता है।
रसायन विज्ञान में परीक्षा उत्तीर्ण करने वालों में एक आम गलती एक गलतफहमी है कि एक जलीय घोल में अमोनिया एक कमजोर आधार बनाता है - प्रतिक्रिया के कारण अमोनियम हाइड्रॉक्साइड:
एनएच 3 + एच 2 ओ<=>NH4OH
इस संबंध में, अमोनिया का एक जलीय घोल धातु के लवण के घोल के साथ मिश्रित होने पर एक अवक्षेप देता है जो अघुलनशील हाइड्रॉक्साइड बनाते हैं:
3NH 3 + 3H 2 O + AlCl 3 \u003d अल (OH) 3 + 3NH 4 Cl
किसी दिए गए परिवर्तन योजना में
Cu X > CuCl 2 Y > CuI
पदार्थ X और Y हैं:
उत्तर: 35
व्याख्या:
कॉपर एक धातु है जो हाइड्रोजन के दाईं ओर गतिविधि श्रृंखला में स्थित है, अर्थात। एसिड के साथ प्रतिक्रिया नहीं करता है (एच 2 एसओ 4 (सांद्रिक) और एचएनओ 3 को छोड़कर)। इस प्रकार, हमारे मामले में क्लोरीन के साथ प्रतिक्रिया से ही कॉपर (ll) क्लोराइड का निर्माण संभव है:
Cu + Cl 2 = CuCl 2
आयोडाइड आयन (I -) समान विलयन में द्विसंयोजी कॉपर आयनों के साथ सह-अस्तित्व में नहीं रह सकते, क्योंकि ऑक्सीकृत होते हैं:
घन 2+ + 3आई - \u003d क्यूआई + आई 2
इस प्रतिक्रिया में प्रतिक्रिया समीकरण और ऑक्सीकरण पदार्थ के बीच एक पत्राचार स्थापित करें: एक पत्र द्वारा इंगित प्रत्येक स्थिति के लिए, एक संख्या द्वारा इंगित संबंधित स्थिति का चयन करें।
|
प्रतिक्रिया समीकरण ए) एच 2 + 2ली \u003d 2एलआईएच बी) एन 2 एच 4 + एच 2 \u003d 2एनएच 3 सी) एन 2 ओ + एच 2 \u003d एन 2 + एच 2 ओ डी) एन 2 एच 4 + 2एन 2 ओ \u003d 3एन 2 + 2एच 2 ओ |
आक्सीकारक |
तालिका में चयनित संख्याओं को संबंधित अक्षरों के नीचे लिखें।
उत्तर: 1433
व्याख्या:
एक प्रतिक्रिया में एक ऑक्सीकरण एजेंट एक पदार्थ होता है जिसमें एक तत्व होता है जो इसकी ऑक्सीकरण अवस्था को कम करता है।
एक पदार्थ के सूत्र और अभिकर्मकों के बीच एक पत्राचार स्थापित करें, जिनमें से प्रत्येक के साथ यह पदार्थ बातचीत कर सकता है: एक पत्र द्वारा इंगित प्रत्येक स्थिति के लिए, एक संख्या द्वारा इंगित संबंधित स्थिति का चयन करें।
| पदार्थ सूत्र | अभिकर्मकों |
| ए) घन (संख्या 3) 2 | 1) NaOH, Mg, Ba (OH) 2 2) एचसीएल, लीओएच, एच 2 एसओ 4 (समाधान) 3) BaCl 2 , Pb (NO 3) 2 , S 4) सीएच 3 कूह, कोह, FeS 5) हे 2, ब्र 2, एचएनओ 3 |
तालिका में चयनित संख्याओं को संबंधित अक्षरों के नीचे लिखें।
उत्तर: 1215
व्याख्या:
ए) Cu(NO 3) 2 + NaOH और Cu(NO 3) 2 + Ba(OH) 2 - समान अंतःक्रियाएं। धातु हाइड्रॉक्साइड के साथ नमक प्रतिक्रिया करता है यदि प्रारंभिक सामग्री घुलनशील होती है, और उत्पादों में एक अवक्षेप, एक गैस या एक कम-विघटनकारी पदार्थ होता है। पहली और दूसरी प्रतिक्रिया दोनों के लिए, दोनों आवश्यकताएं पूरी होती हैं:
Cu(NO 3) 2 + 2NaOH = 2NaNO 3 + Cu(OH) 2
Cu(NO 3) 2 + Ba(OH) 2 = Na(NO 3) 2 + Cu(OH) 2
Cu (NO 3) 2 + Mg - नमक धातु के साथ प्रतिक्रिया करता है यदि मुक्त धातु नमक में शामिल की तुलना में अधिक सक्रिय है। गतिविधि श्रृंखला में मैग्नीशियम तांबे के बाईं ओर स्थित है, जो इसकी अधिक गतिविधि को इंगित करता है, इसलिए, प्रतिक्रिया आगे बढ़ती है:
Cu(NO 3) 2 + Mg = Mg(NO 3) 2 + Cu
बी) अल (ओएच) 3 - ऑक्सीकरण अवस्था +3 में धातु हाइड्रॉक्साइड। ऑक्सीकरण अवस्था में धातु हाइड्रॉक्साइड +3, +4, और अपवाद के रूप में, हाइड्रॉक्साइड Be (OH) 2 और Zn (OH) 2, उभयचर हैं।
परिभाषा के अनुसार, एम्फ़ोटेरिक हाइड्रॉक्साइड वे होते हैं जो क्षार और लगभग सभी घुलनशील एसिड के साथ प्रतिक्रिया करते हैं। इस कारण से, हम तुरंत यह निष्कर्ष निकाल सकते हैं कि उत्तर 2 उपयुक्त है:
अल (ओएच) 3 + 3 एचसीएल = एलसीएल 3 + 3 एच 2 ओ
अल (ओएच) 3 + लीओएच (समाधान) \u003d ली या अल (ओएच) 3 + लीओएच (ठोस) \u003d से \u003d\u003e लीएएलओ 2 + 2 एच 2 ओ
2Al(OH) 3 + 3H 2 SO 4 = Al 2 (SO 4) 3 + 6H 2 O
सी) ZnCl 2 + NaOH और ZnCl 2 + Ba (OH) 2 - "नमक + धातु हाइड्रॉक्साइड" प्रकार की बातचीत। स्पष्टीकरण पीए में दिया गया है।
ZnCl 2 + 2NaOH = Zn(OH) 2 + 2NaCl
ZnCl 2 + Ba(OH) 2 = Zn(OH) 2 + BaCl 2
यह ध्यान दिया जाना चाहिए कि NaOH और Ba (OH) 2 की अधिकता के साथ:
ZnCl 2 + 4NaOH \u003d ना 2 + 2NaCl
ZnCl 2 + 2Ba(OH) 2 = Ba + BaCl 2
D) Br 2, O 2 प्रबल ऑक्सीकारक हैं। धातुओं में से, वे केवल चांदी, प्लेटिनम, सोने के साथ प्रतिक्रिया नहीं करते हैं:
Cu + Br2 टी° > CuBr2
2Cu + O2 टी° > 2 CuO
एचएनओ 3 मजबूत ऑक्सीकरण गुणों वाला एक एसिड है, क्योंकि हाइड्रोजन केशन के साथ नहीं, बल्कि एक एसिड बनाने वाले तत्व के साथ ऑक्सीकरण करता है - नाइट्रोजन एन +5। प्लेटिनम और सोने को छोड़कर सभी धातुओं के साथ प्रतिक्रिया करता है:
4HNO 3 (संक्षिप्त) + Cu \u003d Cu (NO 3) 2 + 2NO 2 + 2H 2 O
8HNO 3 (razb।) + 3Cu \u003d 3Cu (NO 3) 2 + 2NO + 4H 2 O
सजातीय श्रृंखला के सामान्य सूत्र और इस श्रृंखला से संबंधित पदार्थ के नाम के बीच एक पत्राचार स्थापित करें: एक पत्र द्वारा इंगित प्रत्येक स्थिति के लिए, एक संख्या द्वारा इंगित संबंधित स्थिति का चयन करें।
तालिका में चयनित संख्याओं को संबंधित अक्षरों के नीचे लिखें।
उत्तर: 231
व्याख्या:
पदार्थों की प्रस्तावित सूची में से दो ऐसे पदार्थों का चयन करें जो साइक्लोपेंटेन के समावयवी हों।
1) 2-मिथाइलब्यूटेन
2) 1,2-डाइमिथाइलसाइक्लोप्रोपेन
3) पेंटीन-2
4)हेक्सिन-2
5) साइक्लोपेंटीन
उत्तर क्षेत्र में चयनित पदार्थों की संख्या लिखिए।
उत्तर: 23
व्याख्या:
साइक्लोपेंटेन का आणविक सूत्र C 5 H 10 है। आइए स्थिति में सूचीबद्ध पदार्थों के संरचनात्मक और आणविक सूत्र लिखें
| पदार्थ का नाम | संरचनात्मक सूत्र | आण्विक सूत्र |
| साइक्लोपेंटेन | सी 5 एच 10 | |
| 2-मिथाइलब्यूटेन | सी 5 एच 12 | |
| 1,2-डाइमिथाइलसाइक्लोप्रोपेन | सी 5 एच 10 | |
| पेंटीन-2 | सी 5 एच 10 | |
| हेक्सिन-2 | सी 6 एच 12 | |
| साइक्लोपेंटेन | सी 5 एच 8 |
पदार्थों की प्रस्तावित सूची से, दो पदार्थों का चयन करें, जिनमें से प्रत्येक पोटेशियम परमैंगनेट के समाधान के साथ प्रतिक्रिया करता है।
1) मिथाइलबेंजीन
2) साइक्लोहेक्सेन
3) मिथाइल प्रोपेन
उत्तर क्षेत्र में चयनित पदार्थों की संख्या लिखिए।
उत्तर: 15
व्याख्या:
पोटेशियम परमैंगनेट के जलीय घोल वाले हाइड्रोकार्बन में से, जिनके संरचनात्मक सूत्र में C \u003d C या C \u003d C बॉन्ड होते हैं, साथ ही बेंजीन होमोलॉग (बेंजीन को छोड़कर) प्रतिक्रिया करते हैं।
इस प्रकार मिथाइलबेंजीन और स्टाइरीन उपयुक्त हैं।
पदार्थों की प्रस्तावित सूची में से दो पदार्थों का चयन करें जिनके साथ फिनोल परस्पर क्रिया करता है।
1) हाइड्रोक्लोरिक अम्ल
2) सोडियम हाइड्रॉक्साइड
4) नाइट्रिक अम्ल
5) सोडियम सल्फेट
उत्तर क्षेत्र में चयनित पदार्थों की संख्या लिखिए।
उत्तर: 24
व्याख्या:
फिनोल में कमजोर अम्लीय गुण होते हैं, जो अल्कोहल की तुलना में अधिक स्पष्ट होते हैं। इस कारण से, अल्कोहल के विपरीत, फिनोल, क्षार के साथ प्रतिक्रिया करते हैं:
सी 6 एच 5 ओएच + नाओएच = सी 6 एच 5 ओएनए + एच 2 ओ
फिनोल के अणु में एक हाइड्रॉक्सिल समूह होता है जो सीधे बेंजीन रिंग से जुड़ा होता है। हाइड्रॉक्सी समूह पहली तरह का एक प्राच्य है, अर्थात यह ऑर्थो और पैरा स्थितियों में प्रतिस्थापन प्रतिक्रियाओं की सुविधा प्रदान करता है:
पदार्थों की प्रस्तावित सूची में से दो पदार्थों का चयन करें जो हाइड्रोलिसिस से गुजरते हैं।
1) ग्लूकोज
2) सुक्रोज
3) फ्रुक्टोज
5) स्टार्च
उत्तर क्षेत्र में चयनित पदार्थों की संख्या लिखिए।
उत्तर: 25
व्याख्या:
ये सभी पदार्थ कार्बोहाइड्रेट हैं। मोनोसेकेराइड कार्बोहाइड्रेट से हाइड्रोलिसिस से नहीं गुजरते हैं। ग्लूकोज, फ्रुक्टोज और राइबोज मोनोसैकराइड हैं, सुक्रोज एक डिसैकराइड है, और स्टार्च एक पॉलीसेकेराइड है। नतीजतन, निर्दिष्ट सूची से सुक्रोज और स्टार्च हाइड्रोलिसिस के अधीन हैं।
पदार्थों के परिवर्तन की निम्नलिखित योजना दी गई है:
1,2-डाइब्रोमोइथेन → X → ब्रोमोइथेन → Y → एथिल फॉर्मेट
निर्धारित करें कि निम्नलिखित में से कौन से पदार्थ पदार्थ X और Y हैं।
2) एथनाल
4) क्लोरोइथेन
5) एसिटिलीन
चयनित पदार्थों की संख्या को संबंधित अक्षरों के नीचे तालिका में लिखिए।
उत्तर: 31
व्याख्या:
प्रारंभिक पदार्थ के नाम और ब्रोमीन के साथ इस पदार्थ की बातचीत के दौरान मुख्य रूप से बनने वाले उत्पाद के बीच एक पत्राचार स्थापित करें: एक पत्र द्वारा इंगित प्रत्येक स्थिति के लिए, एक संख्या द्वारा इंगित संबंधित स्थिति का चयन करें।
तालिका में चयनित संख्याओं को संबंधित अक्षरों के नीचे लिखें।
उत्तर: 2134
व्याख्या:
द्वितीयक कार्बन परमाणु में प्रतिस्थापन प्राथमिक की तुलना में अधिक मात्रा में होता है। इस प्रकार, प्रोपेन ब्रोमिनेशन का मुख्य उत्पाद 2-ब्रोमोप्रोपेन है न कि 1-ब्रोमोप्रोपेन:
साइक्लोहेक्सेन एक साइक्लोअल्केन है जिसमें 4 से अधिक कार्बन परमाणुओं का वलय आकार होता है। 4 से अधिक कार्बन परमाणुओं के वलय आकार वाले साइक्लोअल्केन्स, जब हैलोजन के साथ परस्पर क्रिया करते हैं, तो चक्र के संरक्षण के साथ एक प्रतिस्थापन प्रतिक्रिया में प्रवेश करते हैं:
साइक्लोप्रोपेन और साइक्लोब्यूटेन - न्यूनतम रिंग आकार वाले साइक्लोअल्केन मुख्य रूप से रिंग ब्रेक के साथ अतिरिक्त प्रतिक्रियाओं में प्रवेश करते हैं:
तृतीयक कार्बन परमाणु में हाइड्रोजन परमाणुओं का प्रतिस्थापन द्वितीयक और प्राथमिक की तुलना में अधिक मात्रा में होता है। इस प्रकार, आइसोब्यूटेन का ब्रोमिनेशन मुख्य रूप से निम्नानुसार होता है:
प्रतिक्रिया योजना और कार्बनिक पदार्थ के बीच एक पत्राचार स्थापित करें जो इस प्रतिक्रिया का उत्पाद है: एक पत्र द्वारा इंगित प्रत्येक स्थिति के लिए, एक संख्या द्वारा इंगित संबंधित स्थिति का चयन करें।
तालिका में चयनित संख्याओं को संबंधित अक्षरों के नीचे लिखें।
उत्तर: 6134
व्याख्या:
ताजा अवक्षेपित कॉपर हाइड्रॉक्साइड के साथ एल्डिहाइड को गर्म करने से एल्डिहाइड समूह का कार्बोक्सिल समूह में ऑक्सीकरण होता है:
एल्डिहाइड और कीटोन्स हाइड्रोजन द्वारा निकल, प्लैटिनम या पैलेडियम की उपस्थिति में अल्कोहल में कम हो जाते हैं:
प्राथमिक और द्वितीयक ऐल्कोहॉल गर्म CuO द्वारा क्रमशः एल्डिहाइड और कीटोन में ऑक्सीकृत होते हैं:
हीटिंग के दौरान इथेनॉल पर केंद्रित सल्फ्यूरिक एसिड की क्रिया के तहत, दो अलग-अलग उत्पाद संभव हैं। जब 140 डिग्री सेल्सियस से नीचे के तापमान पर गर्म किया जाता है, तो इंटरमॉलिक्युलर डिहाइड्रेशन मुख्य रूप से डायथाइल ईथर के निर्माण के साथ होता है, और जब 140 डिग्री सेल्सियस से ऊपर गर्म किया जाता है, तो इंट्रामोल्युलर डिहाइड्रेशन होता है, जिसके परिणामस्वरूप एथिलीन का निर्माण होता है:
पदार्थों की प्रस्तावित सूची में से ऐसे दो पदार्थों का चयन कीजिए जिनकी तापीय अपघटन अभिक्रिया रेडॉक्स है।
1) एल्युमिनियम नाइट्रेट
2) पोटेशियम बाइकार्बोनेट
3) एल्युमिनियम हाइड्रॉक्साइड
4) अमोनियम कार्बोनेट
5) अमोनियम नाइट्रेट
उत्तर क्षेत्र में चयनित पदार्थों की संख्या लिखिए।
उत्तर: 15
व्याख्या:
रेडॉक्स प्रतिक्रियाएं ऐसी प्रतिक्रियाएं हैं जिनके परिणामस्वरूप रासायनिक एक या अधिक रासायनिक तत्व अपनी ऑक्सीकरण अवस्था बदलते हैं।
बिल्कुल सभी नाइट्रेट्स की अपघटन प्रतिक्रियाएं रेडॉक्स प्रतिक्रियाएं हैं। Mg से Cu तक धातु नाइट्रेट धातु ऑक्साइड, नाइट्रोजन डाइऑक्साइड और आणविक ऑक्सीजन के लिए समावेशी विघटित होते हैं:
सभी धातु बाइकार्बोनेट पहले से ही धातु कार्बोनेट, कार्बन डाइऑक्साइड और पानी में मामूली हीटिंग (60 डिग्री सेल्सियस) के साथ विघटित हो जाते हैं। इस स्थिति में, ऑक्सीकरण अवस्थाओं में कोई परिवर्तन नहीं होता है:
गर्म करने पर अघुलनशील ऑक्साइड विघटित हो जाते हैं। इस मामले में प्रतिक्रिया एक रेडॉक्स प्रतिक्रिया नहीं है, क्योंकि इसके परिणामस्वरूप एक भी रासायनिक तत्व अपनी ऑक्सीकरण अवस्था नहीं बदलता है:
अमोनियम कार्बोनेट कार्बन डाइऑक्साइड, पानी और अमोनिया में गर्म होने पर विघटित हो जाता है। प्रतिक्रिया रेडॉक्स नहीं है:
अमोनियम नाइट्रेट नाइट्रिक ऑक्साइड (I) और पानी में विघटित हो जाता है। प्रतिक्रिया ओवीआर को संदर्भित करती है:
प्रस्तावित सूची से, दो बाहरी प्रभावों का चयन करें जो हाइड्रोजन के साथ नाइट्रोजन की प्रतिक्रिया की दर में वृद्धि का कारण बनते हैं।
1) तापमान कम करना
2) प्रणाली में दबाव में वृद्धि
5) एक अवरोधक का उपयोग
उत्तर क्षेत्र में चयनित बाहरी प्रभावों की संख्या लिखें।
उत्तर: 24
व्याख्या:
1) तापमान कम करना:
किसी भी प्रतिक्रिया की दर घटते तापमान के साथ घट जाती है।
2) प्रणाली में दबाव में वृद्धि:
दबाव में वृद्धि से किसी भी प्रतिक्रिया की दर बढ़ जाती है जिसमें कम से कम एक गैसीय पदार्थ भाग लेता है।
3) हाइड्रोजन सांद्रता में कमी
सान्द्रता कम करने से अभिक्रिया की दर सदैव धीमी हो जाती है।
4) नाइट्रोजन सांद्रता में वृद्धि
अभिकारकों की सांद्रता बढ़ाने से अभिक्रिया की दर हमेशा बढ़ जाती है
5) एक अवरोधक का उपयोग
अवरोधक पदार्थ होते हैं जो प्रतिक्रिया की दर को धीमा कर देते हैं।
किसी पदार्थ के सूत्र और इस पदार्थ के जलीय घोल के इलेक्ट्रोलिसिस के उत्पादों के बीच अक्रिय इलेक्ट्रोड पर एक पत्राचार स्थापित करें: एक पत्र द्वारा इंगित प्रत्येक स्थिति के लिए, एक संख्या द्वारा इंगित संबंधित स्थिति का चयन करें।
तालिका में चयनित संख्याओं को संबंधित अक्षरों के नीचे लिखें।
उत्तर: 5251
व्याख्या:
ए) NaBr → Na + + Br -
Na + धनायन और पानी के अणु कैथोड के लिए प्रतिस्पर्धा करते हैं।
2H 2 O + 2e - → H 2 + 2OH -
2Cl - -2e → Cl 2
बी) एमजी (एनओ 3) 2 → एमजी 2+ + 2एनओ 3 -
Mg 2+ धनायन और पानी के अणु कैथोड के लिए प्रतिस्पर्धा करते हैं।
क्षार धातु के धनायन, साथ ही मैग्नीशियम और एल्यूमीनियम, अपनी उच्च गतिविधि के कारण जलीय घोल में ठीक नहीं हो पाते हैं। इस कारण से, उनके बजाय, पानी के अणुओं को समीकरण के अनुसार बहाल किया जाता है:
2H 2 O + 2e - → H 2 + 2OH -
NO 3 आयन और पानी के अणु एनोड के लिए प्रतिस्पर्धा करते हैं।
2H 2 O - 4e - → O 2 + 4H +
तो उत्तर 2 (हाइड्रोजन और ऑक्सीजन) है।
सी) AlCl 3 → अल 3+ + 3Cl -
क्षार धातु के धनायन, साथ ही मैग्नीशियम और एल्यूमीनियम, अपनी उच्च गतिविधि के कारण जलीय घोल में ठीक नहीं हो पाते हैं। इस कारण से, उनके बजाय, पानी के अणुओं को समीकरण के अनुसार बहाल किया जाता है:
2H 2 O + 2e - → H 2 + 2OH -
एनोड के लिए Cl आयन और पानी के अणु प्रतिस्पर्धा करते हैं।
एक रासायनिक तत्व से युक्त आयन (F - को छोड़कर) एनोड पर ऑक्सीकरण के लिए पानी के अणुओं से प्रतिस्पर्धा जीतते हैं:
2Cl - -2e → Cl 2
इस प्रकार उत्तर 5 (हाइड्रोजन और हैलोजन) उपयुक्त है।
डी) CuSO 4 → Cu 2+ + SO 4 2-
गतिविधि श्रृंखला में हाइड्रोजन के दाईं ओर धातु के धनायन एक जलीय घोल में आसानी से कम हो जाते हैं:
घन 2+ + 2e → घन 0
उच्चतम ऑक्सीकरण अवस्था में एसिड बनाने वाले तत्व वाले एसिड अवशेष एनोड पर ऑक्सीकरण के लिए पानी के अणुओं से प्रतिस्पर्धा खो देते हैं:
2H 2 O - 4e - → O 2 + 4H +
इस प्रकार, उत्तर 1 (ऑक्सीजन और धातु) उपयुक्त है।
नमक के नाम और इस नमक के जलीय घोल के माध्यम के बीच एक पत्राचार स्थापित करें: एक अक्षर द्वारा इंगित प्रत्येक स्थिति के लिए, एक संख्या द्वारा इंगित संबंधित स्थिति का चयन करें।
तालिका में चयनित संख्याओं को संबंधित अक्षरों के नीचे लिखें।
उत्तर: 3312
व्याख्या:
ए) आयरन (III) सल्फेट - Fe 2 (SO 4) 3
एक कमजोर "आधार" Fe(OH) 3 और एक मजबूत एसिड H 2 SO 4 द्वारा बनता है। निष्कर्ष - अम्लीय वातावरण
बी) क्रोमियम (III) क्लोराइड - CrCl 3
एक कमजोर "आधार" सीआर (ओएच) 3 और एक मजबूत एसिड एचसीएल द्वारा गठित। निष्कर्ष - अम्लीय वातावरण
सी) सोडियम सल्फेट - ना 2 एसओ 4
मजबूत आधार NaOH और मजबूत एसिड H 2 SO 4 द्वारा निर्मित। निष्कर्ष - माध्यम तटस्थ है
डी) सोडियम सल्फाइड - ना 2 एस
प्रबल क्षार NaOH और दुर्बल अम्ल H2S द्वारा निर्मित। निष्कर्ष - वातावरण क्षारीय है।
एक संतुलन प्रणाली को प्रभावित करने की विधि के बीच एक पत्राचार स्थापित करें
सीओ (जी) + सीएल 2 (जी) सीओसीएल 2 (जी) + क्यू
और इस प्रभाव के परिणामस्वरूप रासायनिक संतुलन की दिशा: एक अक्षर द्वारा इंगित प्रत्येक स्थिति के लिए, एक संख्या द्वारा इंगित संबंधित स्थिति का चयन करें।
तालिका में चयनित संख्याओं को संबंधित अक्षरों के नीचे लिखें।
उत्तर: 3113
व्याख्या:
सिस्टम पर बाहरी प्रभाव के तहत संतुलन बदलाव इस तरह से होता है कि इस बाहरी प्रभाव (ले चेटेलियर के सिद्धांत) के प्रभाव को कम से कम किया जा सके।
ए) सीओ की एकाग्रता में वृद्धि से संतुलन में प्रत्यक्ष प्रतिक्रिया की ओर एक बदलाव होता है, क्योंकि इसके परिणामस्वरूप सीओ की मात्रा कम हो जाती है।
बी) तापमान में वृद्धि संतुलन को एंडोथर्मिक प्रतिक्रिया की ओर स्थानांतरित कर देगी। चूँकि अग्र अभिक्रिया ऊष्माक्षेपी (+Q) है, संतुलन विपरीत प्रतिक्रिया की ओर खिसक जाएगा।
सी) दबाव में कमी से प्रतिक्रिया की दिशा में संतुलन बदल जाएगा जिसके परिणामस्वरूप गैसों की मात्रा में वृद्धि होती है। रिवर्स रिएक्शन के परिणामस्वरूप, फॉरवर्ड रिएक्शन के परिणामस्वरूप अधिक गैसें बनती हैं। इस प्रकार, संतुलन विपरीत प्रतिक्रिया की दिशा में बदल जाएगा।
डी) क्लोरीन की सांद्रता में वृद्धि से संतुलन में एक सीधी प्रतिक्रिया की ओर बदलाव होता है, क्योंकि इसके परिणामस्वरूप क्लोरीन की मात्रा कम हो जाती है।
दो पदार्थों और एक अभिकर्मक के बीच एक पत्राचार स्थापित करें जिसके साथ इन पदार्थों को अलग किया जा सकता है: एक पत्र द्वारा इंगित प्रत्येक स्थिति के लिए, एक संख्या द्वारा इंगित संबंधित स्थिति का चयन करें।
|
पदार्थों ए) FeSO4 और FeCl2 बी) ना 3 पीओ 4 और ना 2 एसओ 4 सी) केओएच और सीए (ओएच) 2 डी) केओएच और केसीएल |
अभिकर्मक |
तालिका में चयनित संख्याओं को संबंधित अक्षरों के नीचे लिखें।
उत्तर: 3454
व्याख्या:
एक तीसरे की मदद से दो पदार्थों में अंतर करना तभी संभव है जब ये दोनों पदार्थ इसके साथ अलग-अलग तरीकों से बातचीत करें, और सबसे महत्वपूर्ण बात यह है कि ये अंतर बाहरी रूप से अलग-अलग हैं।
ए) बेरियम नाइट्रेट के घोल का उपयोग करके FeSO4 और FeCl2 के घोल को अलग किया जा सकता है। FeSO4 के मामले में, बेरियम सल्फेट का एक सफेद अवक्षेप बनता है:
FeSO 4 + BaCl 2 = BaSO 4 + FeCl 2
FeCl 2 के मामले में, अंतःक्रिया के कोई स्पष्ट संकेत नहीं हैं, क्योंकि प्रतिक्रिया आगे नहीं बढ़ती है।
बी) समाधान ना 3 पीओ 4 और ना 2 एसओ 4 को एमजीसीएल 2 के समाधान का उपयोग करके अलग किया जा सकता है। Na 2 SO 4 का घोल प्रतिक्रिया में प्रवेश नहीं करता है, और Na 3 PO 4 के मामले में मैग्नीशियम फॉस्फेट का एक सफेद अवक्षेप होता है:
2Na 3 PO 4 + 3MgCl 2 = Mg 3 (PO 4) 2 + 6NaCl
सी) केओएच और सीए (ओएच) 2 समाधानों को ना 2 सीओ 3 समाधान का उपयोग करके अलग किया जा सकता है। KOH Na 2 CO 3 के साथ प्रतिक्रिया नहीं करता है, लेकिन Ca (OH) 2 Na 2 CO 3 के साथ कैल्शियम कार्बोनेट का एक सफेद अवक्षेप देता है:
Ca(OH) 2 + Na 2 CO 3 = CaCO 3 + 2NaOH
डी) केओएच और केसीएल समाधानों को एमजीसीएल 2 समाधान का उपयोग करके अलग किया जा सकता है। KCl MgCl 2 के साथ प्रतिक्रिया नहीं करता है, और KOH और MgCl 2 के घोल को मिलाने से मैग्नीशियम हाइड्रॉक्साइड का एक सफेद अवक्षेप बनता है:
MgCl 2 + 2KOH \u003d Mg (OH) 2 + 2KCl
पदार्थ और उसके दायरे के बीच एक पत्राचार स्थापित करें: एक पत्र द्वारा इंगित प्रत्येक स्थिति के लिए, एक संख्या द्वारा इंगित संबंधित स्थिति का चयन करें।
तालिका में चयनित संख्याओं को संबंधित अक्षरों के नीचे लिखें।
उत्तर: 2331
व्याख्या:
अमोनिया का उपयोग नाइट्रोजन उर्वरकों के उत्पादन में किया जाता है। विशेष रूप से, अमोनिया नाइट्रिक एसिड के उत्पादन के लिए एक कच्चा माल है, जिससे बदले में उर्वरक प्राप्त होते हैं - सोडियम, पोटेशियम और अमोनियम नाइट्रेट (NaNO 3, KNO 3, NH 4 NO 3)।
सॉल्वैंट्स के रूप में कार्बन टेट्राक्लोराइड और एसीटोन का उपयोग किया जाता है।
एथिलीन का उपयोग उच्च-आणविक यौगिकों (पॉलिमर), अर्थात् पॉलीइथाइलीन के उत्पादन के लिए किया जाता है।
| 27-29 कार्यों का उत्तर एक संख्या है। सटीकता की निर्दिष्ट डिग्री को देखते हुए, इस संख्या को कार्य के पाठ में उत्तर क्षेत्र में लिखें। फिर इस नंबर को पहले सेल से शुरू करते हुए, संबंधित कार्य की संख्या के दाईं ओर ANSWER फॉर्म नंबर 1 में स्थानांतरित करें। प्रपत्र में दिए गए नमूनों के अनुसार प्रत्येक वर्ण को एक अलग बॉक्स में लिखें। भौतिक मात्राओं के मापन की इकाइयों को लिखने की आवश्यकता नहीं है।एक प्रतिक्रिया में जिसका थर्मोकेमिकल समीकरण एमजीओ (टीवी।) + सीओ 2 (जी) → एमजीसीओ 3 (टीवी।) + 102 केजे, 88 ग्राम कार्बन डाइऑक्साइड में प्रवेश किया। इस मामले में कितनी गर्मी जारी की जाएगी? (संख्या को निकटतम पूर्णांक में लिखिए।) उत्तर: ______________________________ केजे। उत्तर: 204 व्याख्या: कार्बन डाइऑक्साइड पदार्थ की मात्रा की गणना करें: n (CO 2) \u003d n (CO 2) / M (CO 2) \u003d 88/44 \u003d 2 mol, प्रतिक्रिया समीकरण के अनुसार, मैग्नीशियम ऑक्साइड के साथ CO2 के 1 mol की परस्पर क्रिया से 102 kJ निकलता है। हमारे मामले में, कार्बन डाइऑक्साइड की मात्रा 2 mol है। इस मामले में जारी गर्मी की मात्रा को x kJ के रूप में निरूपित करते हुए, हम निम्नलिखित अनुपात लिख सकते हैं: 1 मोल सीओ 2 - 102 केजे 2 मोल सीओ 2 - एक्स केजे इसलिए, निम्नलिखित समीकरण मान्य है: 1 एक्स = 2 102 इस प्रकार, मैग्नीशियम ऑक्साइड के साथ प्रतिक्रिया में 88 ग्राम कार्बन डाइऑक्साइड के भाग लेने पर निकलने वाली गर्मी की मात्रा 204 kJ है। जस्ता के द्रव्यमान का निर्धारण करें जो हाइड्रोक्लोरिक एसिड के साथ 2.24 लीटर (एन.ओ.) हाइड्रोजन का उत्पादन करने के लिए प्रतिक्रिया करता है। (संख्या को दहाई तक लिखिए।) उत्तर: ___________________________ उत्तर: 6.5 व्याख्या: आइए प्रतिक्रिया समीकरण लिखें: Zn + 2HCl \u003d ZnCl 2 + H 2 हाइड्रोजन पदार्थ की मात्रा की गणना करें: n (H 2) \u003d V (H 2) / V m \u003d 2.24 / 22.4 \u003d 0.1 mol। चूंकि प्रतिक्रिया समीकरण में जस्ता और हाइड्रोजन से पहले समान गुणांक होते हैं, इसका मतलब है कि प्रतिक्रिया में प्रवेश करने वाले जस्ता पदार्थों की मात्रा और इसके परिणामस्वरूप बनने वाले हाइड्रोजन भी बराबर हैं, अर्थात। n (Zn) \u003d n (H 2) \u003d 0.1 mol, इसलिए: एम (जेडएन) = एन (जेडएन) ∙ एम (जेडएन) = 0.1 ∙ 65 = 6.5 ग्राम।
|
USE 2017 रसायन विज्ञान विशिष्ट परीक्षण कार्य मेदवेदेव

एम.: 2017. - 120 पी।
रसायन विज्ञान में विशिष्ट परीक्षण कार्यों में 2017 में एकीकृत राज्य परीक्षा की सभी विशेषताओं और आवश्यकताओं को ध्यान में रखते हुए संकलित कार्यों के सेट के लिए 10 विकल्प होते हैं। मैनुअल का उद्देश्य पाठकों को रसायन विज्ञान में KIM 2017 की संरचना और सामग्री, कार्यों की कठिनाई की डिग्री के बारे में जानकारी प्रदान करना है। संग्रह में सभी परीक्षण विकल्पों के उत्तर हैं और विकल्पों में से एक के सभी कार्यों के समाधान प्रदान करता है। इसके अलावा, उत्तर और निर्णय रिकॉर्ड करने के लिए परीक्षा में प्रयुक्त प्रपत्रों के उदाहरण दिए गए हैं। कार्यों के लेखक एक प्रमुख वैज्ञानिक, शिक्षक और कार्यप्रणाली हैं, जो परीक्षा के लिए नियंत्रण माप सामग्री के विकास में सीधे शामिल हैं। मैनुअल का उद्देश्य शिक्षकों के लिए रसायन विज्ञान में परीक्षा के लिए छात्रों को तैयार करना है, साथ ही हाई स्कूल के छात्रों और स्नातकों के लिए - आत्म-प्रशिक्षण और आत्म-नियंत्रण के लिए।
प्रारूप:पीडीएफ
आकार: 1.5 एमबी
देखें, डाउनलोड करें:ड्राइव.गूगल
विषय
प्रस्तावना 4
कार्य निर्देश 5
विकल्प 1 8
भाग 1 8
भाग 2, 15
विकल्प 2 17
भाग 1 17
भाग 2 24
विकल्प 3 26
भाग 1 26
भाग 2 33
विकल्प 4 35
भाग 1 35
भाग 2 41
विकल्प 5 43
भाग 1 43
भाग 2 49
विकल्प 6 51
भाग 1 51
भाग 2 57
विकल्प 7 59
भाग 1 59
भाग 2 65
विकल्प 8 67
भाग 1 67
भाग 2 73
विकल्प 9 75
भाग 1 75
भाग 2 81
विकल्प 10 83
भाग 1 83
भाग 2 89
उत्तर और समाधान 91
भाग 1 91 के कार्यों के उत्तर
समाधान और भाग 2 93 के कार्यों के उत्तर
विकल्प 10 99 . के कार्यों का समाधान
भाग 1 99
भाग 2 113
यह पाठ्यपुस्तक रसायन विज्ञान में यूनिफाइड स्टेट परीक्षा (USE) की तैयारी के लिए कार्यों का एक संग्रह है, जो हाई स्कूल पाठ्यक्रम के लिए अंतिम परीक्षा और विश्वविद्यालय में प्रवेश परीक्षा दोनों है। मैनुअल की संरचना रसायन विज्ञान में परीक्षा उत्तीर्ण करने की प्रक्रिया के लिए आधुनिक आवश्यकताओं को दर्शाती है, जो आपको अंतिम प्रमाणीकरण के नए रूपों और विश्वविद्यालयों में प्रवेश के लिए बेहतर तैयारी करने की अनुमति देगी।
मैनुअल में कार्यों के लिए 10 विकल्प होते हैं, जो रूप और सामग्री में एकीकृत राज्य परीक्षा के डेमो संस्करण के करीब होते हैं और रसायन विज्ञान पाठ्यक्रम की सामग्री से आगे नहीं जाते हैं, जो कि राज्य मानक के संघीय घटक द्वारा मानक रूप से निर्धारित किया जाता है। सामान्य शिक्षा। रसायन विज्ञान (शिक्षा मंत्रालय का आदेश संख्या 1089 दिनांक 5 मार्च, 2004)।
असाइनमेंट में शैक्षिक सामग्री की सामग्री की प्रस्तुति का स्तर रसायन विज्ञान में एक माध्यमिक (पूर्ण) स्कूल के स्नातकों की तैयारी के लिए राज्य मानक की आवश्यकताओं के साथ सहसंबद्ध है।
एकीकृत राज्य परीक्षा की नियंत्रण माप सामग्री में तीन प्रकार के कार्यों का उपयोग किया जाता है:
- एक संक्षिप्त उत्तर के साथ जटिलता के बुनियादी स्तर के कार्य,
- संक्षिप्त उत्तर के साथ जटिलता के बढ़े हुए स्तर के कार्य,
- विस्तृत उत्तर के साथ उच्च स्तर की जटिलता के कार्य।
परीक्षा पत्र का प्रत्येक संस्करण एक ही योजना के अनुसार बनाया गया है। कार्य में दो भाग होते हैं, जिसमें कुल 34 कार्य शामिल हैं। भाग 1 में 29 लघु उत्तरीय पद हैं, जिनमें 20 मूल कठिनाई वाले प्रश्न और 9 उन्नत कठिनाई वाले पद शामिल हैं। भाग 2 में एक विस्तृत उत्तर (कार्य संख्या 30-34) के साथ उच्च स्तर की जटिलता के 5 कार्य हैं।
उच्च स्तर की जटिलता के कार्यों में, समाधान का पाठ एक विशेष रूप में लिखा जाता है। इस प्रकार के कार्य विश्वविद्यालयों में प्रवेश परीक्षा में रसायन विज्ञान में लिखित कार्य का बड़ा हिस्सा बनाते हैं।
साइट साइट पर रसायन विज्ञान में परीक्षा की तैयारी के लिए टिप्स
रसायन विज्ञान में परीक्षा (और OGE) को सही ढंग से कैसे पास करें? यदि समय केवल 2 महीने है, और आप अभी तक तैयार नहीं हैं? हां, और केमिस्ट्री से दोस्ती न करें ...
यह प्रत्येक विषय और कार्य के उत्तर के साथ परीक्षण प्रदान करता है, जिसे पास करके आप रसायन विज्ञान में परीक्षा में पाए जाने वाले मूल सिद्धांतों, पैटर्न और सिद्धांत को सीख सकते हैं। हमारे परीक्षण आपको रसायन विज्ञान में परीक्षा में पाए गए अधिकांश प्रश्नों के उत्तर खोजने की अनुमति देते हैं, और हमारे परीक्षण आपको सामग्री को समेकित करने, कमजोरियों का पता लगाने और सामग्री पर काम करने की अनुमति देते हैं।
आपको बस इंटरनेट, स्टेशनरी, समय और एक वेबसाइट चाहिए। सूत्रों/समाधानों/नोटों के लिए एक अलग नोटबुक और यौगिकों के तुच्छ नामों का शब्दकोश होना सबसे अच्छा है।
- शुरू से ही आपको अपने वर्तमान स्तर और जितने अंकों की जरूरत है, उसका आकलन करने की जरूरत है, इसके लिए आपको पास होना चाहिए। यदि सब कुछ बहुत खराब है, लेकिन आपको उत्कृष्ट प्रदर्शन की आवश्यकता है, बधाई हो, अब भी सब कुछ नहीं खोया है। आप एक ट्यूटर की मदद के बिना सफलतापूर्वक उत्तीर्ण होने के लिए खुद को प्रशिक्षित कर सकते हैं।
न्यूनतम अंक तय करें जिसे आप स्कोर करना चाहते हैं, इससे आपको यह समझने में मदद मिलेगी कि आपको आवश्यक स्कोर प्राप्त करने के लिए आपको कितने कार्यों को हल करना होगा।
स्वाभाविक रूप से, ध्यान रखें कि चीजें इतनी आसानी से नहीं चल सकती हैं और जितना संभव हो उतने कार्यों को हल करें, और अधिमानतः सभी। न्यूनतम जो आपने अपने लिए निर्धारित किया है - आपको आदर्श रूप से तय करना होगा। - आइए व्यावहारिक भाग पर चलते हैं - समाधान के लिए प्रशिक्षण।
सबसे कुशल तरीका निम्नलिखित है। केवल वही परीक्षा चुनें जिसमें आपकी रुचि हो और संबंधित परीक्षा को हल करें। लगभग 20 हल किए गए कार्य सभी प्रकार के कार्यों की बैठक की गारंटी देते हैं। जैसे ही आपको लगने लगे कि आप शुरू से अंत तक देखे गए प्रत्येक कार्य को हल करना जानते हैं, अगले कार्य के लिए आगे बढ़ें। यदि आप किसी कार्य को हल करना नहीं जानते हैं, तो हमारी साइट पर खोज का उपयोग करें। हमारी वेबसाइट पर लगभग हमेशा एक समाधान होता है, अन्यथा निचले बाएँ कोने में आइकन पर क्लिक करके ट्यूटर को लिखें - यह मुफ़्त है। - समानांतर में, हम अपनी साइट पर सभी के लिए तीसरे पैराग्राफ को दोहराते हैं, शुरुआत करते हुए।
- जब पहला भाग आपको कम से कम मध्यवर्ती स्तर पर दिया जाता है, तो आप निर्णय लेना शुरू कर देते हैं। यदि कार्यों में से एक खुद को अच्छी तरह से उधार नहीं देता है, और आपने इसके कार्यान्वयन में कोई गलती की है, तो आप इस कार्य के लिए परीक्षण या संबंधित विषय पर परीक्षण के साथ वापस आते हैं।
- भाग 2. यदि आपके पास कोई ट्यूटर है, तो उसके साथ इस भाग को सीखने पर ध्यान दें। (यह मानते हुए कि आप शेष को कम से कम 70% हल करने में सक्षम हैं)। यदि आपने भाग 2 शुरू किया है, तो आपको 100% मामलों में बिना किसी समस्या के उत्तीर्ण अंक प्राप्त करना चाहिए। अगर ऐसा नहीं होता है, तो अभी के लिए पहले भाग पर बने रहना बेहतर है। जब आप भाग 2 के लिए तैयार होते हैं, तो हम अनुशंसा करते हैं कि आप एक अलग नोटबुक प्राप्त करें जहाँ आप केवल भाग 2 के समाधान लिखेंगे। सफलता की कुंजी भाग 1 की तरह ही अधिक से अधिक कार्यों को हल करना है।