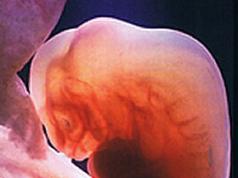
यह भी एक महान पीले रंग की एक बहुत ही सुंदर और रहस्यमय धातु है। इसका भौतिक और ऐतिहासिक मूल्य दोनों है।
"सुनहरी" कहानी
यह कहानी प्राचीन काल में शुरू होती है, क्योंकि यह वह सामग्री थी जिसने एक नए युग - धातुओं के युग को जन्म दिया। तब लोगों ने उनके असामान्य "धूप" रंग के लिए उनकी प्रशंसा की। यह माना जाता था कि केवल महान रक्त के लोग ही इस धातु के अधिकारी हो सकते हैं। यह प्रतिष्ठित था, क्योंकि सोने ने हमेशा एक महत्वपूर्ण भौतिक भूमिका निभाई है। इसे किसी भी चीज़ के लिए बदला जा सकता था, और महिलाओं ने इसके साथ अपने बालों और कपड़ों को सजाया। प्लसस के अलावा, माइनस भी थे। सोना धन है, और धन ने अक्सर अशांति और युद्धों को जन्म दिया है। स्वतंत्रता की इच्छा मानवता से अधिक प्रबल थी, और लोग मारे गए। बहुत से लोग।
सोने के गुण
सोना अपनी भव्यता और सुंदरता के बावजूद बहुत भारी धातु है। यह वस्तुतः किसी भी रासायनिक हमले के संपर्क में नहीं है, जिसने इसे "महान धातु" की उपाधि दी। यह बहुत नरम और नमनीय है, इसलिए विभिन्न प्रकार के सोने के उत्पादों की संख्या लगातार बढ़ रही है, लेकिन अत्यधिक नाजुकता इसे अपने शुद्ध रूप में उपयोग करने की अनुमति नहीं देती है - केवल चांदी या तांबे के अतिरिक्त के साथ। वैसे, उनका रंग सीधे उत्पाद में इन सामग्रियों के प्रतिशत पर निर्भर करता है। अच्छी तापीय चालकता भी विभिन्न प्रकार के उपकरणों के निर्माण में सोने के उपयोग की अनुमति देती है।
खुदाई
सोने का खनन आसान नहीं है, क्योंकि सबसे लोकप्रिय धातु चाहे जो भी हो, इसमें एकाग्रता भी कम होती है। यानी इसकी नगण्य मात्रा एक बड़े स्थान पर पड़ती है। उदाहरण के लिए, महासागरों में इस चट्टान का एक बहुत कुछ है, लेकिन यह समुद्र तल पर इतना बिखरा हुआ है कि इसे प्राप्त करना लगभग असंभव है। वही पृथ्वी की पपड़ी के लिए जाता है। लेकिन समृद्ध जमा भी हैं। मुख्य बात यह जानना है कि कहां देखना है। खनन किए गए सोने के प्रकार भी सीधे उत्पादन के स्थान पर निर्भर करते हैं। जमीन में, सोने के टुकड़े क्रिस्टल जैसे होते हैं, और जो पानी के करीब होते हैं वे गोल होते हैं।
हर समय, सोने का खनन एक बहुत ही लाभदायक व्यवसाय रहा है, लेकिन वास्तव में, यह इतना अधिक नहीं है।
यह धातु, जिसने पृथ्वी पर विजय प्राप्त की और सबसे महत्वपूर्ण धातुओं में से एक बन गई, कभी भी अपना मूल्य नहीं खोएगी। लोगों ने उसे वश में कर लिया है। हमने सीखा कि कैसे मिलाना और बदलना, सुंदर चीजें बनाना और उपयोगी चीजों का आदान-प्रदान करना है। वह हमेशा धातु और कुलीन के धनी रहेगा।
यदि यह संदेश आपके लिए उपयोगी है, तो आपको देखकर अच्छा लगा।
सोने ने कई शताब्दियों तक मन को मोहित किया है, जिससे उन्हें अपना अधिकांश जीवन इसकी तलाश में, युद्ध में जाने, धोखे और विश्वासघात में जाने के लिए मजबूर कर दिया है। हमारे ग्रह पर कई धातुएं और अन्य रसायन हैं जो बहुत पहले ही आवर्तित हो चुके हैं। उनमें से अधिक मूल्यवान हैं, और कुछ ऐसे भी हैं जो अपेक्षाकृत सस्ते हैं और व्यापक रूप से उद्योग में उपयोग किए जाते हैं। धातुओं के मूल्य वर्गों का परिसीमन बहुत पहले हुआ था, यह समझने के लिए कि देश, स्टॉक एक्सचेंज, सबसे बड़ी कंपनियां और सबसे अमीर लोग अभी भी सोने के लिए प्रयास क्यों कर रहे हैं, आपको इसे बेहतर तरीके से जानना चाहिए। रसायन विज्ञान से पहले के विज्ञानों में वैज्ञानिकों द्वारा प्राचीन काल से सोने के सूत्र का उपयोग किया जाता रहा है।
रासायनिक संदर्भ
रसायन विज्ञान में सोने को इलेक्ट्रॉनिक रूप में Aurum, संक्षिप्त Au, के रूप में नामित किया गया है: KLMNO6s1, Eion (Me => Me ++ e) = 9.22 eV। आवर्त सारणी में सोने का परमाणु क्रमांक 79 है। यह छठे आवर्त के 11वें समूह में है। इसके अलावा, सोने का एक अंतरराष्ट्रीय पंजीकरण संख्या CAS: 7440-57-5 है। तत्व का परमाणु द्रव्यमान 196.9665 g/mol है। सोना एक साधारण पदार्थ है, क्योंकि यह एक धातु के समस्थानिकों से बना होता है।

सोने के गुण अद्वितीय हैं और इसका उपयोग इलेक्ट्रॉनिक्स के क्षेत्र में, चिकित्सा में, रासायनिक प्रयोगशालाओं के लिए उपकरणों के उत्पादन में करना संभव बनाता है। इसने तापीय और विद्युत चालकता में वृद्धि की है। यही कारण है कि गैल्वनाइजेशन द्वारा सोने के महीन स्पटरिंग का उपयोग अभी भी इलेक्ट्रिक्स के उत्पादन में किया जा सकता है। सोना केवल 2880 डिग्री पर उबलता है, इसका घनत्व 19.32 ग्राम / सेमी 3 है, और इसका गलनांक 1064.43 डिग्री सेल्सियस है। सोना काफी निष्क्रिय होता है, उच्च तापमान पर भी यह अन्य रासायनिक तत्वों के साथ प्रतिक्रिया नहीं करता है।
सोने का इतिहास
सोने को उसके पीले रंग के लिए यह नाम दिया गया था। कई भाषाओं में इसका नाम अलग-अलग लगता है, लेकिन किसी न किसी रूप में यह पीले, सुनहरे या हरे रंग के पदनाम से जुड़ा है। सोने के कई प्रमुख पैरामीटर हैं। यह एक उत्कृष्ट धातु है, क्योंकि यह बाहरी वातावरण के प्रभाव में जंग नहीं करता है और ऑक्सीडेटिव प्रतिक्रियाओं से नहीं गुजरता है। वैसे, यही कारण है कि दंत चिकित्सा में इसका सफलतापूर्वक उपयोग किया जाता है। सोने का घनत्व अधिक होता है और इसी पर गाद, बालू, नदी के पानी को धोकर इसके निष्कर्षण की व्यवस्था बनाई जाती है। साथ ही सोना बहुत ही सॉफ्ट और प्लास्टिक का होता है। धातु के गुणों के बावजूद, इसे विशेष उपकरणों के उपयोग के बिना भी खरोंच किया जा सकता है।

सोना शायद मनुष्य द्वारा खोजी गई पहली धातु थी। पुरातनता के सभी जीवित स्रोतों में इसका उल्लेख है, इसे उच्च सम्मान में रखा गया था और यह काफी महंगा था। इसमें कोई शक नहीं कि सोने में दिलचस्पी कभी कम नहीं हुई। इसकी सुंदरता और विशेष गुणों के लिए इसकी सराहना की गई, केवल बाद में इसके भौतिक गुणों के मूल्य का एहसास हुआ। पदार्थ का रासायनिक सूत्र ज्ञात होने से पहले ही, सोना खरीदना एक उत्कृष्ट निवेश माना जाता था।
प्राकृतिक सोना
प्रकृति में सोना फॉसिल नगेट्स या प्लेसर के रूप में पाया जाता है। यदि हम अयस्क में बिखरे हुए या पानी से धुले हुए अनाज के बारे में बात नहीं कर रहे हैं, तो ये डली हैं जिन्हें विभिन्न उप-प्रजातियों के लिए जिम्मेदार ठहराया जा सकता है: इलेक्ट्रम, पैलेडियम सोना, कपरस, बिस्मथ। इस मामले में, सोने की रासायनिक संरचना में अशुद्धियाँ शामिल होंगी, जो प्रतिशत में भिन्न हो सकती हैं।

इलेक्ट्रम चांदी के साथ एक मिश्र धातु है, जिसे प्राचीन काल से जाना जाता है। दरअसल, यह पहला मिश्र धातु है जिससे किसी व्यक्ति ने निपटा है। यह एक ऐसा खनिज है जिसमें लगभग आधे पर चांदी के कण होते हैं। इसका नाम "एम्बर" शब्द से आया है, जिसे खनिज की उपस्थिति से उद्धृत किया गया था। पैलेडियम मिश्र धातु चांदी, तांबा, क्रोमियम, निकल और अन्य पदार्थों के साथ यौगिक हैं। इस चांदी-गुलाबी धातु का 4% तक बिस्मथ सोना होता है। क्यूप्रस गोल्ड में 20% तक कॉपर होता है, जो इसे लाल रंग का रंग देता है। लोहा, पारा, इरिडियम से सोने का खनिज निर्माण भी संभव है। प्लेसर गोल्ड को प्लेसर गोल्ड कहा जाता है, और इसमें भारी धातुओं का भंडार होता है, जिसमें सोने के दाने भी होते हैं।
शुद्ध सोना प्राप्त करना
सोना प्रकृति में अपने शुद्ध रूप में लगभग कभी नहीं पाया जाता है। सोने की रेत और अयस्क को धोने की कई शताब्दियों के बाद, मानव जाति ने सोने के दानों को अलग करने का एक अधिक कुशल तरीका खोजा है - समामेलन। इस विधि में ऐसे तत्वों की आवश्यकता होती है जो सोने के साथ प्रतिक्रिया करने में सक्षम हों और यह तत्व पारा है। इसे अयस्क में मिलाया जाता है, सोने के साथ मिलाया जाता है, और फिर हटा दिया जाता है और आगे के काम में लगाया जाता है। साइनाइडेशन भी काम करता है। जिंक का उपयोग करके परिणामी घोल से सोना अवक्षेपित होता है। क्षार समाधान के साथ उत्थान भी किया जा सकता है।

एक नियंत्रित मात्रा और अशुद्धियों की संरचना के साथ एक साफ पिंड या मिश्र धातु प्राप्त करने के लिए, कई प्रक्रियाओं को पूरा किया जाना चाहिए। इस तरह के उपायों के परिसर को शोधन कहा जाता है - शुद्ध सोना प्राप्त करने के लिए अयस्क, स्क्रैप, मिश्र धातु की शुद्धि। काम के लिए एक सामग्री के रूप में, आप किसी भी सोने के कण ले सकते हैं - इलेक्ट्रोड के हिस्से, प्रयोगशाला उपकरण के तत्व, गहने। ऐसे कई तरीके हैं जिन्हें सबसे सफल माना जाता है। सोने की रसायन शास्त्र इन विधियों पर आधारित है, क्योंकि वे सोने के कणों का न्यूनतम नुकसान उठाते हैं और सहायक सामग्री पर कम पैसा खर्च करते हैं।

रासायनिक शोधन अयस्क, सोने के असर वाले प्राकृतिक चिप्स या प्रयुक्त उत्पादों के स्क्रैप से रासायनिक तत्वों को अलग करना है। यह बहु-मंच है और इसमें प्रयोगों की एक श्रृंखला शामिल है जिसका उद्देश्य एक मूल्यवान घटक को उजागर करना है। सबसे पहले, लोहे को संरचना से बाहर रखा गया है, क्योंकि यह आवश्यक संचालन करने की अनुमति नहीं देता है। इसे चुंबक के साथ, या सल्फ्यूरिक या हाइड्रोक्लोरिक एसिड के उपयोग से बाहर रखा जा सकता है, जो इसके कणों को भंग कर देगा। अगले चरण में नाइट्रिक एसिड के उपयोग की आवश्यकता होती है, जो पारंपरिक रूप से सोने से सटे कई अशुद्धियों को घोलता है - तांबा, चांदी, जस्ता, टिन। सोना तलछट में रहता है, और टेबल नमक प्रतिक्रिया में प्रयोग किया जाता है। इसके अलावा, सोने और चांदी से युक्त तलछट को नाइट्रिक और हाइड्रोक्लोरिक एसिड से उपचारित किया जाता है। आवश्यक मिश्रण करने के बाद, हीटिंग और जल निकासी की एक श्रृंखला प्राप्त की जाती है, एक भूरा अवक्षेप प्राप्त होता है, जिसे अच्छी तरह से धोया जाता है। शुद्धिकरण के अंतिम चरण के बाद, सोने की धूल प्राप्त होती है, जिसे एक पिंड में पिघलाया जाता है। ऐसे सोने की शुद्धता 99.95% तक हो सकती है।
उत्पादन एक इलेक्ट्रोकेमिकल सफाई विधि का उपयोग करता है, इस मामले में, शुद्ध कच्चे माल की आवश्यकता होती है, कम से कम 900 नमूने, प्रक्रिया के लिए सबसे शुद्ध सोना, साथ ही साथ एसिड। मिलर की विधि भी है, जो वाष्पशील क्लोरीन का उपयोग करके अशुद्धियों के गैसीय वाष्पीकरण पर आधारित है। यह तरीका खतरनाक हो सकता है क्योंकि जहरीली गैसें हवा में प्रवेश कर सकती हैं।
अब कोई भी सोने की संरचना पर सवाल नहीं उठाता है, लेकिन एक बार इसे न केवल खनिजों का एक घटक और शुद्ध रूप में एक महान धातु माना जाता था, बल्कि कुछ ऐसा भी होता है जिसे किसी अन्य पदार्थ से प्राप्त किया जा सकता है। हम कीमिया के बारे में बात कर रहे हैं, एक विज्ञान जो रसायन विज्ञान से बहुत पहले दिखाई दिया और इसके पूर्वज बन गए। कीमियागरों को जादूगर और धोखेबाज माना जाता था, उन पर भरोसा और डर नहीं था, लेकिन, फिर भी, ऐसा कोई सबूत नहीं है जो निश्चित रूप से यह कहना संभव बना सके कि यह छद्म विज्ञान या कल्पना है। कीमिया पर किताबें, प्रत्यक्षदर्शी खातों, इतिहास में लिखी गई कहानियां हैं। बेशक, सोना हमेशा सबसे बड़ा मूल्य रहा है और इसे प्रयोगों के माध्यम से प्राप्त करने का विचार वैज्ञानिकों की कई पीढ़ियों के लिए "फिक्स आइडिया" बन गया है।

कीमियागरों के पास दुनिया की एक विशेष दृष्टि थी, उनका मानना था कि प्रकृति में सब कुछ एक है और सब कुछ विकसित होता है। यह मानव आत्मा, और खनिजों और पदार्थों पर लागू होता है। सीसा को सबसे कम धातु माना जाता था, यह अपूर्ण था, उच्चतम सोना था, क्योंकि इसमें असाधारण गुण थे। बहुत सारे सबूत इंगित करते हैं कि कीमियागरों ने एक गुप्त यौगिक पाया जिसने टिन और पारा को शुद्धतम सोने में बदल दिया - दार्शनिक का पत्थर। इस पत्थर की संरचना और गुण अज्ञात रहे, क्योंकि जिन लोगों ने इसका आविष्कार किया, वे इस रहस्य को कब्र तक ले गए, और गवाह केवल पाउडर या पत्थर के साथ मिश्रित टिन को सोने में बदलने की प्रक्रिया के बारे में बता सकते थे। अलकेमिकल सोना आज तक मन को उत्साहित करता है, इस तथ्य के बावजूद कि हमारी तकनीकें इतनी उन्नत हैं, सूत्र अभी भी अज्ञात है। इन प्रयोगों की विश्वसनीयता के पक्ष में एकमात्र प्रमाण यूरेनियम के साथ प्रयोग कहा जा सकता है, जब विशेष जोखिम के तहत, यह पूरी तरह से अलग, नए पदार्थ बनाता है। इतिहास को सम्मान की आवश्यकता है, और हमारे युग, लंबी यात्राओं और शानदार आविष्कारकों से पहले बनाई गई भव्य संरचनाओं को याद करते हुए, कोई केवल अपने कंधों को सिकोड़ सकता है, यह मानते हुए कि पुरातनता के कीमियागर धातुओं के बारे में हमसे ज्यादा जानते थे।
रसायन विज्ञान में सोना विशेष गुणों वाले तत्वों में से एक है, लेकिन लोगों के जीवन में इसका नाम अन्य धातुओं की तुलना में पूरी तरह से अलग संघों को प्रेरित करता है। यह धन और सफलता का एक उपाय है, शक्ति और प्रभाव का प्रतीक है। बेशक, इस धातु के साथ अपने परिचित की शुरुआत में, एक व्यक्ति इसकी सुंदरता से आकर्षित हुआ था। सुनहरे रंग ने सूर्य की याद दिला दी, जिसे कई सदियों से कई लोगों द्वारा देवता बनाया गया था। सोना धार्मिक भवनों और साज-सज्जा के लिए एक सामग्री बन गया है। बाद में इससे पहले सिक्के जारी किए गए, इसलिए मुद्रा की अवधारणा प्रचलन में आई। साम्राज्यों और साम्राज्यों के समय में, बर्तनों और परिसरों की सजावट में सोने का उपयोग किया जाता था। चर्चों में, यह हमेशा फ्रेम, कवरिंग, गहनों के लिए इस्तेमाल किया गया है, सोने की पत्ती व्यापक थी, और चर्चों के गुंबद पत्ते से ढके हुए थे। आजकल सोने का उपयोग सौंदर्य और विज्ञान दोनों के लिए किया जाता है।
रासायनिक गुण।
इस तथ्य के बावजूद कि डी.आई. मेंडेलीव की आवधिक प्रणाली में सोना चांदी और तांबे के साथ एक ही समूह में है, इसके रासायनिक गुण प्लैटिनम समूह धातुओं के रासायनिक गुणों के बहुत करीब हैं। Au - Au (111) युग्म का इलेक्ट्रोड विभव - 1.5 V है। इतने उच्च मान के कारण, तनु और सांद्रित HCI, HNO, HSO सोने पर क्रिया नहीं करते हैं। हालांकि, एचसीआई में, यह मैग्नीशियम डाइऑक्साइड, फेरिक क्लोराइड और तांबे जैसे ऑक्सीकरण एजेंटों की उपस्थिति के साथ-साथ ऑक्सीजन की उपस्थिति में उच्च दबाव और उच्च तापमान में घुल जाता है। सोना एचसीआई और एचएनओ (एक्वा रेजिया) के मिश्रण में भी आसानी से घुल जाता है। रासायनिक दृष्टि से सोना एक निष्क्रिय धातु है। हवा में, यह मजबूत हीटिंग के साथ भी नहीं बदलता है। सोना क्लोरीन के पानी में और क्षार धातु साइनाइड के वातित घोल में आसानी से घुल जाता है। पारा भी सोने को घोलता है, एक अमलगम बनाता है, जो 15% से अधिक सोने पर ठोस हो जाता है। ऑक्सीकरण अवस्था +1 और +3 के संगत स्वर्ण यौगिकों की दो ज्ञात श्रृंखलाएँ हैं। तो, सोना दो ऑक्साइड बनाता है - गोल्ड ऑक्साइड, या गोल्ड ऑक्साइड, Au O और गोल्ड ऑक्साइड, या गोल्ड ऑक्साइड, Au O। ऐसे यौगिक जिनमें सोने की ऑक्सीकरण अवस्था +3 अधिक स्थिर होती है। सोने के यौगिक आसानी से धातु में अपचित हो जाते हैं। कम करने वाले एजेंट उच्च दबाव में हाइड्रोजन हो सकते हैं, सोने, हाइड्रोजन पेरोक्साइड, दो टिन क्लोराइड, लौह सल्फेट, टाइटेनियम ट्राइक्लोराइड, लीड ऑक्साइड, मैंगनीज डाइऑक्साइड, क्षार और क्षारीय पृथ्वी धातु पेरोक्साइड तक वोल्टेज की सीमा में कई धातुएं हो सकती हैं। सोने को बहाल करने के लिए विभिन्न कार्बनिक पदार्थों का भी उपयोग किया जाता है: फॉर्मिक और ऑक्सालिक एसिड, हाइड्रोक्विनोन, हाइड्राज़िन, मेटोल, एसिटिलीन, आदि। सोने को उच्च ऊर्जा के कारण ऑक्सीजन और सल्फर युक्त लिगैंड, अमोनिया और एमाइन के साथ कॉम्प्लेक्स बनाने की क्षमता की विशेषता है। संबंधित आयनों का निर्माण। सबसे आम यौगिक मोनोवैलेंट और ट्रिटेंट गोल्ड हैं। उन्हें अक्सर जटिल अणु माना जाता है जिसमें समान संख्या में Au (1) और Au (3) परमाणु होते हैं। त्रिसंयोजक सोना एक बहुत मजबूत ऑक्सीकरण एजेंट है और कई स्थिर यौगिक बनाता है। सोना क्लोरीन, फ्लोरीन, आयोडीन, ऑक्सीजन, सल्फर, टेल्यूरियम और सेलेनियम के साथ मिलकर बनता है।
भौतिक और यांत्रिक गुण।
सोना लंबे समय से वैज्ञानिक अनुसंधान का विषय रहा है और
धातुओं की संख्या से संबंधित है, जिनके गुणों का काफी गहराई से अध्ययन किया गया है। सोने की परमाणु संख्या 79 है, परमाणु द्रव्यमान 197.967 है, और परमाणु मात्रा 10.2 सेमी / मोल है। प्राकृतिक सोना मोनोआइसोटोपिक होता है और सामान्य परिस्थितियों में अधिकांश कार्बनिक और अकार्बनिक पदार्थों के संबंध में निष्क्रिय होता है। सोने में एक चेहरा-केंद्रित घन जाली होती है और यह एलोट्रोपिक परिवर्तनों से नहीं गुजरती है। सोने के पिघलने के तापमान को मापने के परिणामस्वरूप बड़ी विसंगतियां मौजूद हैं - 1062.7 से 1067.4 सी। एक नियम के रूप में, सोने का पिघलने बिंदु 1063 सी माना जाता है। 25 सी पर सोने के उच्च बनाने की क्रिया की गर्मी 87.94 किलो कैलोरी है। पिघले हुए सोने का पृष्ठ तनाव 1.134 J/m है। 20 C पर सोने की की तापीय चालकता 0.743 cal है और बढ़ते तापमान के साथ थोड़ा बदलता है। कम तापमान पर, अधिकतम तापीय चालकता 10 K पर देखी जाती है। 0 - 100 C पर विद्युत प्रतिरोधकता का तापमान गुणांक 0.004 C होता है। जाली दोषों के गठन के परिणामस्वरूप, सोने की सीसा का विकिरण, कार्य सख्त और शमन, जाली पैरामीटर और धातु के आयतन में छोटे बदलावों के लिए। हालांकि, ये परिवर्तन बहुत महत्वपूर्ण नहीं हैं, रैखिक आयाम केवल प्रतिशत के कुछ सौवें हिस्से में बदलते हैं। एनीलिंग की प्रक्रिया में, गुणों का एक थर्मल रिटर्न होता है, जिसमें परिवर्तन जाली दोषों के कारण होता है। विरूपण के दौरान सोने की पुन: क्रिस्टलीकरण की प्रवृत्ति के कारण प्लास्टिक विरूपण के दौरान सुदृढ़ीकरण बहुत महत्वहीन है।
सोने की सामान्य विशेषताएं।
सोना एक चमकदार पीली चमकदार धातु है। सोना सबसे निष्क्रिय धातुओं में से एक है, इसकी मानक इलेक्ट्रोड क्षमता +1.68 वी है। यह बहुत लचीला और लचीला है; रोलिंग द्वारा इसका उपयोग 0.0002 मिमी से कम की मोटाई वाली चादरें बनाने के लिए किया जा सकता है, और 1 ग्राम सोने से 3.5 किमी लंबा तार खींचना संभव है। सोना गर्मी और विद्युत प्रवाह का एक उत्कृष्ट संवाहक है, इस संबंध में चांदी और तांबे के बाद दूसरा स्थान है। सोना एक बहुत ही नरम धातु है (और फिर सबसे नरम नहीं, सीसा और टिन, उदाहरण के लिए, और भी नरम होते हैं)। शुद्ध सोना एक नाखून से खरोंचा जाता है। कोमलता ने हमेशा सोने को प्रसंस्करण के लिए एक बहुत ही सुविधाजनक सामग्री बना दिया है। इसकी कोमलता के कारण, मिश्र धातुओं में सोने का प्रयोग किया जाता है, आमतौर पर चांदी या तांबे के साथ। इन मिश्र धातुओं का उपयोग विद्युत संपर्कों, दंत कृत्रिम अंगों और गहनों के लिए किया जाता है। सोना बहुत आसानी से टूट जाता है, बेहतरीन धूल में बदल जाता है। इस संपत्ति के कारण, यह हर जगह बिखरा हुआ है, और इस प्रकार, प्रकृति में व्यापक है। सोना बहुत लचीला और नमनीय होता है, जो निस्संदेह इसकी कोमलता का परिणाम है। . हवा में, यह उच्च तापमान पर भी नहीं बदलता है, हाइड्रोक्लोरिक, सल्फ्यूरिक और नाइट्रिक एसिड में नहीं घुलता है। लेकिन एक्वा रेजिया में, जटिल क्लोरोऑरिक एसिड प्राप्त करने के लिए सोना आसानी से घुल जाता है:
Au + HNO + 4HCl = H + NO + 2HO
सोना क्लोरीन पानी, पारा और क्षार धातु साइनाइड के वातित (हवा से उड़ा हुआ) घोल में उतनी ही आसानी से घुल जाता है।
प्रकृति में सोना।
सोना प्रकृति में लगभग विशेष रूप से अपने मूल राज्य में पाया जाता है, मुख्य रूप से क्वार्ट्ज में एम्बेडेड या क्वार्ट्ज रेत में निहित छोटे अनाज के रूप में। लोहा, सीसा और तांबे के सल्फाइड अयस्कों में सोना कम मात्रा में पाया जाता है। इसके निशान समुद्र के पानी में पाए जाते हैं। सोने के बड़े भंडार दक्षिण अफ्रीका, अलास्का, कनाडा और ऑस्ट्रेलिया में स्थित हैं।
पानी से धोने से रेत और कुचल क्वार्ट्ज चट्टान से सोना अलग हो जाता है, जो रेत के कणों को हल्का के रूप में दूर ले जाता है, या रेत को तरल पदार्थ के साथ इलाज करके सोना को भंग कर देता है। सबसे अधिक इस्तेमाल किया जाने वाला घोल सोडियम साइनाइड (NaCN) है, जिसमें जटिल आयन बनाने के लिए सोना ऑक्सीजन की उपस्थिति में घुल जाता है -:
4Au + 8NaCN + O 2 + 2H 2 0 -> 4Na + 4NaOH
परिणामी समाधान से, जस्ता के साथ सोना पृथक होता है:
2Na + Zn -> ना 2 + 2Au
मुक्त किए गए सोने को पतला सल्फ्यूरिक एसिड के साथ जस्ता को अलग करने के लिए संसाधित किया जाता है, धोया और सुखाया जाता है। अशुद्धियों (मुख्य रूप से चांदी से) से सोने की आगे शुद्धिकरण गर्म केंद्रित सल्फ्यूरिक एसिड या इलेक्ट्रोलिसिस द्वारा किया जाता है।
1843 में रूसी इंजीनियर पी.आर.बाग्रेशन द्वारा पोटेशियम या सोडियम साइनाइड के घोल का उपयोग करके अयस्कों से सोना निकालने की विधि विकसित की गई थी। यह विधि, जो धातुओं को प्राप्त करने के हाइड्रोमेटेलर्जिकल तरीकों से संबंधित है, वर्तमान में स्वर्ण धातु विज्ञान में सबसे व्यापक है। चांदी और तांबे की अशुद्धियों के साथ देशी सोना समान धातुओं के साथ कृत्रिम मिश्र धातुओं से काफी भिन्न होता है। मिश्र धातु में एक सजातीय संरचना होती है, जो धातुओं के पिघले हुए मिश्रण के जमने के परिणामस्वरूप बनती है। जलीय घोल से क्रिस्टलीकरण के परिणामस्वरूप मूल धातु दिखाई देती है।
अपने शुद्ध रूप में, सोने में एक मजबूत धात्विक चमक के साथ एक सुंदर पुआल-पीला रंग होता है। इस मामले में, हम कह सकते हैं कि सोना सभी धातुओं में सबसे पीला है।
प्रकृति में, शुद्ध सोना नहीं पाया जाता है, और अशुद्धता धातुएं (मुख्य रूप से तांबा और चांदी) इसे विभिन्न रंग और रंग देती हैं - हल्के पीले (यहां तक कि हरा) से लेकर चमकीले पीले-लाल तक। पैलेडियम का एक मिश्रण सोने के सफेद ("सफेद" सोना) को रंग देता है।
सोने का रंग धातु के टुकड़े की मोटाई और उसके एकत्रीकरण की स्थिति पर भी निर्भर करता है। उदाहरण के लिए, एक बहुत पतली सोने की प्लेट हरे रंग की होती है। पिघला हुआ सोना एक ही रंग का होता है, और इसके वाष्प हरे-पीले रंग के होते हैं। उदास अवस्था में सोना आमतौर पर माणिक या गहरे बैंगनी रंग का होता है।
इसके आवेदन के बारे में बात करें।
कभी-कभी देशी सोना लोहे के आक्साइड की एक फिल्म से ढका होता है। इस मामले में, इसका रंग सबसे सामान्य हो सकता है - गंदा भूरा, भूरा या लगभग काला भी। जब खनन किया जाता है, तो ऐसे सोने को मेजबान अपशिष्ट चट्टान से अलग करना बहुत मुश्किल होता है और इसलिए नुकसान से बचने के लिए बहुत सावधानीपूर्वक निगरानी की आवश्यकता होती है। इस तरह के सोने को "एक शर्ट में" कहा जाता है, जिसमें न केवल लोहे के आक्साइड होते हैं। कुछ मामलों में, ये सोने की सतह में दबाए गए अपशिष्ट चट्टान के सबसे छोटे कण हो सकते हैं। यह कहा जाना चाहिए कि इस तरह की "शर्ट" न केवल सोने के बीच अंतर करने में बाधा डालती है, बल्कि इसके प्रसंस्करण को भी जटिल बनाती है।
सोना एक्स-रे को अच्छी तरह अवशोषित करता है। प्राकृतिक सोने का भिन्नात्मक परमाणु द्रव्यमान (196.9) इंगित करता है कि इसमें विभिन्न समस्थानिकों का मिश्रण होता है। एक "महान" धातु के रूप में, सोना बहुत अनिच्छा से रासायनिक प्रतिक्रियाओं में प्रवेश करता है, लेकिन फिर भी यह कुछ तत्वों के साथ बातचीत करता है, विशेष रूप से हैलोजन (क्लोरीन, ब्रोमीन, आयोडीन) के साथ, AuCl, AuCl 3 जैसे यौगिकों का निर्माण करता है। यह साइनाइड, पारा और टेल्यूरियम के साथ भी संपर्क करता है। तथाकथित विस्फोटक सोना - एयू (एनएच) 3, (सीएच) 3 सहित कृत्रिम साधनों द्वारा प्राप्त यौगिक हैं, जो आसानी से प्रभाव पर या गर्म होने पर आसानी से फट जाते हैं। कुछ तरल पदार्थों में, हालांकि बहुत मुश्किल है, सोना घुल जाता है। अयस्कों, रेत और सायनाइड्स में इसके विघटन के आधार पर सांद्रण से सोना निकालना इसके हाइड्रोमेटालर्जिकल प्रसंस्करण में मुख्य प्रक्रियाओं में से एक है।
घन प्रणाली में सोना क्रिस्टलीकृत होता है। क्रिस्टल लम्बी या अष्टफलकीय हो सकते हैं। पिघलने के बाद ठोस होने पर, सोने के क्रिस्टल अनियमित बहुभुज के रूप में दिखाई देते हैं। शीतलन जितना धीमा होगा, क्रिस्टल का आकार उतना ही बड़ा होगा।
1953 में, एफ। फ्रीडेंसबर्ग, 3000 मीटर के विकास की अधिकतम गहराई से आगे बढ़ते हुए, यह निर्धारित किया कि पृथ्वी की पपड़ी में 4 470 000 टन सोना है। वर्तमान में, दक्षिण अफ्रीका की सोने की खदानें 4 किलोमीटर की गहराई के करीब आ गई हैं। इस गहराई के लिए गणना के परिणाम और भी प्रभावशाली हैं।
उल्कापिंडों में सोने की खोज इस बात का अकाट्य प्रमाण है कि सोना न केवल पृथ्वी पर, बल्कि अन्य ब्रह्मांडीय पिंडों पर भी व्यापक है।
लेकिन सोना सिर्फ चट्टानों में ही नहीं पाया जाता है। समुद्रों और महासागरों में इसका बहुत कुछ है, हालांकि इसकी एकाग्रता और कुल मात्रा स्थापित नहीं की गई है।
विज्ञान और प्रौद्योगिकी में सोने का अनुप्रयोग
हजारों वर्षों से, सोने का उपयोग गहनों और सिक्कों के उत्पादन के लिए किया जाता रहा है, और दंत कृत्रिम अंगों के लिए सोने का उपयोग प्राचीन मिस्रवासियों के लिए जाना जाता है। कांच उद्योग में सोने के उपयोग को 17वीं शताब्दी के अंत से जाना जाता है। सोने की पन्नी, और बाद में सोने की इलेक्ट्रोप्लेटिंग, चर्च के मंदिरों के गुंबदों को सोने के लिए व्यापक रूप से इस्तेमाल किया गया था। केवल पिछले 40 - 45 वर्षों को सोने के विशुद्ध रूप से तकनीकी उपयोग की अवधि के लिए जिम्मेदार ठहराया जा सकता है। सोने के गुणों का एक अनूठा समूह है जो किसी अन्य धातु में नहीं है। इसमें आक्रामक मीडिया के लिए उच्चतम प्रतिरोध है, विद्युत और तापीय चालकता के मामले में यह चांदी और तांबे के बाद दूसरे स्थान पर है, सोने के कोर में एक बड़ा न्यूट्रॉन कैप्चर क्रॉस-सेक्शन है, सोने की अवरक्त किरणों को प्रतिबिंबित करने की क्षमता 100% के करीब है , मिश्र धातुओं में इसमें उत्प्रेरक गुण होते हैं। सोना बहुत तकनीकी रूप से उन्नत है, इससे अल्ट्रा-थिन फ़ॉइल और माइक्रोन तार बनाना आसान है। सोना चढ़ाना आसानी से धातुओं और चीनी मिट्टी की चीज़ें पर लागू होता है। सोना अच्छी तरह से मिलाया जाता है और दबाव वेल्ड किया जाता है। उपयोगी गुणों के इस संयोजन ने प्रौद्योगिकी की सबसे महत्वपूर्ण आधुनिक शाखाओं में सोने का व्यापक उपयोग किया है: इलेक्ट्रॉनिक्स, संचार प्रौद्योगिकी, अंतरिक्ष और विमानन प्रौद्योगिकी, रसायन शास्त्र।
यह ध्यान दिया जाना चाहिए कि 90% सोने का उपयोग इलेक्ट्रॉनिक्स में कोटिंग्स के रूप में किया जाता है। इलेक्ट्रॉनिक्स और संबंधित इंजीनियरिंग उद्योग प्रौद्योगिकी में सोने के मुख्य उपभोक्ता हैं। इस क्षेत्र में, सोल्डरिंग ट्रांजिस्टर तत्वों और अन्य उद्देश्यों के लिए, दबाव या अल्ट्रासोनिक वेल्डिंग, प्लग कनेक्टर के संपर्कों, पतले तार कंडक्टर के रूप में एकीकृत सर्किट को जोड़ने के लिए सोने का व्यापक रूप से उपयोग किया जाता है। बाद के मामले में, यह विशेष रूप से महत्वपूर्ण है कि सोना इंडियम, गैलियम, सिलिकॉन और अन्य तत्वों के साथ कम पिघलने वाले यूटेक्टिक्स बनाता है जिनमें एक निश्चित प्रकार की चालकता होती है। इलेक्ट्रॉनिक्स में तकनीकी सुधार के अलावा, सोने के बजाय कई हिस्सों और असेंबली के लिए, उन्होंने पैलेडियम, टिन कोटिंग्स, टिन-लीड मिश्र और 65% एसएन + 35% नी के मिश्र धातु के साथ सोने की परत का उपयोग करना शुरू कर दिया। निकल के साथ टिन के मिश्र धातु में उच्च पहनने के प्रतिरोध, संक्षारण प्रतिरोध, स्वीकार्य संपर्क प्रतिरोध और विद्युत चालकता है। इस तथ्य के बावजूद कि वर्तमान में इलेक्ट्रॉनिक्स में सोने की खपत लगातार बढ़ रही है, यह माना जाता है कि सोने को बचाने के उपायों के लिए नहीं तो यह 30% अधिक हो सकता है।
माइक्रोइलेक्ट्रॉनिक में, विभिन्न विद्युत प्रतिरोध वाले सोने पर आधारित पेस्ट का व्यापक रूप से उपयोग किया जाता है। कम-वर्तमान उपकरणों के संपर्कों के लिए सोने और उसके मिश्र धातुओं का व्यापक उपयोग इसके उच्च विद्युत और संक्षारक गुणों के कारण होता है। चांदी, प्लेटिनम और उनके मिश्र धातु, जब माइक्रोवोल्टेज पर माइक्रोक्यूरेंट स्विच करने वाले संपर्कों के रूप में उपयोग किए जाते हैं, तो बहुत खराब परिणाम देते हैं। हाइड्रोजन सल्फाइड से दूषित वातावरण में चांदी जल्दी खराब हो जाती है, जबकि प्लैटिनम कार्बनिक यौगिकों को पोलीमराइज़ करता है। सोना इन कमियों से मुक्त है, और इसके मिश्र धातु संपर्क उच्च विश्वसनीयता और लंबी सेवा जीवन प्रदान करते हैं। कम वाष्प दबाव वाले सोने के सोल्डर का उपयोग इलेक्ट्रॉनिक ट्यूब भागों के वैक्यूम-टाइट सीम के साथ-साथ एयरोस्पेस उद्योग में सोल्डर असेंबलियों के लिए किया जाता है।
कोबाल्ट या क्रोमियम के साथ सोने के मिश्र धातुओं का उपयोग तापमान को नियंत्रित करने और विशेष रूप से कम तापमान को मापने के लिए तकनीक को मापने में किया जाता है। रासायनिक उद्योग में, सोने का उपयोग मुख्य रूप से संक्षारक पदार्थों के परिवहन के लिए स्टील पाइप पर चढ़ने के लिए किया जाता है।
सोने की मिश्रधातुओं का उपयोग घड़ी के मामलों और फाउंटेन पेन के निब के निर्माण में किया जाता है। चिकित्सा में, न केवल कृत्रिम सोने की मिश्र धातुओं का उपयोग किया जाता है, बल्कि विभिन्न प्रयोजनों के लिए सोने के लवण युक्त औषधीय तैयारी भी होती है, उदाहरण के लिए, तपेदिक के उपचार में। रेडियोधर्मी सोने का उपयोग घातक ट्यूमर के उपचार में किया जाता है। वैज्ञानिक अनुसंधान में, सोने का उपयोग धीमे न्यूट्रॉनों को पकड़ने के लिए किया जाता है। सोने के रेडियोधर्मी समस्थानिकों की सहायता से धातुओं और मिश्र धातुओं में प्रसार प्रक्रियाओं का अध्ययन किया जाता है।
इमारतों में खिड़की के शीशे के धातुकरण के लिए सोने का उपयोग किया जाता है। गर्म गर्मी के महीनों के दौरान, एक महत्वपूर्ण मात्रा में अवरक्त विकिरण इमारतों के कांच के शीशे से होकर गुजरता है। इन परिस्थितियों में, एक पतली फिल्म (0.13 माइक्रोन) अवरक्त विकिरण को दर्शाती है और कमरा अधिक ठंडा हो जाता है। यदि ऐसे कांच के माध्यम से एक धारा प्रवाहित की जाती है, तो यह कोहरे-विरोधी गुण प्राप्त कर लेगा। जहाजों, बिजली के इंजनों आदि के सोने से मढ़वाया दृष्टि चश्मा। वर्ष के किसी भी समय प्रभावी।
योजना।
सोने की सामान्य विशेषताएं।
रासायनिक गुण।
भौतिक और यांत्रिक गुण।
प्रकृति में सोना।
विज्ञान और प्रौद्योगिकी में सोने का उपयोग।
ग्रंथ सूची।
ग्रंथ सूची।
1. एन्युफ्रीवा एल.वी. एंटरटेनिंग केमिस्ट्री: ए बुक फॉर स्टूडेंट्स, टीचर्स एंड पेरेंट्स। मास्को एड. "एएसटी-प्रेस", 1994।
2. मनकेविच वी.ए. रसायन विज्ञान की मूल बातें। निर्देशिका। सेंट पीटर्सबर्ग, 1990
3. घर में पढ़ने के लिए स्टेपिन बीडी केमिस्ट्री की किताब। मास्को: रसायन विज्ञान, 1995।
4. टोकरेव बी.एन. रसायन शास्त्र के बारे में उत्सुक। मास्को एड. "रसायन विज्ञान", 1978
5. रासायनिक तत्वों का लोकप्रिय पुस्तकालय। ईडी। "विज्ञान" मास्को 1973
6. रसायन विज्ञान। विश्वकोश। वी। वोलोडिन द्वारा संपादित। मास्को 2000
सोना (रासायनिक तत्व) सोना (रासायनिक तत्व)
सोना (lat.Aurum )
, Au ("औरम" पढ़ें), परमाणु संख्या 79, परमाणु द्रव्यमान 196.9665 के साथ एक रासायनिक तत्व। यह प्राचीन काल से जाना जाता है। प्रकृति में, एक स्थिर आइसोटोप है, 197 Au। बाहरी और पूर्व-बाहरी इलेक्ट्रॉनिक बाड़ों का विन्यास 5 एस 2
पी 6
डी 10
6एसएक । समूह IВ में स्थित है और आवर्त सारणी के छठे आवर्त में, यह महान धातुओं से संबंधित है। ऑक्सीकरण 0, +1, +3, +5 (I, III, V से संयोजकता) बताता है।
सोने के परमाणु की धातु त्रिज्या 0.137 एनएम है, एयू + आयन की त्रिज्या समन्वय संख्या 6 के लिए 0.151 एनएम है, एयू 3+ आयन 0.084 एनएम है, और समन्वय संख्या 4 और 6 के लिए 0.099 एनएम है। आयनीकरण ऊर्जा Au 0 - Au + - Au 2+ - Au 3 + क्रमशः 9.23, 20.5 और 30.47 eV के बराबर हैं। पॉलिंग इलेक्ट्रोनगेटिविटी (सेमी।पोलिंग लिनुस) 2,4.
प्रकृति में होना
पृथ्वी की पपड़ी में सामग्री वजन से 4.3 · 10 -7% है, समुद्र और महासागरों के पानी में 5 · 10 -6% मिलीग्राम / लीटर से कम है। बिखरे हुए तत्वों को संदर्भित करता है। 20 से अधिक खनिज ज्ञात हैं, जिनमें से मुख्य एक देशी सोना (इलेक्ट्रम, कपरस, पैलेडियम, बिस्मथ सोना) है। बड़ी डली अत्यंत दुर्लभ हैं और आमतौर पर उनके व्यक्तिगत नाम होते हैं। सोने के रासायनिक यौगिक प्रकृति में दुर्लभ हैं, मुख्य रूप से टेलुराइड्स - केलवेराइट एयूटीई 2, क्रैनेराइट (एयू, एजी) ते 2, और अन्य। सोना विभिन्न सल्फाइड खनिजों में अशुद्धता के रूप में मौजूद हो सकता है: पाइराइट (सेमी।पाइराइट),
चलकोपीराइट (सेमी।हैलकोपाइराइट),
स्पैलेराइट (सेमी।स्पैलेराइट)और दूसरे।
रासायनिक विश्लेषण के आधुनिक तरीके पौधों और जानवरों के जीवों में, वाइन और कॉन्यैक में, खनिज पानी में और समुद्र के पानी में एयू की ट्रेस मात्रा की उपस्थिति का पता लगाना संभव बनाते हैं।
डिस्कवरी इतिहास
सोना प्राचीन काल से मानव जाति के लिए जाना जाता है। शायद यह पहली धातु थी जिससे कोई व्यक्ति मिला। प्राचीन मिस्र (4100-3900 ईसा पूर्व), भारत और इंडोचीन (2000-1500 ईसा पूर्व) में सोने के निष्कर्षण और उससे उत्पादों के निर्माण पर डेटा है, जहां से पैसे, महंगे गहने, काम किए गए थे। पंथ और कला .
प्राप्त
इसके औद्योगिक उत्पादन में सोने के स्रोत गोल्ड प्लेसर और प्राथमिक जमा के अयस्क और रेत हैं, जिनमें से सोने की सामग्री 5-15 ग्राम प्रति टन प्रारंभिक सामग्री के साथ-साथ मध्यवर्ती उत्पाद (0.5-3 ग्राम / टी) सीसा- जस्ता, तांबा, यूरेनियम और कुछ अन्य उद्योग।
प्लेसर से सोना प्राप्त करने की प्रक्रिया सोने और रेत के घनत्व के अंतर पर आधारित है। पानी के शक्तिशाली जेट की मदद से, कुचली हुई सोने की चट्टान को पानी में निलंबित अवस्था में स्थानांतरित कर दिया जाता है। परिणामी लुगदी एक झुकाव वाले विमान के साथ एक ड्रेज में बहती है। इस मामले में, सोने के भारी कण जम जाते हैं, और रेत के दाने पानी से बह जाते हैं।
दूसरे तरीके से, सोने को तरल पारा के साथ इलाज करके और एक तरल मिश्र धातु - अमलगम प्राप्त करके अयस्क से निकाला जाता है। फिर अमलगम को गर्म किया जाता है, पारा वाष्पित हो जाता है और सोना रह जाता है। अयस्कों से सोना निकालने के लिए साइनाइड विधि का भी उपयोग किया जाता है। इस मामले में, सोने के अयस्क का सोडियम साइनाइड NaCN समाधान के साथ इलाज किया जाता है। वायुमंडलीय ऑक्सीजन की उपस्थिति में, सोना विलयन में जाता है:
4Au + O 2 + 8NaCN + 2H 2 O = 4Na + 4NaOH
इसके बाद, गोल्ड कॉम्प्लेक्स के परिणामी घोल को जिंक डस्ट से उपचारित किया जाता है:
2Na + Zn = Na 2 + NO + H 2 O
इसके बाद विलयन से सोने का चयनात्मक अवक्षेपण होता है, उदाहरण के लिए, FeSO4 का उपयोग करना।
भौतिक और रासायनिक गुण
सोना एक पीली धातु है जिसमें घन फलक-केंद्रित जाली होती है ( ए= 0.40786 एनएम)। गलनांक 1064.4 डिग्री सेल्सियस, क्वथनांक 2880 डिग्री सेल्सियस, घनत्व 19.32 किग्रा / डीएम 3. असाधारण प्लास्टिसिटी, तापीय चालकता और विद्युत चालकता रखता है। 1 मिमी के व्यास के साथ सोने की एक गेंद को 50 मीटर 2 के क्षेत्र के साथ सबसे पतली शीट, पारभासी नीले-हरे रंग में चपटा किया जा सकता है। सोने की सबसे पतली पत्तियों की मोटाई 0.1 माइक्रोन होती है। सोने से बेहतरीन धागे निकाले जा सकते हैं।
सोना हवा और पानी में स्थिर है। ऑक्सीजन के साथ (सेमी।ऑक्सीजन), नाइट्रोजन (सेमी।नाइट्रोजन)हाइड्रोजन (सेमी।हाइड्रोजन), फास्फोरस (सेमी।फास्फोरस), सुरमा (सेमी।सुरमा)और कार्बन (सेमी।कार्बन)सीधे तौर पर बातचीत नहीं करता है। एंटीमोनाइड AuSb 2 और गोल्ड फॉस्फाइड Au 2 P 3 अप्रत्यक्ष रूप से प्राप्त होते हैं।
मानक क्षमता की श्रृंखला में, सोना हाइड्रोजन के दाईं ओर स्थित है, इसलिए, यह गैर-ऑक्सीकरण एसिड के साथ प्रतिक्रिया नहीं करता है। गर्म सेलेनिक एसिड में घुल जाता है:
2Au + 6H 2 SeO 4 = Au 2 (SeO 4) 3 + 3H 2 SeO 3 + 3H 2 O,
क्लोरीन के घोल से गुजरते समय सांद्र हाइड्रोक्लोरिक एसिड में:
2Au + 3Cl 2 + 2HCl = 2H
परिणामी घोल के सावधानीपूर्वक वाष्पीकरण पर, हाइड्रोक्लोरिक एसिड HAuCl 4 3H 2 O के पीले क्रिस्टल प्राप्त किए जा सकते हैं।
हलोजन के साथ (सेमी।हलोजन)गर्म किए बिना, नमी की अनुपस्थिति में, सोना प्रतिक्रिया नहीं करता है। जब सोने के पाउडर को हैलोजन या क्सीनन डिफ्लुओराइड के साथ गर्म किया जाता है, तो सोने के हैलाइड बनते हैं:
2Au + 3Cl 2 = 2AuCl 3,
2Au + 3XeF 2 = 2AuF 3 + 3Xe
केवल AuCl 3 और AuBr 3 पानी में घुलनशील हैं, जिसमें डिमेरिक अणु होते हैं:
हेक्साफ्लोरोएरेट्स (वी) का थर्मल अपघटन, उदाहरण के लिए, ओ 2 + - प्राप्त सोने के फ्लोराइड एयूएफ 5 और एयूएफ 7। वे सोने या उसके ट्राइफ्लोराइड को KrF 2 और XeF 6 के साथ ऑक्सीकृत करके भी प्राप्त किए जा सकते हैं।
सोने के मोनोहैलाइड्स AuCl, AuBr, और AuI तब बनते हैं जब संगत उच्च हैलाइडों को निर्वात में गर्म किया जाता है। गर्म होने पर, वे या तो विघटित हो जाते हैं:
2AuCl = 2Au + Cl 2
या अनुपातहीन:
3एयूबीआर = एयूबीआर 3 + 2एयू।
सोने के यौगिक अस्थिर होते हैं और जलीय घोल में हाइड्रोलाइज होते हैं, आसानी से धातु में कम हो जाते हैं।
H के घोल में क्षार या Mg (OH) 2 मिलाने पर सोना (III) हाइड्रॉक्साइड Au (OH) 3 बनता है:
एच + 2 एमजी (ओएच) 2 = एयू (ओएच) 3 Ї + 2 एमजीसीएल 2 + एच 2 ओ
गर्म होने पर, Au (OH) 3 आसानी से निर्जलित हो जाता है, जिससे सोना (III) ऑक्साइड बनता है:
2Au (OH) 3 = Au 2 O 3 + 3H 2 O
सोना (III) हाइड्रॉक्साइड अम्ल और क्षार के विलयन के साथ अभिक्रिया करके उभयधर्मी गुण प्रदर्शित करता है:
एयू (ओएच) 3 + 4 एचसीएल = एच + 3 एच 2 ओ,
Au (OH) 3 + NaOH = Na
सोने के अन्य ऑक्सीजन यौगिक अस्थिर होते हैं और आसानी से विस्फोटक मिश्रण बनाते हैं। अमोनिया Au 2 O 3 · 4NH 3 - "विस्फोटक सोना" के साथ सोना (III) ऑक्साइड का यौगिक गर्म होने पर फट जाता है।
जब सोने को उसके लवणों के तनु विलयनों से अपघटित किया जाता है, साथ ही जब सोने को विद्युत रूप से पानी में छिड़का जाता है, तो सोने का एक स्थिर कोलॉइडी विलयन बनता है:
2AuCl 3 + 3SnCl 2 = 3SnCl 4 + 2Au
सोने के कोलॉइडी विलयनों का रंग सोने के कणों के फैलाव की मात्रा और उनकी सघनता की तीव्रता पर निर्भर करता है। विलयन में सोने के कण सदैव ऋणावेशित होते हैं।
आवेदन
सोने और उसके मिश्र धातुओं का उपयोग गहने, सिक्के, पदक, कृत्रिम अंग, रासायनिक उपकरण के पुर्जे, विद्युत संपर्क और तार, माइक्रोइलेक्ट्रॉनिक उत्पादों के निर्माण के लिए, रासायनिक उद्योग में पाइपों पर क्लैडिंग के लिए, सोल्डर, उत्प्रेरक, घड़ियों के उत्पादन में किया जाता है। चश्मा रंगना, फाउंटेन पेन के लिए पंख बनाना, धातु की सतहों पर कोटिंग करना। आमतौर पर, चांदी या पैलेडियम (सफेद सोना, जिसे प्लैटिनम और अन्य धातुओं के साथ सोने का मिश्र धातु भी कहा जाता है) के साथ मिश्र धातु में सोने का उपयोग किया जाता है। मिश्र धातु में सोने की सामग्री को राज्य चिह्न द्वारा निर्दिष्ट किया जाता है। सोना 583 परख मूल्य वजन के हिसाब से 58.3% सोने के साथ एक मिश्र धातु है। यह भी देखें सोना (अर्थशास्त्र में) (सेमी।सोना (अर्थव्यवस्था में)).
शारीरिक क्रिया
कुछ सोने के यौगिक विषाक्त होते हैं, गुर्दे, यकृत, प्लीहा और हाइपोथैलेमस में जमा हो जाते हैं, जिससे कार्बनिक रोग और जिल्द की सूजन, स्टामाटाइटिस, थ्रोम्बोसाइटोपेनिया हो सकता है।
विश्वकोश शब्दकोश. 2009 .
देखें कि "सोना (रासायनिक तत्व)" अन्य शब्दकोशों में क्या है:
एक रासायनिक तत्व समान परमाणु आवेश और प्रोटॉन की संख्या वाले परमाणुओं का एक समूह है, जो आवर्त सारणी में क्रमसूचक (परमाणु) संख्या के साथ मेल खाता है। प्रत्येक रासायनिक तत्व का अपना नाम और प्रतीक होता है, जो ... ... विकिपीडिया . में दिया गया है
पैलेडियम (लैटिन पैलेडियम, सबसे बड़े क्षुद्रग्रहों में से एक के नाम पर पल्लास), पीडी (पढ़ें "पैलेडियम"), परमाणु संख्या 46 के साथ एक रासायनिक तत्व, परमाणु द्रव्यमान 106.42। प्राकृतिक पैलेडियम में छह स्थिर आइसोटोप होते हैं 102Pd (1.00%), 104Pd ... ... विश्वकोश शब्दकोश
- (फ्रेंच क्लोर, जर्मन क्लोर, इंग्लिश क्लोरीन) हैलोजन के समूह का एक तत्व; सीएल पर हस्ताक्षर करें; परमाणु भार 35.451 [स्टास डेटा की क्लार्क की गणना के अनुसार] ओ = 16 पर; कण Cl 2, जो ...... के संबंध में बन्सन और रेग्नॉल्ट द्वारा पाए गए घनत्वों से अच्छी तरह मेल खाता है।
- (केम।; फॉस्फोर फ्रेंच।, फॉस्फोर जर्मन।, फॉस्फोरस इंग्लिश। और लैट।, जहां से पदनाम पी, कभी-कभी पीएच; परमाणु भार 31 [आधुनिक समय में, एफ का परमाणु भार पाया जाता है। (वैन डेर प्लाट्स) इस प्रकार है : 30.93 एफ धातु के एक निश्चित वजन के साथ बहाली द्वारा ... ... एनसाइक्लोपीडिक डिक्शनरी ऑफ एफ.ए. ब्रोकहॉस और आई.ए. एफ्रोन
- (अर्जेंटीना, अर्जेन्ट, सिलबर), रसायन। एजी मार्क। एस प्राचीन काल में मनुष्य को ज्ञात धातुओं में से एक है। प्रकृति में, यह अपनी मूल अवस्था में और अन्य निकायों के साथ यौगिकों के रूप में होता है (सल्फर के साथ, उदाहरण के लिए, Ag 2S ... ... एनसाइक्लोपीडिक डिक्शनरी ऑफ एफ.ए. ब्रोकहॉस और आई.ए. एफ्रोन
- (अर्जेंटीना, अर्जेन्ट, सिलबर), रसायन। एजी मार्क। एस प्राचीन काल में मनुष्य को ज्ञात धातुओं में से एक है। प्रकृति में, यह अपनी मूल अवस्था में और अन्य निकायों के साथ यौगिकों के रूप में होता है (सल्फर के साथ, उदाहरण के लिए Ag2S चांदी ... एनसाइक्लोपीडिक डिक्शनरी ऑफ एफ.ए. ब्रोकहॉस और आई.ए. एफ्रोन
- (प्लेटिन फ्र।, प्लेटिना या उम अंग्रेजी, प्लेटिन जर्मन; पं = 194.83, यदि ओ = 16 के। सीबर्ट के अनुसार)। पी. आमतौर पर अन्य धातुओं के साथ होता है, और इन धातुओं में से जो उनके रासायनिक गुणों में इसके निकट होते हैं उन्हें कहा जाता है ... ... एनसाइक्लोपीडिक डिक्शनरी ऑफ एफ.ए. ब्रोकहॉस और आई.ए. एफ्रोन
यू (यूरेन, यूरेनियम; ओ = 16 परमाणु भार यू = 240 पर) उच्चतम परमाणु भार वाला तत्व; परमाणु भार के अनुसार सभी तत्वों को हाइड्रोजन और यूरेनियम के बीच रखा जाता है। यह आवधिक प्रणाली के समूह के धातु उपसमूह VI का सबसे कठिन सदस्य है (देखें क्रोमियम, ... ... एनसाइक्लोपीडिक डिक्शनरी ऑफ एफ.ए. ब्रोकहॉस और आई.ए. एफ्रोन
- (ब्रोमम; रासायनिक रूप। Br, परमाणु भार 80) गैर-धातु तत्व, हैलोजन के समूह से, 1826 में फ्रांसीसी रसायनज्ञ बलार्ड द्वारा समुद्री जल लवण के मातृ समाधान में खोजा गया था; B. का नाम ग्रीक शब्द Βρωμος stench से मिला है। ... ... एनसाइक्लोपीडिक डिक्शनरी ऑफ एफ.ए. ब्रोकहॉस और आई.ए. एफ्रोन
सोना धन और धूप का प्रतीक है, जो मनुष्य को ज्ञात सबसे पुरानी धातु है। प्राचीन लोगों के अधिक व्यावहारिक कांस्य और लोहे से परिचित होने से बहुत पहले सोने के गहने बनने लगे। इस धातु को बनाने के लिए कीमियागर व्यर्थ थे, और मानव जाति ने आकर्षक प्रकाश से चमकने वाली पीली धातु के टुकड़ों के लिए बहुत खून बहाया। लेकिन यह मूल रूप से क्या है?
सोने के बारे में सामान्य जानकारी
शुद्ध सोना एक भारी धातु है, जिसमें सिल्लियों के रूप में उच्च तन्यता और तन्यता के गुण होते हैं। सोने के भौतिक गुण केवल एक ग्राम पदार्थ से 2 किमी लंबा तार बनाना संभव बनाते हैं। सोने का उपयोग इस तथ्य के कारण बहुत व्यापक है कि यह धातु गर्मी और बिजली का संचालन अच्छी तरह से करती है, लेकिन यह ऑक्सीकरण नहीं करती है और व्यावहारिक रूप से अन्य पदार्थों के साथ प्रतिक्रिया नहीं करती है।
सोने के अणु हवा और पानी में वितरित होते हैं, मिट्टी में और कुछ पौधों में बहुत कम मात्रा में (विशेष रूप से, मकई में) जमा होते हैं।यह धातु शायद ही कभी अन्य रासायनिक तत्वों के साथ खनिज बनाती है, जो मुख्य रूप से मिट्टी में सोने की डली या सुनहरी रेत के रूप में पाई जाती है। औद्योगिक महत्व के गोल्ड प्लेसर वर्तमान में 41 देशों में पाए जाते हैं, और सबसे बड़ा सोना जमा दक्षिण अफ्रीका, कनाडा और सीआईएस देशों में स्थित है।
सोने का खनन मुख्य रूप से समामेलन विधि द्वारा प्लेसर से किया जाता है।
एक चट्टान से शुद्ध सोना प्राप्त करने के लिए, इसे पहले कुचल और लाभकारी होना चाहिए, और फिर खारा समाधान (आमतौर पर सोडियम साइनाइड या पोटेशियम साइनाइड का उपयोग किया जाता है) के साथ इलाज किया जाना चाहिए। उसके बाद, सोने को जिंक के घोल के साथ अवक्षेपित किया जाता है और बाद में इलेक्ट्रोलिसिस द्वारा शुद्ध सोना प्राप्त किया जाता है।
पहले, सोने की सॉल्वेंसी और सोने के मानक की अवधारणा के कारण बहुत आर्थिक महत्व था - यानी। सोने पर निर्भर किसी भी वस्तु के मूल्य का माप। सोने के मानक का परित्याग इस तथ्य के कारण वैश्विक अर्थव्यवस्था के लिए एक बड़ा कदम था, जैसा कि पहले ही उल्लेख किया गया है, सोना एक बहुत ही नरम धातु है जो ऑपरेशन के दौरान विरूपण और घर्षण के लिए अतिसंवेदनशील है। इस धातु के छोटे भंडार और इसके व्यापक तकनीकी उपयोग के कारण आज सोना निवेश की वस्तु है।
 उद्योग में, सोने का उपयोग अक्सर कंडक्टर और विद्युत संपर्कों के रूप में किया जाता है। इसके अलावा, सोने का उपयोग परमाणु उद्योग में, निर्माण में (खिड़की के शीशे के लिए एक कोटिंग के रूप में), धातु विज्ञान, कॉस्मेटोलॉजी और यहां तक कि खाद्य उद्योग में भी जाना जाता है। इसके अलावा, सोने के रेडियोधर्मी समस्थानिकों का उपयोग कैंसर के इलाज के लिए किया जाता है। लेकिन सोने के लिए सबसे लोकप्रिय उपयोग, निश्चित रूप से, आभूषण उद्योग में है।
उद्योग में, सोने का उपयोग अक्सर कंडक्टर और विद्युत संपर्कों के रूप में किया जाता है। इसके अलावा, सोने का उपयोग परमाणु उद्योग में, निर्माण में (खिड़की के शीशे के लिए एक कोटिंग के रूप में), धातु विज्ञान, कॉस्मेटोलॉजी और यहां तक कि खाद्य उद्योग में भी जाना जाता है। इसके अलावा, सोने के रेडियोधर्मी समस्थानिकों का उपयोग कैंसर के इलाज के लिए किया जाता है। लेकिन सोने के लिए सबसे लोकप्रिय उपयोग, निश्चित रूप से, आभूषण उद्योग में है।
सोने के नमूनों की अवधारणा
सोने की सुंदरता एक संकेतक है जो एक नमूने में शुद्ध सोने की मात्रा को दर्शाता है। फिलहाल, मीट्रिक और कैरेट नमूना पदनाम प्रणाली का उपयोग किया जाता है। मीट्रिक प्रणाली प्रति 1000 इकाई पदार्थ में सोने की मात्रा की गणना पर आधारित है, और कैरेट प्रणाली 24 इकाइयों पर आधारित है। स्पूल सैंपल सिस्टम भी था, जो अब पुराना हो चुका है। उसने 96 इकाइयों की दर से शुद्ध पदार्थ को मापने के लिए एक प्रणाली का इस्तेमाल किया।
 ऐसा लगता है कि शुद्ध सोना हर तरह से सबसे मूल्यवान है और इसके लिए आपको गहनों का एक टुकड़ा चुनते समय लड़ने की जरूरत है।हालांकि, सजावटी उद्देश्यों की पूर्ति के लिए 24 कैरेट सोने का घनत्व बहुत कम है। अपने शुद्ध रूप में, यह धातु बहुत नरम है, और इसे पहनना असंभव होगा - यह तुरंत विकृत हो जाएगा। ऐसे नमूनों का उपयोग तकनीकी उद्देश्यों के लिए किया जाता है - इलेक्ट्रोड प्राप्त करने के लिए, दवा या अन्य उद्योगों के लिए कच्चा माल, संदर्भ सिल्लियां आदि के रूप में।
ऐसा लगता है कि शुद्ध सोना हर तरह से सबसे मूल्यवान है और इसके लिए आपको गहनों का एक टुकड़ा चुनते समय लड़ने की जरूरत है।हालांकि, सजावटी उद्देश्यों की पूर्ति के लिए 24 कैरेट सोने का घनत्व बहुत कम है। अपने शुद्ध रूप में, यह धातु बहुत नरम है, और इसे पहनना असंभव होगा - यह तुरंत विकृत हो जाएगा। ऐसे नमूनों का उपयोग तकनीकी उद्देश्यों के लिए किया जाता है - इलेक्ट्रोड प्राप्त करने के लिए, दवा या अन्य उद्योगों के लिए कच्चा माल, संदर्भ सिल्लियां आदि के रूप में।
सोने की उच्च लचीलापन का एक उत्कृष्ट संकेतक प्रतिष्ठित "दांत के लिए परीक्षण" इशारा है। प्राचीन समय में, जब सोने के सिक्कों को अपेक्षाकृत उच्च शुद्धता की डली से ढाला जाता था, सिक्कों के काटने से शुद्ध धातु को तांबे के साथ मिश्र धातु से अलग करना संभव हो जाता था - एक असली सिक्के पर एक दांत का निशान बना रहता था, जबकि तांबे से जुड़े सिक्के लगभग असंभव थे। इस तरह से नुकसान।
गहनों में, 56 सोने का उपयोग अक्सर पुरानी प्रणाली के अनुसार किया जाता है, या आधुनिक के अनुसार 14 कैरेट का। इसके लिए, मिश्र धातुओं को विभिन्न अलौह धातुओं से बनाया जाता है, जो इस बात पर निर्भर करता है कि अंतिम मिश्र धातु में अलग-अलग कठोरता, फ्यूज़िबिलिटी, रंग, चमक और अन्य विशेषताएं हैं।
उदाहरण के लिए, सफेद सोना विभिन्न अनुपातों में निकल, जस्ता, पैलेडियम, चांदी या तांबे की अशुद्धियों को मिलाकर बनाया जाता है। सोने का गुलाबी रंग चांदी, पैलेडियम और तांबे के मिश्रण से दिया जाता है। तांबे और चांदी का मिश्रण एक आकर्षक लाल रंग बनाता है। इसके अलावा, रोडियम चढ़ाना धातु को चमकदार और ठंडा रंग देता है, जिसका उपयोग उत्पाद की ताकत बढ़ाने के लिए भी किया जाता है।
 सोने का घनत्व 19.32 g/cm³ है। यह सोने को बहुत भारी धातु बनाता है, जो शुद्ध सजावटी उद्देश्यों के लिए भी अवांछनीय है। हालांकि, सोने का इतना अधिक घनत्व इसके निष्कर्षण के कार्य को बहुत आसान बना देता है, क्योंकि फ्लशिंग के दौरान यह पहले से ही हल्की धातुओं, चट्टानों और खनिजों से अलग हो जाता है। सोने का विशिष्ट गुरुत्व लगभग 197 g/mol है। सोने की रासायनिक संरचना शुद्ध धातु के अणु होते हैं जो एक घन क्रिस्टल जाली से जुड़े होते हैं।
सोने का घनत्व 19.32 g/cm³ है। यह सोने को बहुत भारी धातु बनाता है, जो शुद्ध सजावटी उद्देश्यों के लिए भी अवांछनीय है। हालांकि, सोने का इतना अधिक घनत्व इसके निष्कर्षण के कार्य को बहुत आसान बना देता है, क्योंकि फ्लशिंग के दौरान यह पहले से ही हल्की धातुओं, चट्टानों और खनिजों से अलग हो जाता है। सोने का विशिष्ट गुरुत्व लगभग 197 g/mol है। सोने की रासायनिक संरचना शुद्ध धातु के अणु होते हैं जो एक घन क्रिस्टल जाली से जुड़े होते हैं।
सोने की प्रामाणिकता का निर्धारण कैसे करें?
यह आश्चर्य की बात नहीं है कि सोने जैसे मूल्यवान और उपयोगी खनिज का उपयोग सभी प्रकार की धोखाधड़ी योजनाओं में किया जा रहा है। हालांकि, ज्यादातर मामलों में सोने के गुण कुछ सरल जोड़तोड़ के साथ एक कीमती धातु को नकली से अलग करना संभव बनाते हैं। हालांकि, किसी को तुरंत एक आरक्षण करना चाहिए कि हम शुद्ध सोने के निर्धारण के बारे में बात करेंगे, उदाहरण के लिए, मिश्र धातु, ताकि इन तरीकों से केवल सिल्लियों की प्रामाणिकता निर्धारित करना संभव हो सके। गहनों में कितने प्रतिशत सोना है इसका खुलासा नहीं किया जा सकता है।
 सबसे पहले, यह याद रखना चाहिए कि एयू तत्व चुंबकीय नहीं है।इसलिए चुम्बक से जाँच करने पर शुद्ध सोना उसकी ओर आकर्षित नहीं होना चाहिए। यदि चुंबक हाथ में नहीं है, तो आप रासायनिक रूप से सोने का परीक्षण कर सकते हैं। उत्पाद के कम से कम दिखाई देने वाले क्षेत्र का चयन करें और उस पर कुछ मिनट के लिए आयोडीन की एक छोटी बूंद छोड़ दें, फिर इसे मिटा दें। शुद्ध सोना एक गहरा निशान छोड़ेगा।
सबसे पहले, यह याद रखना चाहिए कि एयू तत्व चुंबकीय नहीं है।इसलिए चुम्बक से जाँच करने पर शुद्ध सोना उसकी ओर आकर्षित नहीं होना चाहिए। यदि चुंबक हाथ में नहीं है, तो आप रासायनिक रूप से सोने का परीक्षण कर सकते हैं। उत्पाद के कम से कम दिखाई देने वाले क्षेत्र का चयन करें और उस पर कुछ मिनट के लिए आयोडीन की एक छोटी बूंद छोड़ दें, फिर इसे मिटा दें। शुद्ध सोना एक गहरा निशान छोड़ेगा।
आप सोने और सिरके की जांच कर सकते हैं। धातु के एक टुकड़े को सिरके में कुछ मिनट के लिए भिगो दें। यदि सोना काला पड़ने लगे तो वह किसी अन्य धातु की मिश्रधातु है, क्योंकि शुद्ध सोना एसिटिक एसिड के साथ प्रतिक्रिया नहीं करता है।
सोने की सुंदरता का निर्धारण करने के लिए, आपको एक जौहरी के पास जाना होगा। परीक्षण विभिन्न तरीकों से किया जाता है, जिनमें से सबसे लोकप्रिय सोने की सुइयों का उपयोग है।
सत्यापन में परीक्षण के तहत सामग्री के लिए नमूना (सुई) के सोने के घनत्व की तुलना करना शामिल है। यदि सुई में सोने की मात्रा अधिक है, तो यह उत्पाद की सतह पर कोई निशान नहीं छोड़ेगा, क्योंकि मिश्र धातुओं की तुलना में सोने का घनत्व कम होता है।
इसके अलावा, आभूषण कार्यशालाओं में बिना किसी खरोंच के सोने के नमूनों का विश्लेषण किया जाता है। डिवाइस में समाधान और उनके बाद के विश्लेषण का उपयोग करके या एक्स-रे का उपयोग करके नमूने की एक हार्डवेयर जांच होती है, जिसका उपयोग केवल अपेक्षाकृत बड़ी प्रयोगशालाओं में ही संभव है। यह सुनिश्चित करने के लिए एक्स-रे की आवश्यकता होती है कि सोने की सलाखों में कोई अन्य धातु कोर न हो।
 पाए गए सोने की डली और अन्य बड़े नमूनों की जांच परख विश्लेषण द्वारा की जाती है। यह विधि छोटी वस्तुओं के लिए उपयुक्त नहीं है, क्योंकि इसके लिए कुछ बलिदानों की आवश्यकता होती है - नमूने के एक टुकड़े को पिघलाना चाहिए और फिर सीसा और चांदी के साथ मिला देना चाहिए। उसके बाद, द्रव्यमान और मात्रा की गणना की जाती है, जिससे शुद्ध सोने के अनुपात की गणना की जाती है।
पाए गए सोने की डली और अन्य बड़े नमूनों की जांच परख विश्लेषण द्वारा की जाती है। यह विधि छोटी वस्तुओं के लिए उपयुक्त नहीं है, क्योंकि इसके लिए कुछ बलिदानों की आवश्यकता होती है - नमूने के एक टुकड़े को पिघलाना चाहिए और फिर सीसा और चांदी के साथ मिला देना चाहिए। उसके बाद, द्रव्यमान और मात्रा की गणना की जाती है, जिससे शुद्ध सोने के अनुपात की गणना की जाती है।
आधुनिक धोखेबाज निष्क्रिय अशुद्धियों के साथ सोने की मिश्र धातु बनाते हैं, इसलिए इस तरह के नकली तरीके पुराने सोने के नमूनों पर अधिक काम करते हैं।इसके अलावा, घरेलू प्रयोग एक विश्वसनीय परिणाम दिए बिना गहनों को नुकसान पहुंचा सकते हैं, इसलिए यह बेहतर है, यदि आवश्यक हो, तो धातु की शुद्धता का निर्धारण करने के लिए, ऐसे पेशेवरों से संपर्क करें जो नमूने की प्रामाणिकता की जल्दी और सुरक्षित रूप से पुष्टि कर सकें।