MINISTERIO DE SALUD DE LA FEDERACIÓN DE RUSIA
AUTORIZACIÓN DE FARMACOPIAS
ginsengpresenteraícesFS.2.5.0013.15
Panacis ginseng base en lugar de GFXI, tema. 2, arte. 66
Recolectado a fines de agosto - principios de septiembre y raíces secas de una hierba perenne cultivada y silvestre de ginseng real - Panax ginseng C. A. mey, familia araliáceas - araliáceas.
AUTENTICIDAD
Signos externos. Materia prima entera. Raíces de hasta 25 cm de largo, 0,7 a 2,5 cm de espesor, con 2 a 5 ramas grandes, con menos frecuencia sin ellas. Las raíces están arrancadas, longitudinalmente, rara vez arrugadas en espiral, quebradizas, la fractura es uniforme. El "cuerpo" de la raíz está engrosado, casi cilíndrico, desde arriba con engrosamientos anulares claramente expresados. En la parte superior de la raíz hay un rizoma arrugado transversalmente estrecho: el "cuello". El rizoma es corto con varias cicatrices de tallos caídos, en la parte superior forma una “cabeza”, que es un remanente de tallo extendido y una yema apical (a veces 2-3). Una o más raíces adventicias a veces parten del "cuello". Puede que falten el "cuello" y la "cabeza". El color de las raíces desde la superficie y en el corte es blanco amarillento, en una fractura fresca es blanco. El olor es específico. El sabor del extracto de agua es dulce, ardiente y luego picante-amargo.
materias primas trituradas. Al examinar las materias primas trituradas bajo una lupa (10×) o un microscopio estereoscópico (16×), se ven trozos de raíces de varias formas, que pasan a través de un tamiz con orificios de 7 mm. El color en la superficie y en la rotura es blanco amarillento. El olor es específico. El sabor del extracto de agua es dulce, ardiente y luego picante-amargo.
Polvo. Al examinar el polvo con una lupa (10x) o un microscopio estereoscópico (16x), se ve una mezcla de partículas trituradas de raíces de varias formas de color blanco amarillento, que pasan a través de un tamiz con orificios de 2 mm. El olor es específico. El sabor del extracto de agua es dulce, ardiente y luego picante-amargo.
signos microscópicos. Materia prima entera. En la sección transversal de la raíz principal, se ven una capa estrecha de corcho de color marrón claro, una corteza ancha, una línea clara de cambium y madera.
La raíz principal está cubierta de peridermis, cuyas células son de paredes delgadas y lignificadas, no corchosas. El floema y el xilema están separados por la zona cambial, que pasa aproximadamente por la mitad del radio de la raíz y
a veces no se ve. A la periferia del xilema primario parten rayos radiales primarios de células grandes del tejido parenquimatoso, entre los cuales hay un xilema secundario, atravesado por numerosos rayos radiales secundarios del parénquima principal. El xilema consiste en células parenquimatosas de paredes delgadas que contienen granos de almidón. Los vasos de los radios medulares tienen paredes lignificadas engrosadas y están ubicados solos o reunidos en grupos de 3-6. En el parénquima de la madera se encuentran ocasionalmente células que contienen pigmentos amarillos. En el centro de la raíz se diagnostican indistintamente remanentes de xilema primario en forma de 2 radios. El floema se compone principalmente de elementos de células pequeñas, contiene receptáculos esquizogénicos bien marcados que contienen gotitas de secreción de color amarillo claro a marrón rojizo. Los granos de almidón son pequeños, redondos, simples. Algunas células del parénquima contienen drusas de oxalato de calcio. La parte externa de la corteza secundaria limita con una zona de varias (4 a 6) filas de grandes células felodérmicas parenquimatosas tangencialmente alargadas, redondas u ovaladas, con una membrana ligeramente engrosada.
|
|
||
|
|
|
|
|
|
|
|
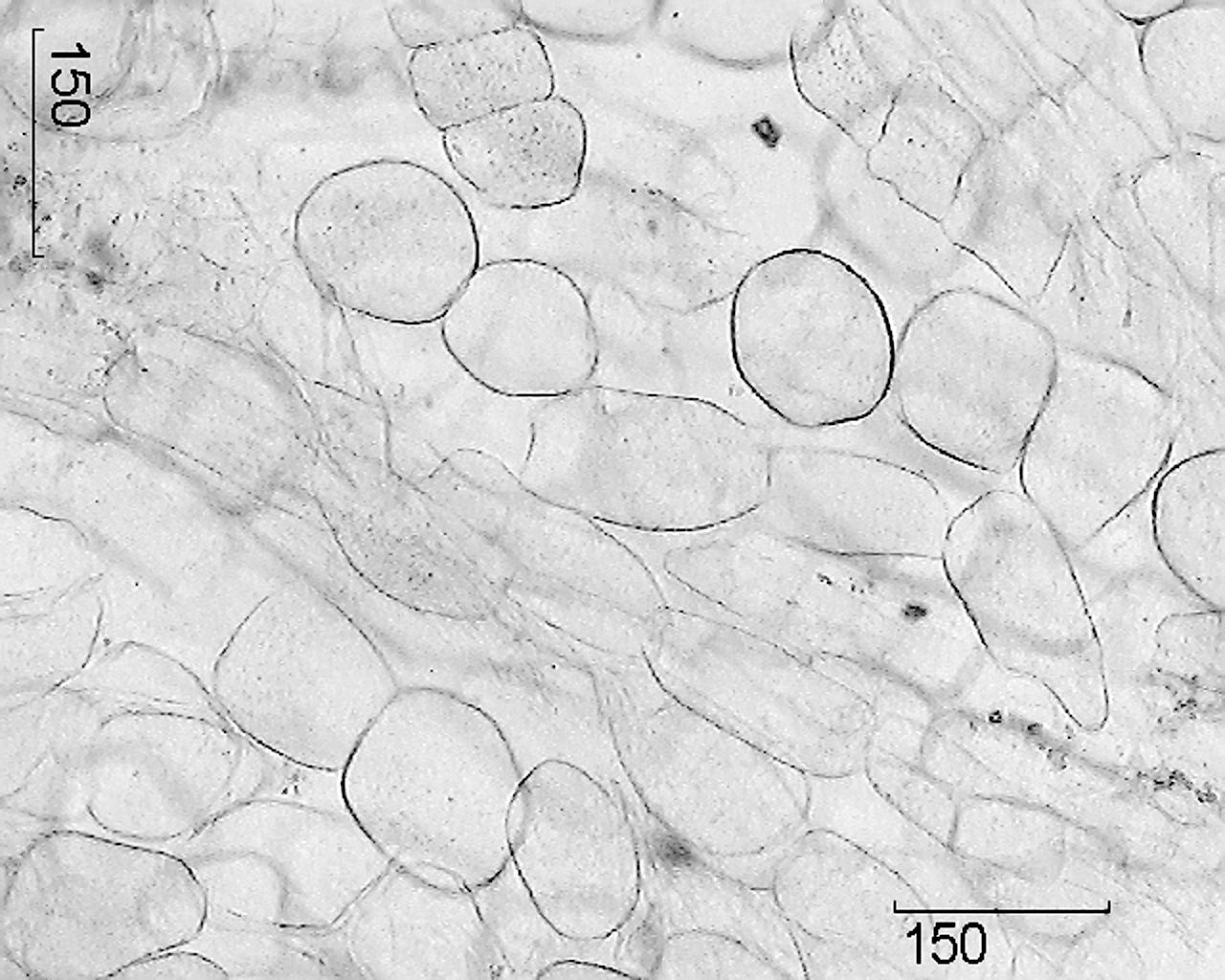
Figura - Raíces presentes de Ginseng.
1 – fragmento de una sección transversal de la raíz principal (100×); 2 – fragmento de corcho (400×); 3 - fragmento de una sección transversal de una raíz adventicia: a - vasos de xilema, b - granos de almidón (400×); 4 - un fragmento de una sección transversal de la raíz principal con un canal secretor: a - células de revestimiento del canal, b - cavidad del canal (400×); 5 - fragmento del parénquima de los radios medulares: a - drusas de oxalato de calcio, b - granos de almidón (400×); 6 - células del parénquima del radio medular (100×).
En la sección transversal de la raíz adventicia en el centro, el rayo de vasos del xilema primario es el remanente del haz vascular diarch en la estructura primaria. Los dos sectores del xilema secundario están separados por rayos radiales del parénquima principal. Las células del parénquima son redondas u ovaladas, parcial o completamente llenas de granos de almidón. El corcho consta de 5 a 7 capas de células rectangulares, de paredes delgadas y débilmente lignificadas.
materias primas trituradas. Al examinar una preparación triturada, deben verse fragmentos de secciones transversales y longitudinales de las raíces principales y adventicias.
Los fragmentos de la raíz principal están representados por rayos de xilema y vasos que llenan las células del parénquima de los rayos medulares con granos de almidón, cavidades del canal y células de revestimiento, células del parénquima con pigmentos y células cambiales.
Los fragmentos de raíces adventicias están representados por células de corcho, parénquima con granos de almidón, receptáculos, corteza primaria y secundaria, vasos, rayos medulares.
Polvo. Al examinar la micropreparación, se ven fragmentos de epidermis, corcho, madera, parénquima y drusas de oxalato de calcio.
Determinación de los principales grupos de sustancias biológicamente activas
Cromatografía de capa fina
En la línea de salida de una placa cromatográfica analítica con una capa de gel de sílice con indicador fluorescente de 10 × 15 cm sobre un sustrato de aluminio, aplicar 20 μl de la solución de prueba (ver sección "Determinación cuantitativa" preparación de la solución A de la prueba solución) y 50 μl de la solución de muestra estándar (RS) de panaxoside Rg 1 (consulte la sección "Determinación cuantitativa" preparación de la solución A CO de panaxoside Rg 1). La placa con las muestras aplicadas se seca al aire, se coloca en cámara, se satura preliminarmente por al menos 2 h con una mezcla de solventes cloroformo - metanol - agua (26:14:3), y se cromatografía en forma ascendente. Cuando el frente de solvente pasa alrededor del 80 - 90% de la longitud de la placa desde la línea de salida, se retira de la cámara, se seca para eliminar trazas de solventes, se trata con ácido fosfotúngstico con una solución de alcohol al 20% y se calienta en un horno a 100 - 105 ºC durante 3 minutos, después de lo que se ve a la luz del día.
El cromatograma de la solución de prueba debe mostrar al menos 6 zonas de adsorción de rosa claro a rosa oscuro; la zona dominante está al nivel de la zona del cromatograma de la solución de CO de panaxósido Rg 1 ; se permite la detección de otras zonas de adsorción.
Cuando se aplica una gota de ácido sulfúrico concentrado al polvo de raíces de ginseng, después de 1-2 minutos, aparece un color rojo ladrillo, que se convierte en rojo violeta y luego en violeta (panaxósidos).
Pruebas
Humedad. toda la materia prima, materia prima triturada, polvo - no más del 13%.
La ceniza es común. toda la materia prima, materia prima triturada, polvo - no más del 5%.
Ceniza insoluble en ácido clorhídrico. toda la materia prima, materia prima triturada, polvo - no más del 2%.
Finura de las materias primas.Toda la materia prima: partículas que pasan a través de un tamiz con orificios de 3 mm, no más del 5%. Materias primas trituradas: partículas que no pasan por un tamiz con orificios de 7 mm, no más del 5%; partículas que pasan a través de un tamiz con orificios de 0,5 mm, no más del 5%. Polvo: partículas que no pasan a través de un tamiz con orificios de 2 mm de tamaño, no más del 5%; partículas que pasan a través de un tamiz con orificios de 0,18 mm de tamaño, no más del 5%.
Asunto extranjero
Raíces oscurecidas desde la superficie. . toda la materia prima, materia prima triturada no más del 3%.
impureza orgánica. toda la materia prima, materia prima triturada no más del 0,5%.
impureza mineral . Materias primas enteras, materias primas trituradas, polvo - no más del 1%.
Metales pesados. De acuerdo con los requisitos de la Monografía de Farmacopea General "Determinación del contenido de metales pesados y arsénico en materias primas de hierbas medicinales y preparaciones de hierbas medicinales".
radionucleidos. De acuerdo con los requisitos de la Monografía de Farmacopea General "Determinación del contenido de radionucleidos en materias primas de hierbas medicinales y preparaciones de hierbas medicinales".
Cantidades residuales de pesticidas. De acuerdo con los requisitos de la Monografía de Farmacopea General "Determinación del contenido de pesticidas residuales en materias primas de hierbas medicinales y preparaciones de hierbas medicinales".
Pureza microbiológica. De acuerdo con los requisitos de la Monografía de la Farmacopea General "Pureza microbiológica".
cuantificación. toda la materia prima, materia prima triturada, polvo: la suma de panaxósidos en términos de panaxósido Rg 1 no menos del 2%; extractivos extraídos con 70% de alcohol - no menos del 20%.
¿Qué es una farmacopea? Si comienza desde lejos, a todas las personas se les debe haber ocurrido al menos una vez cómo los médicos logran memorizar tantos medicamentos, conocer sus dosis, composición química y mecanismo de acción. En esto les ayudan numerosos libros de referencia y compendios que contienen la información necesaria. Y sus autores, a su vez, se inspiran en la farmacopea. ¿Así que qué es lo?
Definición
La farmacopea es una colección de documentos oficiales que especifican los estándares de calidad de materias primas medicinales, excipientes, medicamentos terminados y otros medicamentos utilizados en medicina.
Para establecer el "estándar de oro", se involucran especialistas en el campo de la química y el análisis farmacéutico, se llevan a cabo ensayos controlados doble ciego internacionales aleatorios para descubrir todo lo posible sobre las materias primas y preparaciones medicinales a partir de él. El cumplimiento de todas las normas garantiza la calidad de los productos farmacéuticos.
La Farmacopea Estatal es una farmacopea que tiene fuerza legal y está bajo supervisión estatal. Los requisitos y recomendaciones establecidos en el mismo son vinculantes para todas las organizaciones del país involucradas en la fabricación, almacenamiento, venta y uso de medicamentos. Por la violación de las reglas fijadas en el documento, una persona jurídica o un individuo enfrenta responsabilidad penal.
Historia de la Farmacopea Internacional

Los pensamientos sobre la creación de una lista única de medicamentos que indiquen las dosis y la estandarización de la nomenclatura aparecieron en la comunidad médica científica a fines del siglo XIX, en 1874. La primera conferencia sobre este tema se celebró en Bruselas en 1092. En él, los expertos llegaron a un acuerdo sobre los nombres comunes de los medicamentos y la forma de su extracto en las recetas. En cuatro años, este acuerdo fue ratificado en veinte países. Este éxito se convirtió en el punto de partida para el desarrollo posterior de la farmacopea y su publicación. Veinte años después, tuvo lugar la segunda conferencia en Bruselas, a la que asistieron representantes de cuarenta y un países del mundo.
A partir de ese momento, el cuidado de la publicación y revisión de la farmacopea pasó a la Sociedad de las Naciones. En el momento del acuerdo, se incluyeron en el compendio los principios de preparación y dosificación de 77 sustancias medicinales. Doce años más tarde, en 1937, se constituyó una comisión de expertos de Bélgica, Dinamarca, Francia, Suiza, EE. UU., Países Bajos y Gran Bretaña, quienes se familiarizaron con todas las disposiciones de la farmacopea y decidieron ampliarla a un documento internacional. .
La Segunda Guerra Mundial interrumpió el trabajo de la comisión, pero ya en 1947 los expertos volvieron a su trabajo. En 1959, la comisión se denominó Comité de Expertos en la Especificación de Preparaciones Farmacéuticas. En una de las reuniones de la OMS se decidió crear un programa de denominaciones comunes internacionales para la unificación de la nomenclatura de medicamentos.
Primera edición

La Farmacopea es un documento internacional que ya ha tenido cuatro ediciones, y tras cada una de ellas adquirió algo nuevo.
La primera edición fue aprobada en la tercera Asamblea Mundial de la OMS. Se estableció una secretaría permanente de la Farmacopea Internacional. El libro se publicó en 1951 y cuatro años más tarde se publicó el segundo volumen con adiciones en tres idiomas comunes europeos: inglés, francés y español. Después de un corto período de tiempo, aparecieron publicaciones en alemán y japonés. La primera farmacopea es una colección de documentos normativos para todos los medicamentos conocidos en ese momento. A saber:
- 344 artículos sobre sustancias medicinales;
- 183 artículos sobre formas de dosificación (tabletas, cápsulas, tinturas, soluciones en ampollas);
- 84 modos de diagnóstico de laboratorio.
Los títulos de los artículos estaban en latín, ya que esta era una designación común para todos los trabajadores médicos. Para recolectar la información necesaria se involucraron expertos en estandarización biológica, así como especialistas acotados en las enfermedades más endémicas y peligrosas.
Ediciones posteriores de la Farmacopea Internacional
La segunda edición apareció en 1967. Se dedicaba al control de calidad de los productos farmacéuticos. Además, se tuvieron en cuenta los errores de la primera edición y se agregaron 162 fármacos.
La tercera edición de la farmacopea estaba dirigida a los países en desarrollo. Presentó una lista de sustancias que son ampliamente utilizadas en el cuidado de la salud y al mismo tiempo tienen un costo relativamente bajo. Esta edición contenía cinco volúmenes y se publicó en 1975. Recién en 2008 se realizaron nuevas revisiones al documento. Se referían a la estandarización de medicamentos, métodos de fabricación y distribución.

Una farmacopea es un libro que combina no solo la nomenclatura de sustancias medicinales, sino también instrucciones para su fabricación, almacenamiento y propósito. Este libro contiene una descripción de los métodos químicos, físicos y biológicos de análisis de drogas. Además, contiene información sobre reactivos e indicadores, sustancias medicinales y preparados.
El Comité de la OMS compiló listas de sustancias venenosas (lista A) y potentes (lista B), así como tablas de dosis máximas únicas y diarias de medicamentos.
farmacopea europea

La Farmacopea Europea es un documento normativo que se utiliza en la mayoría de los países europeos en la producción de productos farmacéuticos a la par de la Farmacopea Internacional, la complementa y se centra en las peculiaridades de la medicina en esta región. Este libro ha sido desarrollado por la Dirección Europea para la Calidad de los Medicamentos, que forma parte del Consejo de Europa. La Farmacopea tiene un estatus legal diferente de otros documentos similares, que le fue otorgado por el Consejo de Ministros. El idioma oficial de la Farmacopea Europea es el francés. La última, sexta, reedición fue en 2005.
Farmacopeas nacionales

Dado que la Farmacopea Internacional no tiene fuerza legal y es más bien de carácter consultivo, los países individuales han emitido farmacopeas nacionales para la regulación interna de cuestiones relacionadas con los medicamentos. Por el momento, la mayoría de los países del mundo tienen libros individuales. En Rusia, la primera farmacopea se publicó en 1778 en latín. Solo veinte años después salió una versión en ruso, convirtiéndose en el primer libro de este tipo en el idioma nacional.
En 1866, medio siglo después, se publicó la primera farmacopea oficial en ruso. La 11ª edición, la última durante la existencia de la URSS, apareció a principios de los años noventa del siglo pasado. La preparación, adición y reedición del documento solía estar a cargo del Comité de Farmacopea, pero ahora esto lo realiza el Ministerio de Salud, Roszdravnadzor y el Fondo General de Seguro Médico con la participación de los principales científicos del país.
Farmacopea estatal de la Federación Rusa 12 y 13 ediciones
En el período en que la Farmacopea del Estado estaba sujeta a ajuste, la calidad de los medicamentos se regulaba a través de los artículos de la farmacopea de la empresa (FSP) y los artículos de la farmacopea general (GPM). La duodécima edición de la Farmacopea estatal de la Federación Rusa estuvo significativamente influenciada por el hecho de que especialistas rusos participaron en el trabajo de la farmacopea. La duodécima edición consta de cinco partes, cada una de las cuales incluye normas y reglamentos básicos para la fabricación, prescripción o venta de medicamentos. Este libro fue publicado en 2009.

Seis años después, se revisó la duodécima edición. A fines de 2015, la Farmacopea estatal, 13ª edición, apareció en el sitio web oficial del Ministerio de Salud de la Federación Rusa. Era una versión electrónica, ya que la liberación se realizó con cargo a los fondos de la venta. Por lo tanto, se decidió a nivel legislativo que cada farmacia y empresa de comercio mayorista debería tener una farmacopea estatal (13ª edición). Esto permitió que el libro se pagara solo.
¿Qué es una monografía de farmacopea?
Hay dos tipos de sustancia y forma de dosificación final. Cada artículo "sobre la sustancia" tiene un título en dos idiomas: ruso y latín, nombre común internacional y químico. Contiene fórmulas empíricas y estructurales, peso molecular y cantidad de la sustancia activa principal. Además, hay una descripción detallada de la apariencia de la sustancia medicinal, criterios de control de calidad, solubilidad en líquidos y otras propiedades físicas y químicas. Se estipulan las condiciones de embalaje, fabricación, almacenamiento y transporte. Y también la fecha de caducidad.
El artículo para la forma de dosificación terminada, además de todo lo anterior, contiene los resultados de las pruebas clínicas y de laboratorio, las desviaciones permitidas en la masa, el volumen y el tamaño de las partículas de la sustancia medicinal, así como las dosis máximas únicas y diarias para niños. y adultos
Ministerio de Salud de la Federación Rusa
Institución Educativa Presupuestaria del Estado Federal
Educación más alta
PRIMER MÉDICO DEL ESTADO DE MOSCÚ
UNIVERSIDAD lleva el nombre de I.M. SECHENOV
FACULTAD DE FARMACÉUTICA
DEPARTAMENTO DE FARMACOGNOSIA
Guía práctica
Según la farmacognosia
Tema: Dominar los métodos de análisis farmacognostico
Moscú 2016
TEMA 1
MÉTODOS DE ANÁLISIS FARMACOGNOSTICO
En las clases prácticas, el estudiante recibe las habilidades y destrezas prácticas para resolver problemas profesionales en el análisis de materiales de plantas medicinales enteras de acuerdo con los estándares de calidad estatales.
Para implementar las competencias de control de calidad, los estudiantes deben utilizar la Farmacopea Estatal de la Federación Rusa (http://www.femb.ru/feml), que refleja los requisitos de calidad modernos para todos los medicamentos, incluidas las materias primas de hierbas medicinales y los productos medicinales a base de hierbas, métodos para determinar la calidad y las normas. La Ley Federal No. 61 "Sobre la Circulación de Medicamentos" incluye el Capítulo 3 "Farmacopea Estatal".
El Estándar Educativo del Estado Federal en la especialidad "Farmacia" incluye competencia profesional:
Ø capacidad y disposición para analizar y evaluar la calidad de los materiales de plantas medicinales (órganos vegetales utilizados, estructura histológica, composición química de los activos y otros grupos de sustancias biológicamente activas);
fecha_______ SESIÓN 1
AUTENTICACIÓN DE HOJAS ENTERAS
Trabajo independiente(preparación para la clase)
Ejercicio 1. Analizar OFS. 1.5.1.0001.15 “Materiales de plantas medicinales. Sustancias farmacéuticas de origen vegetal”, OFS.1.5.3.0004.15 “Determinación de la autenticidad, finura y contenido de impurezas en materias primas de plantas medicinales y preparados de hierbas medicinales”, OFS. 1.5.1.0003.15 “Hojas. Folia" Anote las definiciones de los conceptos:
« planta medicinal» -___________________
« Materiales de plantas medicinales» - _________
"Sustancia farmacéutica de origen vegetal" -
« Autenticidad» - _____________________________
Materiales de plantas medicinales Hojas» - ____
¿Qué documento regula el análisis de las "hojas" de materias primas de plantas medicinales? ___
Tarea 2. Dibuja la forma de las hojas. Lirio de los valles de mayo, ortiga, gayuba común, dedalera lanuda.
Tarea 3. Dibuja la nervadura de las hojas. plátano grande y dedalera de flor grande.
Tarea 4. Dibujar el borde de la hoja. púrpura digital, menta, lirio de los valles, uña de caballo.
Tarea 5. Dibujar los tipos de complejos de hojas estomáticas arándano rojo, menta, reloj de tres hojas, belladona común, lirio de los valles de mayo y dar sus nombres.
Tarea 6. Dibuje los tipos de pelos simples y capitados, y dé ejemplos de "hojas" de MV donde ocurran.
| pelos simples | pelos capitados | ||||
| Estructura | Imagen | LRS | Estructura | Imagen | LRS |
| unicelular, liso | cabeza unicelular sobre tallo unicelular | ||||
| "Retorta" unicelular | cabeza bicelular sobre un tallo unicelular | ||||
| 2-4 células, con una superficie verrugosa | cabeza unicelular en un tallo multicelular | ||||
| 3-4 celdas, celda superior larga, fuertemente curvada | cabeza pluricelular sobre tallo unicelular | ||||
| cabeza multicelular sobre un tallo multicelular |
Anote en qué tejido se encuentran los pelos: ________________________________
Tarea 7. Dibuja los tipos de inclusiones de oxalato de calcio en las hojas. ortiga, lirio de los valles de mayo, casia (sen) acebo, belladona.
Anote en qué tejido se encuentran las inclusiones de oxalato de calcio: ____________
Tarea 8. Dibuja las estructuras secretoras que se encuentran en las hojas. menta, ajenjo, eucalipto e indicar su ubicación.
"Control de entrada superado" ___________________ "____" _______ 20___ GRAMO.
(firma del profesor)
TRABAJO EN LA CLASE
Nota:
Ø La autenticidad de las "hojas" de MRL durante la lección se establece de acuerdo con las secciones de la Asamblea Federal "Señales externas" y "Microscopía".
Ø Al estudiar los signos externos de las hojas, las dimensiones y la forma (a excepción de las hojas coriáceas) se determinan visualmente en materias primas empapadas, otros signos, en materias primas secas. El olor se establece frotando las materias primas. El sabor se determina solo en plantas no venenosas en extracto de agua o al masticar materias primas (sin tragar).
Ø Durante el análisis microscópico de la muestra, es necesario establecer la localización de signos de diagnóstico en los tejidos (epidermis, mesófilo).
Ø La documentación reglamentaria se utiliza solo en la etapa final del análisis de materias primas para comparar los resultados obtenidos y escribir una conclusión sobre la conformidad de la autenticidad de la muestra propuesta. Si una muestra de materias primas no cumple con los requisitos del FS, es necesario indicar en qué secciones hay una discrepancia.
Tarea 1. Realice un análisis de la muestra propuesta de materias primas en las secciones "Signos externos" y "Microscopía" del ND. Preparar un protocolo de análisis.
PROTOCOLO DE ANÁLISIS
Las materias primas de hierbas medicinales enteras se enviaron para su análisis. (ruso, nombres latinos)_____
Planta(s) productora(s) ( Ruso, nombres latinos)________________________
Familia ( Ruso, nombres latinos)__________
La calidad del MPS analizado está regulada por ( nombre, numero)_____________________
La materia prima es _______________________
Ejercicio 1. Realice un análisis macroscópico de las materias primas y describa sus características externas en forma de tabla:
Tarea 2. Realizar análisis microscópicos de materias primas.
1. Escriba el método para preparar una micropreparación de una hoja a partir de la superficie: _________
2. Prepare una micropreparación de la hoja _________________ de la superficie, estúdiela, dibuje la estructura anatómica y dé las designaciones de los signos.
3. Completar la tabla de distribución de características diagnósticas por tejidos:
4. Llegue a una conclusión sobre el cumplimiento de los materiales de plantas medicinales con las secciones "Signos externos" y "Microscopía" del FS.
Conclusión. Las materias primas recibidas para análisis ________ ___ cumplen (no cumplen) los requisitos del artículo _____ GF XIII, apartados "Signos externos" y "Microscopía".
Tarea 2. Familiarícese con muestras del herbario de materiales de plantas medicinales de coltsfoot, plátano grande, especies de eucalipto, salvia medicinal, menta, arándano rojo común, gayuba común, ortiga.
"Se acredita el protocolo de la lección" ___________________ "____" _______ 20___ GRAMO.
(firma del profesor)
Materiales de referencia
Farmacopea estatal de la Federación Rusa XIII edición, v. 2
OFS.1.5.1.0001.15 Materiales de plantas medicinales. Sustancias farmaceuticas
origen vegetal
Los requisitos de este Artículo de la Farmacopea General se aplican a los materiales de plantas medicinales y sustancias farmacéuticas de origen vegetal.
Términos básicos y definiciones
Materias primas de plantas medicinales: plantas frescas o secas, o partes de las mismas, utilizadas para la producción de medicamentos por organizaciones de fabricación de medicamentos o para la fabricación de medicamentos por organizaciones de farmacia, organizaciones de farmacia veterinaria, empresarios individuales con licencia para actividades farmacéuticas.
Sustancia farmacéutica de origen vegetal: una materia prima de plantas medicinales estandarizadas, así como una sustancia o sustancias de origen vegetal y/o combinaciones de las mismas, productos de síntesis primaria y secundaria de plantas, incluidas las obtenidas a partir de cultivos de células vegetales, la cantidad de biológicamente sustancias activas de plantas, productos obtenidos por extracción, destilación, fermentación u otro procesamiento de materiales de plantas medicinales, y utilizados para la prevención y tratamiento de enfermedades.
Producto medicinal a base de hierbas: un producto medicinal producido o fabricado a partir de un tipo de materia prima de plantas medicinales o varios tipos de dichas materias primas y vendido en envases secundarios (de consumo).
Los materiales de plantas medicinales pueden estar representados por varios grupos morfológicos: hierbas, hojas, flores, frutos, semillas, cortezas, yemas, raíces, rizomas, bulbos, tubérculos, cormos y otros.
Al moler, los materiales de plantas medicinales pueden ser:
Entero;
aplastada;
Polvo.
Los materiales de plantas medicinales se distinguen por la presencia de los principales grupos de sustancias biológicamente activas utilizadas para estandarizar los materiales de plantas medicinales, por ejemplo, materias primas que contienen flavonoides, glucósidos cardíacos, alcaloides, derivados de antraceno, taninos, etc.
Con cita previa, las materias primas de plantas medicinales se dividen en materias primas:
Utilizado para la producción de hierbas medicinales.
drogas (por ejemplo, flores trituradas en paquetes, polvo en bolsas de filtro);
Se utiliza para hacer hierbas medicinales.
drogas (por ejemplo, infusiones, decocciones).
PRODUCCIÓN
Los materiales de plantas medicinales y las sustancias farmacéuticas de origen vegetal se obtienen de plantas cultivadas o silvestres. Para garantizar la calidad de las materias primas de hierbas medicinales y las sustancias farmacéuticas de origen vegetal, es necesario seguir las reglas apropiadas para las condiciones de cultivo, cosecha, secado, molienda y almacenamiento. En materiales de plantas medicinales y sustancias farmacéuticas.
de origen vegetal, se permite el contenido de impurezas extrañas, tanto de origen orgánico (partes de otras plantas no tóxicas) como mineral (tierra, arena, guijarros), de acuerdo con los requisitos de la Monografía de la Farmacopea General "Determinación de la autenticidad, finura y contenido de impurezas en materias primas de plantas medicinales y preparaciones medicinales a base de hierbas".
Los materiales de plantas medicinales y las sustancias farmacéuticas de origen vegetal utilizadas para la producción y fabricación de medicamentos deben cumplir con los requisitos de los artículos de farmacopea o documentos reglamentarios pertinentes.
Para realizar un análisis con el fin de determinar el cumplimiento de la calidad de los materiales de plantas medicinales y sustancias farmacéuticas de origen vegetal y los medicamentos a base de plantas derivados de ellos con los requisitos de un artículo de farmacopea o documentación reglamentaria, se establecen requisitos uniformes para el muestreo (de acuerdo con con los requisitos de la Monografía de Farmacopea General "Muestreo de materiales de plantas medicinales y medicamentos de plantas medicinales").
En la fabricación de infusiones y decocciones a partir de materiales de plantas medicinales y sustancias farmacéuticas de origen vegetal, el coeficiente de absorción de agua y el coeficiente de consumo se determinan de acuerdo con los requisitos de la Monografía de la Farmacopea General "Determinación del coeficiente de absorción de agua y el coeficiente de consumo de plantas medicinales". materiales”.
INDICADORES DE CALIDAD Y MÉTODOS DE PRUEBA DE MATERIAS PRIMAS DE PLANTAS MEDICINALES
Autenticidad. Las materias primas de plantas medicinales se identifican por características macroscópicas (externas) y microscópicas (anatómicas) (de acuerdo con los requisitos de la Monografía de Farmacopea General para el grupo morfológico de materias primas y la Monografía de Farmacopea General "Técnica para el examen microscópico y microquímico de plantas medicinales materias primas y preparaciones de hierbas medicinales"), y también determinar la presencia en las materias primas vegetales medicinales analizadas de los principales grupos de sustancias biológicamente activas, confirmando su autenticidad (de acuerdo con los requisitos de la Monografía de la Farmacopea General "Determinación de la autenticidad, finura y contenido de impurezas en materias primas de plantas medicinales y preparaciones a base de hierbas"). Para ello se utilizan métodos de análisis fisicoquímicos, químicos, histoquímicos y microquímicos.
Aplastante. La determinación se lleva a cabo de acuerdo con la Monografía de la Farmacopea General "Determinación de la autenticidad, finura y contenido de impurezas en materiales de plantas medicinales y preparaciones medicinales a base de hierbas".
Humedad. La determinación se lleva a cabo de acuerdo con los requisitos de la Monografía de la Farmacopea General "Determinación del contenido de humedad de materiales de plantas medicinales y preparaciones de hierbas medicinales".
La ceniza es común. La determinación se lleva a cabo de acuerdo con los requisitos de la Monografía de la Farmacopea General "Cenizas totales". No se aplica al cultivo de células vegetales.
Ceniza insoluble en ácido clorhídrico. La determinación se lleva a cabo de acuerdo con los requisitos de la Monografía de la Farmacopea General "Cenizas insolubles en ácido clorhídrico". No se aplica al cultivo de células vegetales.
Impurezas orgánicas y minerales. La determinación se lleva a cabo de acuerdo con la Monografía de la Farmacopea General "Determinación de la autenticidad, finura y contenido de impurezas en materiales de plantas medicinales y preparaciones medicinales a base de hierbas". No se aplica al cultivo de células vegetales.
Existencias de infestación de plagas. La determinación se lleva a cabo de acuerdo con la Monografía de la Farmacopea General "Determinación del grado de contaminación de materiales de plantas medicinales y preparaciones de plantas medicinales con plagas comunes". Este indicador se evalúa durante el almacenamiento de los materiales de plantas medicinales y cuando ingresan a procesamiento.
Metales pesados. La determinación se lleva a cabo de acuerdo con la Monografía de la Farmacopea General "Determinación del contenido de metales pesados y arsénico en materiales de plantas medicinales y preparaciones medicinales a base de hierbas".
radionucleidos. La determinación se lleva a cabo de acuerdo con la Monografía de la Farmacopea General "Determinación del contenido de radionucleidos en materiales de plantas medicinales y preparaciones medicinales a base de hierbas".
Cantidades residuales de plaguicidas. La determinación se lleva a cabo de acuerdo con la Monografía de Farmacopea General "Determinación del contenido de pesticidas residuales en materiales de plantas medicinales y preparaciones de hierbas medicinales" en la etapa del proceso tecnológico.
Pureza microbiológica. La determinación se lleva a cabo de acuerdo con la OFS "Pureza microbiológica".
cuantificación. El contenido de sustancias biológicamente activas que determinan la acción farmacológica de los materiales de plantas medicinales se determina mediante el método especificado en la monografía de la farmacopea o la documentación reglamentaria. Deben validarse los métodos utilizados para la determinación cuantitativa de los principales grupos de sustancias biológicamente activas.
Dependiendo del propósito de las materias primas de plantas medicinales para el mismo tipo de materias primas de plantas medicinales, se pueden dar las normas para el contenido de uno, dos o más grupos de sustancias biológicamente activas.
En las materias primas de plantas medicinales se realiza una determinación cuantitativa:
Sustancias extractivas: de acuerdo con los requisitos de la Monografía de la Farmacopea General "Determinación del contenido de sustancias extractivas en materiales de plantas medicinales y preparaciones medicinales a base de hierbas";
Aceite esencial: de acuerdo con los requisitos de la Monografía de la Farmacopea General "Determinación del contenido de aceite esencial en materias primas de plantas medicinales y preparaciones de hierbas medicinales";
Aceites grasos: de acuerdo con los requisitos de la Monografía de la Farmacopea General "Aceites vegetales grasos";
Taninos: de acuerdo con los requisitos de la Monografía de la Farmacopea General "Determinación del contenido de taninos en materias primas de plantas medicinales y preparaciones de hierbas medicinales".
Otros grupos de sustancias biológicamente activas de acuerdo con los requisitos de los artículos de la farmacopea o la documentación reglamentaria.
El contenido de sustancias biológicamente activas relacionadas con sustancias tóxicas y potentes (glucósidos cardíacos, alcaloides, etc.) se indica con la designación de dos límites "no menos" y "no más". En el caso de un contenido sobreestimado de estos grupos de sustancias biológicamente activas en materiales de plantas medicinales, se permite su uso posterior para la producción de medicamentos, que se calcula mediante la fórmula:
donde m es la cantidad de material vegetal medicinal necesario para la producción de medicamentos a base de plantas, g;
A - la cantidad prescrita de materiales de plantas medicinales, g:
B - el número real de unidades de acción en la materia prima o el contenido de sustancias activas biológicamente activas en 1 g de materia prima en%;
B es el contenido estándar de unidades de acción en materias primas o el contenido de sustancias activas biológicamente activas en 1 g de materias primas en %.
Embalaje, marcado y transporte. Se lleva a cabo de acuerdo con los requisitos de la Monografía de la Farmacopea General "Envasado, etiquetado y transporte de materiales de plantas medicinales y medicamentos a base de plantas".
Almacenamiento. Se lleva a cabo de acuerdo con los requisitos de la Monografía de la Farmacopea General "Almacenamiento de materias primas de hierbas medicinales y preparaciones de hierbas medicinales". En el caso de utilizar desinfectantes, desinfectantes y otros agentes durante el almacenamiento de materias primas de plantas medicinales, es necesario confirmar que no afecten a las materias primas y que se eliminen casi por completo después del procesamiento.
OFS. 1.5.1.0003.15 Hojas. Folia.
Las hojas en la práctica farmacéutica se denominan materiales de plantas medicinales, que son hojas secas o frescas u hojas individuales de una hoja compleja. Las hojas generalmente se cosechan completamente desarrolladas, con o sin pecíolo.
Signos externos. Materias primas enteras y trituradas. Preparación de objetos para el análisis:
Las hojas pequeñas y coriáceas se examinan secas;
Las hojas grandes y delgadas (generalmente arrugadas) se reblandecen en una cámara húmeda o sumergiéndolas durante varios minutos en agua caliente;
Las hojas frescas se examinan sin pretratamiento.
Las hojas preparadas para el análisis se colocan sobre una placa de vidrio, se extienden con cuidado, se examinan a simple vista con una lupa (10x) o un microscopio estereoscópico (8*, 16*, 24*, etc.). Preste atención a las siguientes características anatómicas y de diagnóstico:
1. Estructura (simple, compleja - pinnada no pareada, pinnada pareada, pinnada pareada doble, pinnada pareada doble, compuesta palmeada, compuesta tricatelica, etc.) y las dimensiones de la lámina de la hoja.
2. Forma de hoja(redondeadas, elípticas, ampliamente elípticas, estrechamente elípticas, oblongas, ovadas, ampliamente ovoides, estrechamente ovadas, obovadas, redondeadas obovadas, ampliamente obovadas, lanceoladas, en forma de corazón, sagitadas, en forma de lanza, en forma de hoz, en forma de aguja, etc. .).
3. Profundidad de corte de la lámina de la hoja (palchatolobe, pinnada-lobulada, ternada-lobulada, digitipartida, pinnada, ternada, digitidisectada, pinnada-disectada, ternada-disectada).
4. La naturaleza de la base (redondeada, redondeada ancha, redondeada estrecha, en forma de cuña, en forma de cuña estrecha, en forma de cuña ancha, truncada, con muescas, en forma de corazón, etc.) y el ápice (afilado , redondeada, obtusa, entallada, estirada, etc.) de la lámina de la hoja.
5. La naturaleza del borde de la hoja (macizo, dentado, doblemente dentado, dentado, almenado, dentado).
6. La presencia de un pecíolo, sus dimensiones.
7. La naturaleza de la superficie del pecíolo (lisa, acostillada, surcada, etc.).
8. La presencia de la vagina, estipulaciones (libres, fusionadas), características, dimensiones.
9. Pubescencia de la hoja y pecíolo (abundancia y disposición de pelos).
10. Venación de la hoja (en monocotiledóneas - paralela, arqueada; en dicotiledóneas - pinnada, palmeada; en helechos y plantas con semillas primitivas (gingko) - dicotómica).
11. La presencia de glándulas de aceite esencial y otras formaciones en la superficie de la hoja o la presencia de receptáculos en el mesófilo.
Las dimensiones se determinan usando una regla de medición o papel cuadriculado. Mida la longitud y el ancho de la lámina de la hoja, la longitud y el diámetro del pecíolo.
El color se determina en ambos lados de la hoja sobre un material seco a la luz del día.
El olor se determina moliendo.
El sabor se determina probando una materia prima seca o un extracto acuoso de las hojas (solo en objetos no venenosos).
Para las hojas trituradas, se determina la trituración: el tamaño de los orificios del tamiz a través de los cuales pasa la mezcla de partículas.
Polvo. Se examinan a simple vista, utilizando una lupa (10x) o un microscopio estereoscópico (8*, 16*, 24*, etc.). Se anota el color de la mezcla de partículas (masa total e inclusiones individuales), la forma de las partículas, el origen de las partículas y su naturaleza (si se determina). Cuando se observa con lupa o microscopio estereoscópico, se presta atención a la pubescencia de los fragmentos, la naturaleza de la superficie (lisa, rugosa, cubierta de glándulas, etc.). Determine el olor y el sabor (similar a las hojas enteras y trituradas). Se determina la finura (el tamaño de las aberturas del tamiz a través de las cuales pasa la mezcla de partículas).
Microscopía. Hojas enteras y trituradas. Los micropreparados se preparan de acuerdo con la Monografía de la Farmacopea General "Técnica para el examen microscópico y microquímico de materiales de plantas medicinales y medicamentos a base de hierbas" a partir de hojas enteras o trozos de una hoja con un borde y una vena, trozos de una hoja de la base y arriba, trozos de pecíolo (si la hoja tiene pecíolo), examinándolos desde la superficie. Al analizar hojas gruesas y coriáceas (eucalipto, gayuba, arándano rojo), se preparan secciones transversales y micropreparaciones "prensadas". Si es necesario, también se preparan secciones transversales de los pecíolos.
Preste atención a las siguientes características anatómicas y de diagnóstico:
1. La naturaleza de la cutícula de la epidermis superior e inferior (lisa, arrugada, incluso longitudinalmente arrugada, transversalmente arrugada, radiante arrugada, rayada, en forma de cresta, etc.).
2. La forma de las células de la epidermis superior e inferior (isodiamétrica: redonda, cuadrada, poligonal; poligonal: rectangular, ovalada, en forma de diamante, en forma de huso, combinada, etc.); sinuosidad de las paredes celulares de la epidermis superior e inferior (recta, sinuosa, ondulada, en zigzag, irregular, etc.), grado de sinuosidad; engrosamiento de las paredes celulares de la epidermis superior e inferior (uniforme, con cuentas).
3. La presencia de estomas, su forma (redonda, ovalada), tamaño, frecuencia de aparición en la epidermis superior e inferior.
4. Tipo de aparato estomático:
Tipo anomocítico (al azar celular) - anomocítico (o ranunculoide) - los estomas están rodeados por un número indefinido de células que no difieren en forma y tamaño del resto de las células de la epidermis;
Tipo diacítico (bicelular): los estomas están rodeados por dos células parótidas, cuyas paredes adyacentes son perpendiculares al espacio estomático;
Tipo paracítico (célula paralela): a cada lado de los estomas, a lo largo de su eje longitudinal, hay una o más células parótidas;
Tipo anisocítico (no isocelular): los estomas están rodeados por tres células parótidas, de las cuales una es mucho más pequeña que las otras dos;
Tipo tetracítico: los estomas están rodeados por 4 células parotídeas ubicadas simétricamente: dos células son paralelas a la brecha estomática y las otras dos están adyacentes a los polos de las células protectoras;
Tipo hexacítico: los estomas están rodeados por 6 células parótidas: dos pares están ubicados simétricamente a lo largo de las células protectoras y dos células ocupan posiciones polares;
Tipo enciclocítico: las células laterales forman un anillo estrecho alrededor de las células protectoras;
Tipo actinocítico: caracterizado por varias células laterales, que divergen radialmente de las células posteriores.
5. La presencia de estomas de agua (se diferencian por su gran tamaño y suelen estar situados en la parte superior de la hoja o del diente, por encima del hidátodo).
6. Inmersión de estomas en la epidermis (sobresaliendo por encima de la epidermis, sumergidos en la epidermis).
7. La presencia y estructura de los pelos en la epidermis superior e inferior (simple y grande, unicelular y multicelular, uni, bi y multifila, en haz, ramificado y no ramificado), su tamaño, características de sus sitios de unión (la presencia de una roseta), engrosamiento de las paredes (paredes gruesas y delgadas), la naturaleza de la cutícula (lisa, verrugosa, shrikhovy).
8. La presencia de glándulas en la epidermis superior e inferior, su estructura, tamaño.
9. Presencia de canales secretores, lactíferos, receptáculos (en el parénquima debajo de la epidermis).
10. La presencia y estructura de inclusiones cristalinas (cristales individuales de varias formas, drusas, ráfidos, estiloides, cistolitas, arena cristalina, etc.), su localización (en el parénquima debajo de la epidermis, en el parénquima en forma de cristal -revestimiento de cojinete alrededor de los haces conductores y grupos de fibras, rara vez en las células epidérmicas)
11. La presencia de inclusiones de nutrientes de reserva: moco, inulina, etc. (en el parénquima debajo de la epidermis, con menos frecuencia en las células de la epidermis).
12. Estructura del mesófilo (forma celular, homogeneidad, ubicación, presencia de aerénquima).
13. Estructura de la hoja (dorsoventral, aislada).
14. La estructura del sistema vascular de la hoja (la forma de la vena principal; el número, la forma, la ubicación de los haces vasculares en la vena; la estructura de los haces vasculares: la ubicación del floema y el xilema, la presencia de tejidos mecánicos).
15. La presencia de tejido mecánico (colénquima, fibras esclerenquimatosas, células pedregosas, fibras bastas, etc.).
16. La estructura del pecíolo: en la sección transversal del pecíolo de la hoja, indique su forma en las partes media, basal y apical (redondeada, triangular, acanalada, en forma de hoz, ligeramente pterigoidea, de alas anchas), el número y ubicación de los rayos vasculares, la presencia de tejido mecánico (colénquima, esclerénquima).
Polvo. Las micropreparaciones de polvo de hojas se preparan de acuerdo con la Monografía de la Farmacopea General "Técnica para el examen microscópico y microquímico de materias primas de plantas medicinales y preparaciones de hierbas medicinales". En las micropreparaciones del polvo se consideran fragmentos de hojas con las nervaduras principales y secundarias, fragmentos de hojas con el borde del limbo, fragmentos de la parte superior de la hoja, fragmentos en sección transversal, fragmentos del pecíolo. En las partículas de polvo estudiadas, se observan todas las características anatómicas y de diagnóstico que se manifiestan enumeradas para hojas enteras y trituradas. Preste atención al hecho de que una serie de elementos (pelos, glándulas, cristales, drusas, etc.) se pueden separar de las partículas de la hoja; En el polvo se observan muchos fragmentos de tejidos y elementos individuales: cabellos y sus fragmentos, glándulas, cristales individuales de oxalato de calcio y fragmentos del revestimiento que contiene cristales, células mecánicas - fibras, esclereidas, fragmentos de canales secretores, receptáculos, lactifers, etc.
En un polvo con un tamaño de partícula de más de 0,5 mm, en los fragmentos considerados, se pueden distinguir casi todas las características características de las materias primas enteras y trituradas. Algunos elementos de la epidermis pueden estar en forma de fragmentos de pelos, glándulas, etc.; debido a la destrucción de las células, pueden producirse cristales individuales, drusas, etc.
Es aún más difícil aislar características anatómicas y diagnósticas en el polvo de materias primas de plantas medicinales con un tamaño de partícula inferior a 0,5 mm. También puede haber fragmentos de varias partes de la epidermis de la hoja, sin embargo, si es posible, se debe prestar más atención a los elementos individuales: pelos individuales, glándulas, cristales, características celulares, etc.
En el polvo de materias primas de plantas medicinales con un tamaño de partícula inferior a 0,5 mm, se presta atención a las características estructurales de las células y la presencia de elementos individuales de la epidermis y el mesófilo de la hoja: pelos individuales, glándulas, sus fragmentos, cristales. , etc.
La descripción de las principales características diagnósticas debe ir acompañada de material ilustrativo.
Microscopía de luminiscencia. Considere un polvo seco, con menos frecuencia una sección transversal de una lámina, preparado a partir de materias primas enteras o trituradas después de un ablandamiento preliminar en una cámara húmeda. Hay fluorescencia propia (primaria) de la materia prima en luz ultravioleta. La cutícula, las membranas celulares de los tejidos mecánicos, los elementos del xilema, los cabellos, el contenido de células individuales o tejidos del mesófilo, la epidermis de la hoja, según su composición química, tienen el brillo más brillante. Las hojas de algunas plantas se caracterizan por un brillo intenso y específico del contenido de las glándulas, canales secretores y receptáculos, según la composición química del contenido.
Reacciones microquímicas e histoquímicas cualitativas
realizado en micropreparaciones de hojas (en secciones transversales, preparaciones de la superficie, en polvo), más a menudo para detectar cutícula gruesa, aceite esencial (puede presentarse en forma de gotas o encerrado en recipientes y/o túbulos), así como moco de acuerdo con los requisitos de la Monografía de Farmacopea General "Técnica para el examen microscópico y microquímico de materias primas de plantas medicinales y preparaciones de plantas medicinales".
Las reacciones cualitativas se llevan a cabo con extracción de las hojas de acuerdo con los métodos indicados en artículos de farmacopea o documentos reglamentarios.
Cromatografía. Los extractos se analizan mediante diversas técnicas cromatográficas utilizando muestras estándar. Muy a menudo, los componentes de los aceites esenciales, flavonoides, etc. se determinan cromatográficamente en extractos de hojas.
Espectro (espectro UV). El análisis se lleva a cabo en el extracto de las hojas en presencia de las instrucciones apropiadas en la monografía o documentación reglamentaria. Se permite una referencia a la sección "Cuantificación". Se da una descripción de las condiciones para registrar el espectro, indicando las longitudes de onda en las que se deben observar máximo(s) y mínimo(s) de absorción.
En conjunto, las materias primas trituradas y el polvo determinan:
Es posible determinar sustancias extractivas de acuerdo con los requisitos de la Monografía de Farmacopea General "Determinación del contenido de sustancias extractivas en materiales de plantas medicinales y preparaciones medicinales a base de hierbas";
Humedad de acuerdo con los requisitos de la Monografía de Farmacopea General "Determinación del contenido de humedad de materias primas de hierbas medicinales y preparaciones de hierbas medicinales";
ácido clorhídrico, de acuerdo con los requisitos de la Monografía de Farmacopea General "Cenizas generales" y la Monografía de Farmacopea General "Cenizas insolubles en ácido clorhídrico";
Finura y contenido de impurezas de acuerdo con los requisitos de la Monografía de la Farmacopea General "Determinación de la autenticidad, finura y
La masa del contenido del paquete debe cumplir con los requisitos de la Monografía de la Farmacopea General "Muestreo de materiales de plantas medicinales y medicamentos a base de hierbas".
Existencias de infestación de plagas. La determinación se lleva a cabo de acuerdo con la Farmacopea General
"Determinación del grado de contaminación de materias primas de plantas medicinales y preparados de plantas medicinales con plagas comunes".
Una característica de la etapa actual de estandarización de medicamentos es la necesidad de armonizar los requisitos para la calidad de los medicamentos y los métodos para su prueba, presentados por la Farmacopea Rusa y las principales farmacopeas extranjeras.
La XII edición de la Farmacopea Estatal de la Federación Rusa incluirá cinco partes.
La primera parte describe las disposiciones generales, los métodos de análisis, los requisitos para las sustancias farmacéuticas y los artículos de la farmacopea sobre la sustancia.
La Farmacopea Estatal (SP) es una colección de estándares básicos utilizados en el análisis farmacopeico y la producción de medicamentos. La Farmacopea Estatal tiene carácter legislativo. La Farmacopea Estatal se basa en artículos de farmacopea general (GPM) y artículos de farmacopea (FS). La OFS describe las disposiciones generales adoptadas en el análisis de la farmacopea, los métodos de análisis o incluye una lista de indicadores estandarizados y métodos de prueba para una forma de dosificación en particular. El FS determina el nivel de requisitos para medicamentos específicos.
CONTENIDO
I. CONSEJO EDITORIAL DE ROSZDRAVNADZOR PARA LA ORGANIZACIÓN DEL TRABAJO SOBRE LA FARMACOPEIA DEL ESTADO 7
II. PRÓLOGO 9
tercero ORGANIZACIONES, INSTITUCIONES DE RUSIA Y ESPECIALISTAS QUE PARTICIPARON EN LA PREPARACIÓN DE LA PARTE 1 DEL FARMACOPEO ESTATAL DE LA FEDERACIÓN DE RUSIA XII EDICIÓN 10
IV. INTRODUCCIÓN 13
FARMACOPIAS GENERALES
1. Reglas para el uso de monografías de farmacopea (OFS 42-0031-07) 17
2. Unidades del sistema internacional (SI) utilizadas en la farmacopea y su correspondencia con otras unidades (OFS 42-0032-07) 22
MÉTODOS DE ANÁLISIS 26
3. Equipo (OFS42-0033-07) 26
MÉTODOS DE ANÁLISIS FÍSICOS Y FISICOQUÍMICOS 29
4. Punto de fusión (OFS 42-0034-07) 29
5. Temperatura de solidificación (OFS 42-0035-07) 34
6. Límites de temperatura de destilación y punto de ebullición (OFS 42-0036-07) 36
7. Densidad (OFS 42-0037-07) 38
8. Viscosidad (OFS 42-0038-07) 41
9. Determinación de alcohol etílico en preparados farmacéuticos líquidos (OFS 42-0039-07) 49
10. Refractometría (OFS 42-0040-07) 52
11. Polarimetría (OFS 42-0041-07) 54
12. Métodos espectroscópicos 56
12.1. Espectrofotometría en las regiones ultravioleta y visible (OFS 42-0042-07) 56
12.2. Espectrometría en la región infrarroja (OFS 42-0043-07) 62
12.3. Espectrometría de emisión atómica y absorción atómica (OFS 42-0044-07) 66
12.4. Fluorimetría (OFS 42-0045-07) 70
12.5. Espectroscopía de resonancia magnética nuclear (OFS42-0046-07) 73
13. Osmolaridad (OFS 42-0047-07) 78
14. Yoyom&trt (OFS 42-0048-07) 85
15. Solubilidad (OFS 42-0049-07) 92
16. El grado de color de los líquidos (OFS 42-0050-07) 93
17. Transparencia y grado de turbidez de los líquidos (OFS 42-0051-07) 98
MÉTODOS QUÍMICOS DE ANÁLISIS 101
18. Determinación de nitrógeno en compuestos orgánicos por el método Kjeldahl (OFS 42-0052-0 7) 101
19. Determinación de proteína (OFS 42-0053-07) 105
20. Nitritometría SOFS 42-0054-0 7) 114
PRUEBA DE LÍMITE 115
21. Total de cenizas (OFS 42-0055-07) 115
22. Ceniza sulfatada (OFS 42-0056-07) 115
23. Disolventes orgánicos residuales (OFS 42-0057-07) 115
24. Prueba de pureza y límites de impurezas 118
24.1. Hierro (OFS 42-0058-07) 119
24.2. Metales pesados (OFS 42-0059-07) 121
MÉTODOS DE CONTROL BIOLÓGICO 124
25. Toxicidad anómala (OFS 42-0060-07) 124
26. Pirogenicidad (OFS 42-0061-07) 125
27. Endotoxinas bacterianas (OFS 42-0062-07) 128
28. Prueba de histamina ("OFS 42-0063-07) 136
29. Prueba de sustancias depresoras (OFS 42-0064-07) 140
30. Métodos biológicos para evaluar la actividad de materiales de plantas medicinales y fármacos que contienen glucósidos cardíacos (OFS 42-0065-07) 141
31. Esterilidad (OFS 42-0066-0 7) 150
32. Pureza microbiológica (OFS 42-0067-07) 160
33. Determinación de la actividad antimicrobiana de los antibióticos por el método de difusión en agar (OFS 42-0068-0 7) 194
34. Determinación de la eficacia de conservantes antimicrobianos de fármacos (OFS 42-0069-07) 216
REACTIVOS 220
35. Reactivos. Indicadores (OFS 42-0070-07) 220
36. Soluciones tituladas (OFS 42-0071-07) 425
37. Soluciones tampón (OFS 42-0072-07) 443
38. Radiofármacos (OFS 42-0073-07) 456
39. Sustancias farmacéuticas (OFS 42-0074-07) 484
40. Periodo de validez de los medicamentos (OFS 42-0075-07) 488
FARMACOPIAS 493
Descargue gratis el libro electrónico en un formato conveniente, mire y lea:
Descargue el libro La Farmacopea Estatal de la Federación Rusa, XII edición, Parte 1, 2007 - fileskachat.com, descarga rápida y gratuita.
Descargar archivo #1 - doc
Descargar archivo #2 - djvu
A continuación puede comprar este libro al mejor precio con descuento y entrega en toda Rusia.