MBOU Beyskaya միջնակարգ գիշերօթիկ դպրոց
միջնակարգ (ամբողջական) հանրակրթ
Ուսուցիչը OBZH-ի կազմակերպիչ Մալանչիկ Պավել Իվանովիչն է։
Պլան - նկարչության դասի ուրվագիծ 8-րդ դասարանի համար
Դասի թեմաԵրկրաչափական մարմինների բացված մակերեսների գծագրեր
Դասի նպատակըՍովորեցնել, թե ինչպես նախագծել օբյեկտը 3 հարթության վրա: Զարգացնել տարածական մտածողությունը: Մշակել ճշգրտություն նկարներ կատարելիս:
ՄեթոդներԶրույց, բացատրություն, ցուցադրություն, ինքնուրույն աշխատանք։
ՍարքավորումներԴասագիրք, պաստառ, նկարչական գործիքներ, մոդելներ։
Դասի տեսակըՆոր նյութի ուսուցում
Դասի կառուցվածքը
Օրգ. պահ - 2-3 ր.
Գրաֆիկական աշխատանքի վերլուծություն - 5ր.
Ամրագրում - 25 րոպե:
Եզրափակիչ մաս - 3 ր.
Դասերի ժամանակ
Օրգ. պահը.
Բարև, նստե՛ք:
Այսօրվա դասի թեման է՝ «Երկրաչափական մարմինների բացված մակերեսների գծագրեր»։ Գրեք այն ձեր նոթատետրում նկարչական տիպով (թեման գրված է գրատախտակին), և այդ ժամանակ ձեր աշխատանքը կբաժանեմ ձեզ։
Դասի նպատակի սահմանում, առաջիկա գործունեության մոտիվացիա, (ցանկալի է, որ դասում իրենց գործունեության նպատակները սահմանեն հենց երեխաները, բավարար է երկու-երեք հոգի.
Գրաֆիկական աշխատանքի կատարման վերլուծություն.
Ընդհանուր սխալները դրեք գրատախտակին, նշեք լավագույն աշխատանքը:
նոր նյութ
Պրիզմաների և գլանների բացված մակերեսների գծագրեր:
Բացատրության ընթացքում ցուցադրեք կտրված սքաները, ցույց տվեք երեխաների կողմից անցած տարիներին արված սքաները։
Հաստոցների, օդափոխման խողովակների և որոշ այլ ապրանքների համար պարիսպների արտադրության համար դրանց վերամշակիչները կտրված են թիթեղից:
Ցանկացած ուղիղ պրիզմայի մակերևույթների զարգացումը հարթ կերպար է, որը կազմված է կողային երեսներից՝ ուղղանկյուններից և երկու հիմքերից՝ բազմանկյուններից:
Օրինակ, վեցանկյուն պրիզմայի մակերևույթների մշակման ժամանակ (նկ. 139, բ) բոլոր երեսները հավասար ուղղանկյուններ են՝ a լայնությամբ և բարձրությամբ / i, իսկ հիմքերը՝ կանոնավոր վեցանկյուններ, որոնց կողմը հավասար է a-ին:
Այսպիսով, հնարավոր է կառուցել ցանկացած պրիզմայի մակերեսների մաքրման գծանկար:
Մխոցի մակերեսների զարգացումը բաղկացած է ուղղանկյունից և երկու շրջանից (նկ. 140, բ): Ուղղանկյան մի կողմը հավասար է մխոցի բարձրությանը, մյուսը հիմքի շրջագիծն է։ Մաքրման գծագրում ուղղանկյունին ամրացված են երկու շրջան, որոնց տրամագիծը հավասար է գլանի հիմքերի տրամագծին։


Կոնի և բուրգի մակերևույթների զարգացումների գծագրեր:
Կոնու մակերևույթների զարգացումը հարթ գործիչ է, որը բաղկացած է հատվածից՝ կողային մակերեսի զարգացումից և շրջանից՝ կոնի հիմքից (նկ. 141, բ):
Կառուցումները կատարվում են այսպես.
1. Գծվում է առանցքային գիծ և s կետից «դրա վրա s երկարությանը հավասար շառավղով» նկարագրում են «կոնի գեներատոր, շրջանագծի աղեղ։ Կոնի հիմքի շրջագիծը գծագրվում է վրա. այն.
s կետը միացված է աղեղի վերջավոր կետերին։ 2. Ստացված պատկերին կցվում է շրջան՝ հատվածը։ Այս շրջանագծի տրամագիծը հավասար է կոնի հիմքի տրամագծին։

Շրջանակի շրջագիծը հատված կառուցելիս կարելի է որոշել
ըստ C \u003d nD բանաձևի:
A անկյունը հաշվարկվում է բանաձևով ![]() ,
,
դ - հիմքի շրջագծի տրամագիծը,
R-ը կոնի ծագման երկարությունն է, այն կարելի է հաշվարկել Պյութագորասի թեորեմի միջոցով։
Բուրգի մակերեսների մաքրման նկարը կառուցված է այսպես
(նկ. 142, բ):
O կամայական կետից նկարագրվում է R շառավղով աղեղ, որը հավասար է բուրգի կողային եզրի երկարությանը: Այս աղեղի վրա դրեք չորս հատված, որը հավասար է հիմքի կողքին: Ծայրահեղ կետերը ուղիղ գծերով միացված են O կետին: Այնուհետև կցվում է քառակուսի, որը հավասար է բուրգի հիմքին:
Ուշադրություն դարձրեք, թե ինչպես են գծագրվում մաքրման գծագրերը: Պատկերի վերևում գրում են «Սկան»՝ ներքևում տողով։ Ծալովի գծերից, որոնք գծված են երկու կետով գծիկավոր գծով, գծում են առաջատար գծեր և գրում «Ծալովի գծեր» դարակում.

Մաքրումների կառուցումը սովորաբար իրականացվում է գրաֆիկական տեխնիկայով՝ օգտագործելով նկարագրական երկրաչափության առաջարկած մեթոդները:
Հարթություններով սահմանափակված մասերի կամ զարգացվող կոր մակերևույթների մակերեսները կարող են մշակվել և ճշգրտորեն համապատասխանեցնել հարթությանը: Այս դեպքում մակերեսի վրա ընկած կետերը (հատվածները) պահվում են սկանավորման վրա, և մաքրման յուրաքանչյուր կետ (ուղիղ գծի հատված) համապատասխանում է մասի մակերևույթի լավ սահմանված և եզակի կետին (ուղիղ գծի հատված), և հակառակը։
Նկարում ներկայացված են բազմանիստ մարմինների և հեղափոխության մարմինների բացված մակերեսները։
Բազմեյդրոնի մակերևույթի կառուցումը կրճատվում է նրա յուրաքանչյուր դեմքի բնական չափը որոշելով: Սկզբում գծվում է կողային մակերեսը, այնուհետև պոլիէդրոնի հիմքերը ամրացվում են երեսներից մեկին (մեկ կամ երկու, կախված նրանից, թե դա պրիզմա է, թե բուրգ:

Բազմանդամների և հեղափոխության մարմինների զարգացումների օրինակներ



խարսխում
Երեխաների հետ միասին երկրաչափական մարմինների ամբողջական և դիզայներական մաքրում.
Մխոց, կոն, պրիզմա, բուրգ:
Շինարարության ընթացքում ևս մեկ անգամ կանգ առեք այս աշխատանքի իրականացման առանձնահատկությունների վրա: Ցուցադրել կտրված սկանավորումները, ցույց տալ սկանավորումները, որոնք արվել են երեխաների կողմից անցյալ տարիներին:
Վերջնական մաս
Ամփոփելով.
Ի՞նչն է ձեզ դուր եկել այսօրվա դասից:
Ի՞նչը ձեզ չէր սազում այս դասում (տեմպ, ծավալ և այլն):
Դուք հասե՞լ եք ձեր նպատակներին: Արդյո՞ք բոլորը գործն ավարտեցին:
Ի՞նչ ես սովորել: (կարող է արժե այստեղ հարցեր տալ՝ կախված ժամանակից)
Տնային աշխատանքԲացեք և կպցրեք այն: (Ցանկացած երկրաչափական մարմին ընտրելու համար, չափերը h - առնվազն 70 մմ
Առաջադրանքի նպատակը- մակերեսային մշակումների կառուցում՝ մակերևույթների հատման գիծ գծելով։
Տրված է.Նկարչություն «»:
Անհրաժեշտ:Կառուցեք մխոցի զարգացումը և դրա վրա նշեք մխոցի և կիսագնդի մակերեսների փոխադարձ հատման գիծը:
Մենք արդեն նկարել ենք գլանների սկանավորում, ուստի կկրկնենք ուսումնասիրված նյութը։ Ընդ որում, բնօրինակ գծանկարը և սկզբնական գծագրի կառուցման եղանակը տարբերվում են նախորդից։
Մխոցների մաքրման ալգորիթմ
- Մենք կառուցում ենք մխոցի կողային մակերեսի զարգացում:
- Մխոցի հիմքը բաժանում ենք 12 հավասար մասերի։
- Մենք չափում ենք ակորդը բազային շրջանի ցանկացած երկու հարակից բաժանման կետերի միջև և մի կողմ ենք դնում այս հեռավորությունը գլանների մաքրման ստորին մասի երկայնքով:
- Մխոցի հիմքերը ամրացնում ենք կողային մակերեսի ցանկացած գեներատորի վրա։
- Գլանի կողային մակերեսի զարգացման վրա դրեցինք կոնի և գլանների հատման գիծը։
Քանի որ մենք ունենք մխոցի և կիսագնդի փոխադարձ խաչմերուկի միայն մեկ պրոյեկցիա (ճակատային), մենք կկառուցենք միայն մխոցի պրոֆիլային պրոյեկցիան: Մխոցի պրոֆիլային պրոյեկցիան՝ բոլոր օժանդակ կոնստրուկցիաներով, որոնք անհրաժեշտ են բալոնի մշակման կառուցման համար, կնշվի բարակ գծերով և կհամարվի օժանդակ կոնստրուկցիաներ։
Լրացուցիչ մանրամասների համար տես տեսանյութի ձեռնարկը:
Видео «Գլանների մաքրում».
Այս վիդեո ձեռնարկը և հոդվածը ներառված են AutoCAD-ի պրոֆեսիոնալ անվճար ձեռնարկում, որը հարմար է ինչպես սկսնակ օգտատերերի, այնպես էլ նրանց համար, ովքեր երկար ժամանակ աշխատում են AutoCAD-ում:
Նկարչության դասի ամփոփում.
Թեմա:Որոշ երկրաչափական մարմինների ավլումների գծագրեր:
Նպատակները:
- համախմբել երկրաչափական մարմինների հայեցակարգը.
Նպաստել երկրաչափական մարմինների մաքրման կառուցման անկախ ուսումնասիրությանը.
Մշակել տարածական պատկերացումներ և մտածողություն, տեղեկատվության աղբյուրների հետ աշխատելու կարողություն.
Թիմում ժամանակի, պատասխանատվության զգացում զարգացնել։
Դասի տեսակը.դաս սովորելու նոր նյութ
Նյութական աջակցություն.երկրաչափական մարմինների մոդելներ, քարտեր՝ առաջադրանքներ, դասագրքեր, նկարչական պարագաներ, նկարչական թուղթ։
ԴԱՍԵՐԻ ԺԱՄԱՆԱԿ.
1. Կազմակերպչական մաս.
Շատ ճիշտ, շատ իմաստուն
Թող ծուլությունը խոչընդոտ չլինի,
Առավոտյան բոլորին ասեք. «Բարի ... (առավոտ)»,
Դե, կեսօրին, ասեք. «Բարի… (օր)»:
Դիտեք ուսանողների պատրաստակամությունը դասին:
Պատրա՞ստ եք սկսել դասը:
Արդյո՞ք ամեն ինչ իր տեղում է: Ամեն ինչ կարգին է:
Գրքեր, գրիչներ, մատիտներ և նոթատետրե՞ր:
Մենք ունենք այս կարգախոսը.
Այն ամենը, ինչ ձեզ հարկավոր է ձեր մատների վրա:
2. Գիտելիքների թարմացում
Անցած դասերի ընթացքում մենք ուսումնասիրեցինք որոշ երկրաչափական մարմիններ, սովորեցինք, թե ինչպես կառուցել դրանց գծագրերը: Եկեք հիշենք, թե ինչ են երկրաչափական մարմինները:
Ես ցույց եմ տալիս և ուսանողների անունները.
Եկեք ստուգենք, թե ինչպես եք սովորել նյութը:
Ո՞րն է կանխատեսումների հերթականությունը:(ճակատային, հորիզոնական և պրոֆիլ):
Մեկն աշխատում է գրատախտակի վրա (Յուրա)՝ կատարելով կոնի պրոյեկցիաներ, իսկ մնացածներն աշխատում են ինքնուրույն նոթատետրում։
Կոնի բարձրությունը L= 40 մմ, հիմքի տրամագիծը՝ 30 մմ։
3. Նոր նյութի ուսուցում.
Դասի թեման.
Այսօր մենք կշարունակենք աշխատել երկրաչափական մարմինների հետ, այսօրվա դասի թեման է. Որոշ երկրաչափական մարմինների ավլումների գծագրեր:
Դասի ընթացքում մենք պետք է ինքնուրույն սովորենք, թե ինչպես բացել որոշ երկրաչափական մարմիններ:
Մակերեւութային բացվածքների հաճախ հանդիպում ենք առօրյա կյանքում, արտադրության մեջ, շինարարության մեջ։ Հյութի, քաղցրավենիքի, օծանելիքի, տոնական տուփի կամ պայուսակի և այլնի համար փաթեթավորում պատրաստելու համար պետք է երկրաչափական մարմինների մակերևույթները մաքրել:
Դիտարկենք բացված փաթեթները և ասա ինձ, թե ինչ երկրաչափական ձևերից են դրանք բաղկացած:
Իսկ ի՞նչ է ավլումը: Բացենք 63-րդ էջի դասագրքերը և կարդանք սահմանումը։
Իսկ հիմա ես ձեզ ցույց կտամ որոշ երկրաչափական մարմինների բացման կարգը։
Բուրգի մակերեսի զարգացումը.
Փաթաթելու համար եկեք որոշենք, թե ինչ ձևերից է բաղկացած բուրգը։
Բուրգի կողային մակերեսը բաղկացած է չորս հավասար եռանկյուններից։ Եռանկյուն կառուցելու համար անհրաժեշտ է իմանալ դրա կողմերի չափերը: Բուրգի հավասար եզրերը ծառայում են որպես երեսների (եռանկյունների) կողմեր: Կամայական կետից մենք նկարագրում ենք մի աղեղ, որի շառավիղը հավասար է բուրգի կողային եզրի երկարությանը: Այս աղեղի վրա մենք մի կողմ ենք դնում չորս հատված, որը հավասար է հիմքի կողմին: Ծայրահեղ կետերը ուղիղ գծերով միացնում ենք նկարագրված աղեղի կենտրոնով։ Այնուհետև ամրացնում ենք բուրգի հիմքին հավասար քառակուսի։
Գլանների մակերեսների վերամշակում:
Մխոցի կողային մակերեսի զարգացումը բաղկացած է ուղղանկյունից և երկու շրջանից։ Ուղղանկյան մի կողմը հավասար է մխոցի բարձրությանը, մյուսը հիմքի շրջագիծն է։
Շրջագիծը հաշվարկվում է բանաձևով՝ L= Pi*D։
Մաքրման գծագրում ուղղանկյունին ամրացված են երկու շրջան, որոնց տրամագիծը հավասար է գլանների հիմքի տրամագծին։
Շերտերի գծագրեր կատարելիս գործչի պատկերի վերևում կիրառվում է նշան.
Ծալովի գծերը պետք է գծել երկու կետ ունեցող գծիկներով:
Ամեն ինչ պարզ է? Նոր նյութը համախմբելու համար մենք զույգերով գործնական աշխատանք կկատարենք քարտերի վրա։ Եվ տախտակի մոտ գտնվող մեկը կբացի խորանարդը:

4. Գործնական աշխատանք զույգերով.Նախքան աշխատանքը սկսելը, խնդրում եմ, ասեք, թե ինչ գործիքներով և ինչ նյութով եք աշխատելու։
5. Ամփոփում.
Ի՞նչ նոր բան սովորեցիք դասում:
Ինչի՞ հետ հանդիպեցիք։
Որտե՞ղ են դրանք կիրառվում:
Ի՞նչ ես սովորել։
6. Անդրադարձ.
Ձեզ դուր եկավ դասը:
Գո՞հ եք դասարանում ձեր աշխատանքից:
Ձեր գրասեղանին էմոցիոններ ունեք:
Ընտրեք էմոցիան, որը համապատասխանում է դասի ձեր աշխատանքի գնահատմանը։
7. Սովորողների գնահատում.
Ես շնորհակալ եմ ձեզ դասի համար, այն բանի համար, որ լավ եք արել: Հուսով եմ, որ ձեր հետաքրքրությունը նկարչություն սովորելու նկատմամբ չի մարի։
Ցտեսություն!
Առաջադրանքի քարտ.Մխոցների մշակում (էջ 65. նկ. 137):
Բարձրությունը H = 40 մմ, D = 40 մմ:

Առաջադրանքի քարտ.Բուրգի զարգացում (էջ 64. Նկ. 134):
50 մմ, A = 40 մմ:
Առաջադրանքի քարտ.Եռանկյուն պրիզմայի մշակում (էջ 65. նկ. 136):
Պրիզմայի բարձրությունը H = 40 մմ, հիմքի կողմը A = 30 մմ

Առաջադրանքի քարտ. Cube մշակում (էջ 64. նկ. 132):
A խորանարդի կողմը = 30 մմ:

Ներածման ամսաթիվ 1974-07-01
Սույն ստանդարտը սահմանում է արդյունաբերության բոլոր ճյուղերի համար աշխատանքային փաստաթղթերի մշակման փուլում մասերի, հավաքման, ընդհանուր և մոնտաժային գծագրերի կատարման հիմնական պահանջները:
(Փոփոխված հրատարակություն, Rev. No. 8,).
1. ԸՆԴՀԱՆՈՒՐ ՊԱՀԱՆՋՆԵՐ ԱՇԽԱՏԱՆՔԱՅԻՆ ԳԾԱԳՐԵՐԻՆ
1.1. Ընդհանուր դրույթներ
1.1.1. Աշխատանքային գծագրեր մշակելիս տրամադրեք.
ա) ստանդարտ և գնված արտադրանքի, ինչպես նաև արտադրության մեջ յուրացված և տեխնոլոգիային համապատասխանող արտադրանքի օպտիմալ օգտագործումը.
բ) թելերի, թելերի և այլ կառուցվածքային տարրերի ռացիոնալ սահմանափակ շրջանակ, դրանց չափսեր, ծածկույթներ և այլն.
գ) նյութերի դասակարգերի և տեսականու ռացիոնալ սահմանափակ շրջանակ, ինչպես նաև ամենաէժան և քիչ սակավ նյութերի օգտագործումը.
դ) փոխարինելիության անհրաժեշտ աստիճանը, արտադրանքի արտադրության և վերանորոգման առավել շահավետ եղանակները, ինչպես նաև շահագործման ընթացքում դրանց պահպանման առավելագույն հեշտությունը:
1.1.1 ա. Թղթի վրա աշխատանքային գծագրերը (թղթային ձևով) և էլեկտրոնային գծագրերը կարող են կատարվել մասի էլեկտրոնային մոդելի և հավաքման միավորի էլեկտրոնային մոդելի հիման վրա ( ԳՕՍՏ2.052).
Էլեկտրոնային փաստաթղթերի ընդհանուր պահանջներ - ԳՕՍՏ2.051-ի համաձայն
1.1.2. Սերիական և զանգվածային արտադրության արտադրանքի գծագրերում տեխնիկական բնութագրերին հղումներ կատարելիս վերջիններս պետք է գրանցվեն սահմանված կարգով (այն պետություններում, որտեղ տեխնիկական բնութագրերի պետական գրանցումը պարտադիր է):
Թույլատրվում է հղում կատարել տեխնոլոգիական հրահանգներին, երբ սույն հրահանգներով սահմանված պահանջները միակն են, որոնք երաշխավորում են արտադրանքի պահանջվող որակը. միևնույն ժամանակ, դրանք պետք է կցվեն արտադրանքի նախագծային փաստաթղթերի փաթեթին, երբ այն փոխանցվում է այլ ձեռնարկության:
Չի թույլատրվում հղումներ տալ փաստաթղթերին, որոնք որոշում են արտադրանքի կառուցվածքային տարրերի ձևն ու չափերը (փեղկեր, ակոսներ և այլն), եթե համապատասխան ստանդարտներում այդ տարրերի խորհրդանիշ չկա: Դրանց արտադրության բոլոր տվյալները պետք է տրվեն գծագրերի վրա:
(Փոփոխված հրատարակություն, Rev. No. 4, 10,).
1.1.3. Աշխատանքային գծագրերի վրա չի թույլատրվում տեղադրել տեխնոլոգիական հրահանգներ։ Բացառության կարգով թույլատրվում է.
ա) նշեք արտադրության և հսկողության մեթոդները, եթե դրանք միակն են, որոնք երաշխավորում են արտադրանքի պահանջվող որակը, օրինակ՝ համատեղ մշակումը, հոդերի թեքումը կամ ընդլայնումը և այլն.
բ) ցուցումներ տալ տեխնոլոգիական մշակման (ձուլվածքներ, դարբնոցներ և այլն) տեսակի ընտրության վերաբերյալ.
գ) նշեք որոշակի տեխնոլոգիական մեթոդ, որը երաշխավորում է արտադրանքի համար որոշակի տեխնիկական պահանջների ապահովում, որոնք չեն կարող արտահայտվել օբյեկտիվ ցուցիչներով կամ քանակներով, օրինակ՝ ծերացման գործընթացը, վակուումային ներծծումը, սոսնձման տեխնոլոգիան, կառավարումը, մխոցային զույգի զուգավորումը և այլն։ .
1.1.4. Հիմնական միավորի * և օժանդակ արտադրության արտադրանքի համար, որոշակի ձեռնարկությունում օգտագործման համար նախատեսված գծագրերի վրա, թույլատրվում է տեղադրել տարբեր հրահանգներ արտադրության տեխնոլոգիայի և արտադրանքի վերահսկման վերաբերյալ:
*Մեկ արտադրության արտադրանքի գծագրերի կատարման կանոնները կիրառվում են նաև օժանդակ արտադրության վրա:
1.1.6. Պայմանական նշանների չափերը, որոնք սահմանված չեն ստանդարտներում, որոշվում են՝ հաշվի առնելով գծագրի տեսանելիությունն ու պարզությունը և կրկնվող կրկնությամբ պահպանվում են նույնը:
1.1.7. Արտադրանքի աշխատանքային գծագրում նշեք չափերը, առավելագույն շեղումները, մակերևույթի կոշտությունը և այլ տվյալներ, որոնք այն պետք է համապատասխանի մինչև հավաքումը (նկ. ա).
Բացառություն է պարբերությունում նշված դեպքը:
Հավաքման գործընթացում կամ դրանից հետո մշակման արդյունքում ստացված արտադրանքի տարրերի չափերը, առավելագույն շեղումները և մակերեսային կոշտությունը նշված են հավաքման գծագրում (նկ. բ).
1.1.14. Եթե եզրը (եզրը) պետք է լինի սուր կամ կլորացված, ապա գծագրի վրա տեղադրվում է համապատասխան նշում: Եթե եզրերի կամ կողերի ձևի գծագրում որևէ նշում չկա, ապա դրանք պետք է բթացվեն:
Անհրաժեշտության դեպքում այս դեպքում կարող եք նշել «∟» նշանի կողքին դրված բութի չափը (փեղկ, շառավիղ), օրինակ՝ դժոխք։ .
(Փոփոխված հրատարակություն, Rev. No. 9):
1.2.6. Արտադրանքի գծագրին, որը ստացվել է մշակված մասի մասերի կտրելով և ըստ ներկայացված գծագրի փոխարինելի այլ մշակման մասերից պատրաստված որևէ այլ արտադրանքի հետ, մշակված մասի պատկերը տեղադրված չէ (նկ.):
1.2.7. Աշխատանքային մասը մասերի կտրելու կամ երկու կամ ավելի համատեղ մշակված մասերից բաղկացած արտադրանքի համար, որոնք օգտագործվում են միայն համատեղ և չեն փոխարինվում նույն արտադրանքի մյուս մասերի հետ, մշակվում է մեկ գծագիր (գծագիր):
1.3. Լրացուցիչ վերամշակմամբ կամ փոփոխությամբ ապրանքների գծագրեր
1.3.1. Այլ ապրանքների լրացուցիչ վերամշակմամբ արտադրված արտադրանքի գծագրերը կատարվում են հաշվի առնելով հետևյալ պահանջները.
ա) դատարկ արտադրանքը պատկերված է ամուր բարակ գծերով, լրացուցիչ մշակման արդյունքում ստացված մակերեսները, նոր ներմուծված արտադրանքները և առկաների փոխարեն տեղադրված արտադրանքները՝ ամուր հիմնական գծերով.
Փոփոխության ժամանակ հեռացված մասերը պատկերված չեն.
բ) կիրառել միայն այն չափերը, առավելագույն շեղումները և մակերեսի կոշտության նշանակումները, որոնք անհրաժեշտ են լրացուցիչ մշակման համար (նկ.):
Թույլատրվում է կիրառել հղման, ընդհանուր և միացնող չափսեր, թույլատրվում է պատկերել աշխատանքային մասի միայն մի մասը, որի տարրերը պետք է լրացուցիչ մշակվեն:
1.3.2. Աշխատանքային մասի լրացուցիչ մշակմամբ պատրաստված մասի գծագրում՝ սյունակում 3 հիմնական մակագրությունը գրել բառը « աշխատանքային մաս» և աշխատանքային մասի նշանակումը:
Գնված ապրանքը որպես դատարկ ապրանք օգտագործելիս հիմնական մակագրության 3-րդ սյունակում նշվում է գնված ապրանքի անվանումը և դրա անվանումը, որոնք պարունակվում են արտադրողի (մատակարարի) ուղեկցող փաստաթղթերում:
(Փոփոխված հրատարակություն, Rev. No 11)
Ժողովի գծանկար

Մանրամասն գծագրեր
Տարբերակներում ներառված բաղկացուցիչ մասերի դիրքերը խանգարում են համապատասխան լրացուցիչ պատկերներին (նկ.):
3.3.14. Այն դեպքերում, երբ գնված արտադրանքի առանձին մասերը տեղադրվում են արտադրանքի հավաքման տարբեր ագրեգատներում (օրինակ, կոնաձև գլան առանցքակալներ), գնված ապրանքը գրանցվում է հավաքման միավորի ճշգրտման մեջ, որում այն ներառված է հավաքված ձևի մեջ: Մշակվող արտադրանքի հավաքման գծագրի տեխնիկական պահանջները ցույց են տալիս այն հավաքման միավորները, որոնք ներառում են գնված արտադրանքի առանձին մասեր: Այս հավաքման ստորաբաժանումների բնութագրերում «Ծանոթագրություն» սյունակում նշվում է հստակեցման նշումը, որը ներառում է գնված ապրանքը հավաքված տեսքով: Միևնույն ժամանակ, «Անուն» սյունակում նշեք գնված ապրանքի բաղադրիչի անվանումը, իսկ «Համարը» սյունակում: լրացված չէ.
(Լրացուցիչ ներկայացվում է Փոփոխություն թիվ 8):
4. ՈՒՐՎԱԳԻՐՆԵՐ
4.1. Չափային գծագրերը նախատեսված չեն դրանցից արտադրանքի արտադրության համար և չպետք է պարունակեն տվյալներ արտադրության և հավաքման համար:
4.2. Չափային գծագրի վրա արտադրանքի պատկերը կատարվում է առավելագույն պարզեցումներով: Արտադրանքը պատկերված է այնպես, որ երևում են շարժվող, քաշվող կամ ծալվող մասերի, լծակների, վագոնների, կախովի ծածկոցների և այլնի ծայրահեղ դիրքերը։
Թույլատրվում է չցուցադրել տարրեր, որոնք դուրս են գալիս հիմնական եզրագծից այն կողմ՝ ապրանքի չափսերի համեմատ փոքր քանակությամբ:
4.3. Չափային գծագրի վրա դիտումների քանակը պետք է լինի նվազագույն, բայց բավարար՝ արտադրանքի արտաքին ուրվագծերի, դրա ցցված մասերի դիրքերի (լծակներ, թռչող անիվներ, բռնակներ, կոճակներ և այլն), տարրերի մասին համապարփակ պատկերացում տալու համար։ որը պետք է մշտապես տեսանելի լինի (օրինակ՝ կշեռքներ), ապրանքի այլ ապրանքների հետ հաղորդակցման տարրերի գտնվելու վայրի մասին։
4.4. Ծավալային գծագրի վրա արտադրանքի պատկերը կազմված է ամուր հիմնական գծերով, իսկ ծայրահեղ դիրքերում շարժվող մասերի ուրվագծերը գծիկավոր բարակ գծեր են՝ երկու կետով։
Թույլատրվում է շարժվող մասերի ծայրահեղ դիրքերը պատկերել առանձին տեսարանների վրա։
(Փոփոխված հրատարակություն, Rev. No. 3):
4.5. Ծավալային գծագրի վրա թույլատրվում է պատկերել մասերը և հավաքման միավորները, որոնք արտադրանքի մաս չեն կազմում, որպես ամուր բարակ գծեր:
4.6. Չափային գծագրի վրա կիրառվում են արտադրանքի ընդհանուր չափերը, տեղադրման և միացման չափերը և, անհրաժեշտության դեպքում, չափերը, որոնք որոշում են ցցված մասերի դիրքը:
Մոնտաժման և միացման չափերը, որոնք անհրաժեշտ են այլ ապրանքների հետ կապելու համար, պետք է նշվեն առավելագույն շեղումներով: Թույլատրվում է նշել զանգվածի կենտրոնի կոորդինատները։ Չափային գծագիրը չի նշում, որ դրա վրա տրված բոլոր չափերը հղման համար են:
(Փոփոխված հրատարակություն, Rev. No 8):
4.7. Ծավալային գծագրի վրա թույլատրվում է նշել արտադրանքի օգտագործման, պահպանման, փոխադրման և շահագործման պայմանները տեխնիկական նկարագրության, բնութագրերի կամ արտադրանքի այլ նախագծային փաստաթղթում այդ տվյալների բացակայության դեպքում:
4.8. Չափային գծագրի օրինակը ներկայացված է Նկ. .
5.8. Տեղադրման համար անհրաժեշտ ապրանքները և մոնտաժվող արտադրանքի կողմից չտրամադրված նյութերը գրանցվում են տեղադրման գծագրի ցանկում, իսկ «Ծանոթագրություն» սյունակում կամ տեխնիկական պահանջներում տեղադրվում է համապատասխան նշում, օրինակ՝ «Pos. 7 և 9 ապրանքը չի մատակարարվում» և այլն:
Եթե անհնար է նշել չմատակարարված ապրանքների ճշգրիտ անվանումները և անվանումները, ապա ցուցակում նշվում են դրանց ցուցիչ անվանումները, իսկ գծագրում, անհրաժեշտության դեպքում, չափերը և այլ տվյալներ, որոնք ապահովում են տեղադրման համար անհրաժեշտ ապրանքների ճիշտ ընտրությունը:
5.9. Տեղադրման գծագրի վրա, առաջատար գծի դարակում կամ ուղղակիորեն պատկերի վրա, նշեք սարքի (օբյեկտի) կամ սարքի մի մասի անվանումը և (կամ) նշանակումը, որին կցված է մոնտաժված արտադրանքը:
ՏԵՂԵԿԱՏՎԱԿԱՆ ՏՎՅԱԼՆԵՐ
1. ՄՇԱԿՎԱԾ ԵՎ ՆԵՐԴՐՎԱԾ ԷԽՍՀՄ Մինիստրների խորհրդի ստանդարտների պետական կոմիտե
2. ՀԱՍՏԱՏՎԵԼ ԵՎ ՆԵՐԴՐՎԵԼ ԷԳՈՐԾՈՂՈՒԹՅՈՒՆ ԽՍՀՄ Մինիստրների խորհրդի ստանդարտների պետական կոմիտեի 27.07.73 թիվ 1843 հրամանագրով.
Թիվ 9 փոփոխությունն ընդունվել է Ստանդարտացման, չափագիտության և հավաստագրման միջպետական խորհրդի կողմից (28.05.98 թիվ 13 արձանագրություն)
Գրանցված է IGU-ի թիվ 2907 տեխնիկական քարտուղարության կողմից
| Պետության անվանումը | |
| Բելառուսի Հանրապետություն | |
| Ղազախստանի Հանրապետություն | |
| Ղրղզստանի Հանրապետություն | Ղրղզստանի ստանդարտ |
| Մոլդովայի Հանրապետություն | Մոլդովական ստանդարտ |
| Ռուսաստանի Դաշնություն | Ռուսաստանի Գոստանդարտ |
| Տաջիկստանի Հանրապետություն | Տաջիկստանի ստանդարտ |
| Թուրքմենստան | |
| Ուզբեկստանի Հանրապետություն | Ուզգոստանդարտ |
| Ուկրաինայի պետական ստանդարտ |
Թիվ 10 փոփոխությունն ընդունվել է Ստանդարտացման, չափագիտության և հավաստագրման միջպետական խորհրդի կողմից (թիվ 17 արձանագրություն 22.06.2000թ.)
Գրանցված է IGU-ի թիվ 3526 տեխնիկական քարտուղարության կողմից
| Պետության անվանումը | Ստանդարտացման ազգային մարմնի անվանումը |
| Ադրբեջանի Հանրապետություն | Ազգոստանդարտ |
| Բելառուսի Հանրապետություն | Բելառուսի Հանրապետության պետական ստանդարտ |
| Gruzstandard |
|
| Ղազախստանի Հանրապետություն | Ղազախստանի Հանրապետության պետական ստանդարտ |
| Ղրղզստանի Հանրապետություն | Ղրղզստանի ստանդարտ |
| Մոլդովայի Հանրապետություն | Մոլդովական ստանդարտ |
| Ռուսաստանի Դաշնություն | Ռուսաստանի Գոստանդարտ |
| Տաջիկստանի Հանրապետություն | Տաջիկստանի ստանդարտ |
| Թուրքմենստան | «Թուրքմենստանստանտարտարի» գլխավոր պետական ծառայություն |
3. ԳՕՍՏ 2.107-68 ԳՕՍՏ 2.109-68, ԳՕՍՏ 5292-60-ի ՓՈԽԱՐԵՆ Վ. VIII
4. Հղված ԿԱՆՈՆԱԿԱՐԳՆԵՐ ԵՎ ՏԵԽՆԻԿԱԿԱՆ ՓԱՍՏԱԹՂԹԵՐ
(Փոփոխված հրատարակություն, Rev. No 11)
5. ԽՐԱՏԱՐԱԿՈՒԹՅՈՒՆ (Հունիս 2002) Փոփոխություններով թիվ 1, 2, 3,4, 5, 6, 7, 8, 9, 10, հաստատված 1980 թվականի փետրվարին, 1981 թվականի նոյեմբերին, 1984 թվականի մայիսին, 1984 թվականի դեկտեմբերին, 1985 թվականի մարտ, 1985 թվականի սեպտեմբեր, Մարտ 1986, Սեպտեմբեր 1987, Փետրվար 1999, Դեկտեմբեր 2000 (IUS No. 4-80, 4-82, 8-84, 3-85, 5-85,12-85, 6-86, 12-87, 5-99 , 3-2001)
Բազմեյդրոնի մակերևույթի զարգացումը կոչվում է հարթ պատկեր, որը ստացվում է նրա բոլոր երեսների հարթության հետ համակցվելուց։ Երեսապատ մակերեսների տեղադրումն իրականացվում է մասերի արտադրության մեջ թերթային նյութի կտրում կամ տարբեր նյութերով պատված մասերի մակերեսը որոշելու համար: Տարածքը որոշելը կարևոր է տարբեր ծածկույթների համար՝ ինչպես դեկորատիվ նպատակներով, այնպես էլ մակերեսին որոշակի հատկություններ հաղորդելու նպատակով, ինչպիսիք են էլեկտրական հաղորդունակության բարձրացումը, ինչպես նաև մակերևույթի քիմիական մշակման տարբեր մեթոդների համար:
Երեսապատ մակերեսի զարգացում կառուցելու համար անհրաժեշտ է որոշել դրա երեսների չափերը: Նկատի ունեցեք, որ պոլիէդրոնի ցանկացած երեսի կառուցումը կարելի է անել՝ այն եռանկյունների բաժանելով։ Եռանկյան կողմերի երկարությունը, իր հերթին, կարող է որոշվել հայտնի մեթոդներից որևէ մեկով։
Բուրգի մակերեսային զարգացում. Բուրգի կողային մակերեսի կառուցումը կարող է իրականացվել հետևյալ հաջորդականությամբ.
որոշել բուրգի հիմքի եզրերի և կողմերի երկարությունը. կատարել ավլելու գծանկար՝ եռանկյունների՝ բուրգի երեսների հաջորդական կառուցմամբ:
Եռանկյունաձև բուրգի SABC մակերեսի մշակման կառուցման օրինակ ցույց է տրված 6.14 և 6.15 նկարներում: Նկար 6.14-ում կառուցման հարմարության համար բուրգի կողային եզրերը երկարացվում են մինչև հարթության խաչմերուկը:Ն. Սա հնարավորություն տվեց որոշել հատվածների երկարությունը հորիզոնական պրոյեկցիայի վրա 1-2, 2-3, 3-4 բուրգի նոր հիմքը. Կողքի երկարությունը S-l, S-2, S-3 հայտնաբերվել է դրանք ուղղահայաց առանցքի շուրջ պտտելով՝ հատվածներ s"1 1", s"2 1", s"3 1". Նրանք գտան հատվածներ s"a 1", s"b 1", s"c 1". Նկար 6.15-ում հայտնաբերված հատվածների հիման վրա կառուցվել է կողային մակերեսի մաքրում Solo2o3o1o և ապա S 0 A 0 BoCoAo: A 0 C 0 հատվածի վրա կառուցեց եռանկյունու իրական չափը A 0 B 0 C 0 կողմերի վրա A 0 B 0 և C0B0, հայտնաբերված ուղղանկյուն եռանկյունու մեթոդը (տես նկ. 2.9):
Պրիզմատիկ մակերեսի զարգացում կառուցելը կարող է արտադրվել մի քանի եղանակով՝ նորմալ հատված, եռանկյուններ։
Նորմալ հատվածի մեթոդով նպատակահարմար է կառուցել պրիզմատիկ մակերևույթի զարգացում հետևյալ հաջորդականությամբ (նկ. 6.16).
պրիզմատիկ մակերեսը հատում են նրա եզրերին ուղղահայաց օժանդակ հարթությամբ (P ուղղահայաց 1-2;նորմալ հատված);
ընդլայնել կառուցված բազմագիծը (А0В0С0D0) Օժանդակ հարթության հատումը պրիզմատիկ մակերեսի հետ՝ որոշելով նրա հատվածների երկարությունը (А0B0, B 0 C 0, C 0 D 0);
ընդլայնված հատման գծին (A0D0) ուղղահայացների վրա, մի կողմ դնել պրիզմատիկ մակերևույթի եզրերի հատվածների երկարությունը. (A 0 2 0, BoZo, Bo4o, Co5o, Co6o, Do7o, Do8o)և դրանց ծայրերը միացրեք ուղիղ գծերով:
Գծապատկերում թեքված պրիզմայի կողային մակերևույթի մաքրման կառուցման օրինակ ներկայացված է 6.17 և 6.18 նկարներում: Օժանդակ ինքնաթիռ P կառուցելու համար, պրիզմայի եզրերին ուղղահայաց, ընտրվում է լրացուցիչ պրոյեկցիոն հարթությունՏ, պրիզմայի եզրերին զուգահեռ և հարթությանը ուղղահայացՆ. Օժանդակ ինքնաթիռР-ն տրված է հետևյալ P t-ով պրոյեկցիոն հարթության վրա T S (pl. S ուղղահայաց T):
Եռանկյունների մեթոդի համաձայն, պրիզմատիկ մակերեսի զարգացումը հետևյալն է. քառանկյունները (դեմքերը) անկյունագծերով բաժանվում են եռանկյունների; որոշել եռանկյունների կողմերի երկարությունները; կատարել ավլման նկար՝ հաջորդաբար կառուցելով եռանկյուններ, որոնց վրա բաժանված են դեմքերը:
Բենզոլը չհագեցած միացություն է, սակայն մենք պարզեցինք, որ նրա կառուցվածքում չկան կրկնակի կապեր, այլ արոմատիկ կապ՝ ապատեղայնացված էլեկտրոնային ամպ: Չհագեցած ածխաջրածինների տիպիկ ռեակցիաները՝ էլեկտրոֆիլ հավելումը և օքսիդացումը, բնորոշ չեն բենզոլին։ Այսպիսով, այն չի գունաթափում բրոմային ջուրը, չի տալիս Վագների ռեակցիա (օքսիդացում կալիումի պերմանգանատի լուծույթով սենյակային ջերմաստիճանում): Բենզոլը բնութագրվում է ռեակցիաներով, որոնք չեն հանգեցնում փակ կոնյուգացիոն համակարգի խախտման՝ փոխարինման ռեակցիաներին։ Պարզելու համար, թե ինչ տեսակի փոխարինում (արմատական, էլեկտրոֆիլ, նուկլեոֆիլ) է բնորոշ բենզոլին, հիշեք նրա էլեկտրոնային կառուցվածքը՝ մոլեկուլի σ-կմախքը հարթ է, իսկ հարթության վերևում և ներքևում տեղակայված է արոմատիկ ամպ։ Այս անուշաբույր ամպի հետ փոխազդելու համար ռեագենտը պետք է լինի էլեկտրոֆիլ: Այսպիսով, բենզոլի (և առհասարակ անուշաբույր միացությունների համար) էլեկտրոֆիլային փոխարինման ռեակցիաներ . S E ռեակցիաների օրինակներ են.
Առաջին փուլում էլեկտրոֆիլը մոտենում է բենզոլի մոլեկուլին և փոխազդում է ամբողջ անուշաբույր ամպի հետ (նրանք ձգվում են դեպի միմյանց)։ Ձևավորվել է π-համալիր. Նոր ածխածին-էլեկտրոֆիլ կովալենտային կապ ստեղծելու համար անհրաժեշտ է զույգ էլեկտրոններ։ Էլեկտրոֆիլն այն դուրս է հանում անուշաբույր ամպից՝ առաջանալով σ-բարդ. Դա փակ կոնյուգացիոն համակարգ չէ, քանի որ ածխածնի ատոմը, որը ձևավորեց նոր σ-կապը, անցավ sp 3 հիբրիդացման (այն դուրս եկավ հարթությունից և այլևս չունի ոչ հիբրիդային p z ուղեծիր): Մնացած հինգ ածխածնի ատոմները շարունակում են մասնակցել խոնարհմանը` ձևավորելով ընդհանուր էլեկտրոնային ամպ, որի մեջ չորս էլեկտրոն տեղակայվում են (6-2=4), ուստի σ-համալիրում դրական լիցքը նշված է ոչ թե կոնկրետ ածխածնի ատոմի վրա, այլ բաց ռինգի կենտրոնը: Այսպիսով, σ-համալիրը անուշաբույր կառուցվածք չէ։ Արոմատիկությունը վերականգնելու համար այն պետք է պառակտել ջրածնի պրոտոնը (H +): Այն ընդունվում է ռեակցիայի միջավայրում մնացած նուկլեոֆիլով (Nu -): Երկու C-H կապի էլեկտրոնները վերադառնում են արոմատիկ ամպ, ածխածնի ատոմը կրկին դառնում է
sp 2 - հիբրիդացված և կարող է մասնակցել խոնարհմանը:
Էլեկտրաֆիլ փոխարինող ռեակցիայի արագությունը սահմանափակող փուլը σ-համալիրի առաջացման փուլն է, քանի որ. այս դեպքում առաջանում է բուրավետության կորուստ, որը պահանջում է էներգիայի ծախս:
Բենզոլում էլեկտրոֆիլ փոխարինման տարբեր ռեակցիաներն ընթանում են ընդհանուր մեխանիզմի համաձայն և տարբերվում են միայն էլեկտրոֆիլ մասնիկի առաջացման փուլում։
Նիտրացիոն ռեակցիաբենզոլը առաջանում է խտացված ազոտական և ծծմբական թթուների խառնուրդի ազդեցության տակ (տես վերևում գտնվող ռեակցիայի սխեման): Դիտարկենք դրա մեխանիզմը.
 |
Ռեակցիայի առաջին փուլում ազոտական թթուն փոխազդում է ծծմբաթթվի հետ։ Այս դեպքում ազոտաթթուն հանդես է գալիս որպես հիմք՝ ընդունելով պրոտոն ծծմբաթթվի մոլեկուլից (ըստ Բրոնսթեդի տեսության՝ թթուն մոլեկուլ կամ իոն է, որը տալիս է պրոտոն, իսկ հիմքը՝ մոլեկուլ կամ իոն, որն ընդունում է ջրածնի պրոտոնը։ ) Ձևավորվում է պրոտոնացված ազոտաթթու, որը, պառակտելով ջրի մոլեկուլը, վերածվում է նիտրոնիումի կատիոնի կամ նիտրոնիումի կատիոնի։ Սա էլեկտրոֆիլ մասնիկն է։ Այսպիսով, ծծմբաթթուն հանդես է գալիս որպես կատալիզատոր՝ մասնակցելով էլեկտրոֆիլ ռեագենտի ձևավորմանը։ Ծծմբաթթվի երկրորդ դերը ջրազրկող նյութի դերն է: Ջուրը պետք է հեռացվի ռեակցիայի ոլորտից, որպեսզի նրա հավասարակշռությունը տեղափոխվի աջ։
Էլեկտրաֆիլի՝ նիտրոնի կատիոնի ձևավորումից հետո ռեակցիան ընթանում է ընդհանուր մեխանիզմի համաձայն՝ π- և ձևավորմամբ։
σ-համալիրներ:
Խնդրում ենք նկատի ունենալ. σ-համալիրը նիտրոբենզոլի փոխակերպման փուլում (արոմատիկության վերականգնման փուլ) ծծմբաթթվի անիոնի ազդեցության տակ ջրածնի պրոտոնը բաժանվում է, մինչդեռ ծծմբաթթուն նորից ձևավորվում է, ինչը վկայում է, որ. դա այս ռեակցիայի կատալիզատորն էր:
 Կատալիզատոր հալոգենացման ռեակցիաներայսպես կոչված Լյուիս թթուներն են (ըստ Լյուիսի տեսության՝ թթուները չեզոք մոլեկուլներ կամ իոններ են, որոնք ընդունակ են ընդունել զույգ էլեկտրոններ)՝ FeCl 3, FeBr 3, AlCl 3, AlBr 3 և այլն։ Հալոգենի մոլեկուլը բևեռացնելու համար անհրաժեշտ է կատալիզատոր: Լյուիս թթուն տեղափոխում է քլորի միայնակ էլեկտրոնային զույգը իր վրա՝ ձևավորելով մի համալիր, որում մասնակի դրական լիցքը կենտրոնացած է քլորի ատոմներից մեկի վրա.
Կատալիզատոր հալոգենացման ռեակցիաներայսպես կոչված Լյուիս թթուներն են (ըստ Լյուիսի տեսության՝ թթուները չեզոք մոլեկուլներ կամ իոններ են, որոնք ընդունակ են ընդունել զույգ էլեկտրոններ)՝ FeCl 3, FeBr 3, AlCl 3, AlBr 3 և այլն։ Հալոգենի մոլեկուլը բևեռացնելու համար անհրաժեշտ է կատալիզատոր: Լյուիս թթուն տեղափոխում է քլորի միայնակ էլեկտրոնային զույգը իր վրա՝ ձևավորելով մի համալիր, որում մասնակի դրական լիցքը կենտրոնացած է քլորի ատոմներից մեկի վրա.
π-համալիրի առաջացման փուլում տեղի է ունենում Cl-Cl կապի հետագա բևեռացում, և այն քայքայվում է հետերոլիտիկորեն, և Cl + անմիջապես մասնակցում է σ-համալիրի առաջացմանը։
 շարունակել նույն կերպ ալկիլացման ռեակցիաներ(Friedel-Crafts-ի ռեակցիա):
շարունակել նույն կերպ ալկիլացման ռեակցիաներ(Friedel-Crafts-ի ռեակցիա):
 |
Մեթիլքլորիդում C-Cl կապը բավականաչափ բևեռային չէ հետերոլիտիկ կերպով կոտրելու համար: Լյուիս թթվի ազդեցության տակ ածխածնի ատոմի մասնակի դրական լիցքը մեծանում է, և կատալիզատորի հետ ռեակտիվ նյութի կոմպլեքսը ավելի ուժեղ էլեկտրոֆիլ է, քան սկզբնական մեթիլքլորիդը։
Սուլֆոնացման ռեակցիաբենզոլը առաջանում է օլեումի ազդեցության ներքո (ծծմբային անհիդրիդ SO 3 լուծույթ խտացված ծծմբաթթվի մեջ):
Ծծմբի անհիդրիդի մոլեկուլը էլեկտրոֆիլ է ծծմբի ատոմի մեծ մասնակի դրական լիցքի պատճառով:
 |
Երբ π-կոմպլեքս է գոյանում, S=O կապը (առաջին հերթին՝ π-կապը) բևեռացվում և կոտրվում է հետերոլիտիկ ձևով, հետևաբար, երբ գոյանում է σ-կոմպլեքս, թթվածնի վրա առաջանում է ընդհանուր բացասական լիցք: ատոմ. Արոմատիկությունը վերականգնելու համար ջրածնի պրոտոնը բաժանվում է օղակի ածխածնի ատոմից և անցնում դեպի բացասական լիցքավորված թթվածին։ Առաջանում է բենզոլսուլֆոնաթթու։
Երբ դիտարկում ենք բենզոլում էլեկտրոֆիլ փոխարինող ռեակցիաները, մեզ չի սպառնում այն հարցը, թե որ դիրքում է տեղի ունենում ռեակցիան, քանի որ. Ածխածնի բոլոր ատոմները բացարձակապես հավասար են։ Մեկ այլ բան, եթե բենզոլային օղակն արդեն ունի փոխարինող: Այս դեպքում էլեկտրոֆիլ փոխարինման արդյունքում սկզբունքորեն հնարավոր է երեք իզոմերների ձևավորում.
 |
Հարցին պատասխանելու համար, թե այս հնարավոր արտադրանքներից որն է գերակշռող, անհրաժեշտ է հաշվի առնել փոխարինողի էլեկտրոնային ազդեցությունը:
Եկեք շեղվենք բենզոլի և նրա ածանցյալների էլեկտրոֆիլ փոխարինման ռեակցիաներից և ընդհանուր առմամբ դիտարկենք էլեկտրոնային ազդեցությունները:
Ատոմների փոխադարձ ազդեցությունը օրգանական մոլեկուլներում
կապեր. Էլեկտրոնային էֆեկտներ
Օրգանական միացությունների մոլեկուլների ատոմներն ու ատոմային խմբերը ազդում են միմյանց վրա, և ոչ միայն միմյանց հետ անմիջականորեն կապված ատոմները: Այս ազդեցությունը ինչ-որ կերպ փոխանցվում է մոլեկուլի միջոցով։ Ատոմների ազդեցության փոխանցումը մոլեկուլներում կապերի բևեռացման պատճառով կոչվում է էլեկտրոնային էֆեկտներ . Էլեկտրոնային էֆեկտների երկու տեսակ կա՝ ինդուկտիվ և մեզոմերական էֆեկտներ:
Ինդուկտիվ ազդեցություն- սա փոխարինողների ազդեցության փոխանցումն է σ-կապերի շղթայի երկայնքով՝ պայմանավորված դրանց բևեռացումով: Ինդուկտիվ էֆեկտը նշվում է I նշանով: Դիտարկենք այն՝ օգտագործելով 1-քլորբուտանի օրինակը.
C-Cl կապը բևեռային է քլորի ավելի բարձր էլեկտրաբացասականության պատճառով: Ածխածնի ատոմի վրա առաջանում է մասնակի դրական լիցք (δ+): Հաջորդ σ կապի էլեկտրոնային զույգը տեղափոխվում է դեպի ածխածնի ատոմի էլեկտրոնների պակասը, այսինքն. բևեռացված. Դրա շնորհիվ մասնակի դրական լիցք (δ + ') առաջանում է նաև հաջորդ ածխածնի ատոմի վրա և այլն։ Այսպիսով, քլոր դրդում էբևեռացումը ոչ միայն «սեփական» σ-կապերի, այլ նաև շղթայի հետագա կապերի։ Խնդրում ենք նկատի ունենալ, որ յուրաքանչյուր հաջորդ մասնակի դրական լիցքը փոքր է նախորդից (δ+>δ+’>δ+’’>δ+’’’), այսինքն. ինդուկտիվ էֆեկտը փոխանցվում է շղթայի միջոցով՝ խոնավացումով: Սա կարելի է բացատրել σ կապերի ցածր բևեռացման հնարավորությունով։ Ընդհանրապես ընդունված է, որ ինդուկտիվ ազդեցությունը տարածվում է 3-4 σ-կապերի վրա։ Տվյալ օրինակում քլորի ատոմը փոխում է էլեկտրոնի խտությունը կապի շղթայի երկայնքով ինքս ինձ. Նման ազդեցությունը կոչվում է բացասական ինդուկտիվ ազդեցություն և նշվում է -I Cl-ով:
Փոխարինիչների մեծ մասը ցուցաբերում է բացասական ինդուկտիվ ազդեցություն, քանի որ դրանց կառուցվածքում կան ատոմներ, որոնք ավելի էլեկտրաբացասական են, քան ջրածինը (ջրածնի ինդուկտիվ ազդեցությունը ենթադրվում է զրո): Օրինակ՝ -F, -Cl, -Br, -I, -OH, -NH 2, -NO 2,
-COOH, >C=O.
 |  |
||
Եթե փոխարինողը տեղափոխում է էլեկտրոնի խտությունը σ-կապերի շղթայի երկայնքով Հրել, այն ցուցաբերում է դրական ինդուկտիվ ազդեցություն (+I): Օրինակ:

Ընդհանուր բացասական լիցքով թթվածինը դրսևորում է դրական ինդուկտիվ ազդեցություն:
![]()
Պրոպենի մոլեկուլում մեթիլ խմբի ածխածինը sp 3-հիբրիդացված է, իսկ կրկնակի կապում ածխածնի ատոմները sp 2-հիբրիդացված են, այսինքն. ավելի էլեկտրաբացասական: Հետևաբար, մեթիլ խումբը հեռացնում է էլեկտրոնի խտությունը իրենից՝ ցույց տալով դրական ինդուկտիվ ազդեցություն (+I CH 3):
Այսպիսով, ինդուկտիվ ազդեցությունը կարող է դրսևորվել ցանկացած մոլեկուլում, որի մեջ կան տարբեր էլեկտրաբացասականության ատոմներ։
մեզոմերային ազդեցություն- սա փոխարինողների էլեկտրոնային ազդեցության փոխանցումն է խոնարհված համակարգերում, π կապերի բևեռացման միջոցով: Մեզոմերային էֆեկտը փոխանցվում է առանց թուլացման, քանի որ π կապերը հեշտությամբ բևեռացվում են: Խնդրում ենք նկատի ունենալ. միայն այն փոխարինիչները, որոնք իրենք են հանդիսանում խոնարհված համակարգի մաս, ունեն մեզոմերային ազդեցություն: Օրինակ:
Մեզոմերային էֆեկտը կարող է լինել և՛ դրական (+M), և՛ բացասական (-M):
Վինիլքլորիդի մոլեկուլում քլորի չկիսված էլեկտրոնային զույգը մասնակցում է p, π-կոնյուգացիայի, այսինքն. Քլորի ներդրումը զուգակցված համակարգում ավելի մեծ է, քան ածխածնի յուրաքանչյուր ատոմինը: Հետևաբար, քլորը դրսևորում է դրական մեզոմերային ազդեցություն:
 Ակրիլային ալդեհիդի մոլեկուլն է
Ակրիլային ալդեհիդի մոլեկուլն է
π.π-կոնյուգացիոն համակարգ. Թթվածնի ատոմը մեկ էլեկտրոն է նվիրում խոնարհմանը, նույնը, ինչ ածխածնի յուրաքանչյուր ատոմը, բայց թթվածնի էլեկտրաբացասականությունն ավելի բարձր է, քան ածխածինը, ուստի թթվածինը փոխում է խոնարհված համակարգի էլեկտրոնային խտությունը դեպի իրեն, իսկ ալդեհիդային խումբը, որպես ամբողջություն, ցուցադրում է բացասական: մեզոմերային ազդեցություն.
Այսպիսով, փոխարինողները, որոնք երկու էլեկտրոններ են նվիրաբերում խոնարհմանը, ունեն դրական մեզոմերային ազդեցություն: Դրանք ներառում են.
ա) ընդհանուր բացասական լիցքով փոխարինողներ, օրինակ՝ –O -;
բ) փոխարինողներ, որոնց կառուցվածքում p z օրբիտալներում կան չբաշխված էլեկտրոնային զույգերով ատոմներ, օրինակ՝ -NH 2, -OH,
-F, -Cl, -Br-, -I, -OR (-OCH 3, -OC 2 H 5):
Փոխարինիչները, որոնք փոխակերպում են էլեկտրոնի խտությունը խոնարհված համակարգում իրենց վրա, ցուցադրում են բացասական մեզոմերային ազդեցություն: Դրանք ներառում են փոխարինիչներ, որոնց կառուցվածքում կան կրկնակի կապեր, օրինակ.
 |
Փոխարինիչը կարող է միաժամանակ դրսևորել ինչպես ինդուկտիվ, այնպես էլ մեզոմերային ազդեցություն: Որոշ դեպքերում այդ էֆեկտների ուղղությունը նույնն է (օրինակ՝ -I և -M), որոշ դեպքերում դրանք գործում են հակառակ ուղղություններով (օրինակ՝ -I և +M)։ Ինչպե՞ս որոշել այս դեպքերում փոխարինողի ընդհանուր ազդեցությունը մոլեկուլի մնացած մասի վրա (այլ կերպ ասած՝ ինչպե՞ս որոշել՝ տվյալ փոխարինողը էլեկտրոն դոնոր է, թե էլեկտրոն ընդունող): Փոխարինիչները, որոնք մեծացնում են էլեկտրոնի խտությունը մնացած մոլեկուլում, կոչվում են էլեկտրոն դոնոր փոխարինողներ, իսկ այն փոխարինողները, որոնք նվազեցնում են էլեկտրոնի խտությունը մնացած մոլեկուլում, կոչվում են էլեկտրոններ քաշող փոխարինիչներ։
Փոխարինողի ընդհանուր ազդեցությունը որոշելու համար անհրաժեշտ է համեմատել դրա էլեկտրոնային ազդեցությունը մեծությամբ: Եթե դրական նշանի էֆեկտը գերակշռում է, ապա փոխարինողը էլեկտրոն դոնոր է: Եթե բացասական ազդեցությունը գերակշռում է, ապա փոխարինողը էլեկտրոն քաշող փոխարինող է: Հարկ է նշել, որ, որպես կանոն, մեզոմերային էֆեկտն ավելի ուժեղ է, քան ինդուկտիվը (պ կապերի բևեռացման ավելի մեծ ունակության շնորհիվ)։ Սակայն այս կանոնից կան բացառություններ՝ հալոգենների ինդուկտիվ ազդեցությունն ավելի ուժեղ է, քան մեզոմերականը։
Դիտարկենք կոնկրետ օրինակներ.
Այս միացության մեջ ամինո խումբը էլեկտրոն նվիրաբերող փոխարինող է, քանի որ դրա դրական մեզոմերիկ ազդեցությունն ավելի ցայտուն է, քան բացասական ինդուկտիվը:
 Այս միացության մեջ ամինո խումբը էլեկտրոն քաշող փոխարինող է, քանի որ ցուցադրում է միայն բացասական ինդուկտիվ ազդեցություն:
Այս միացության մեջ ամինո խումբը էլեկտրոն քաշող փոխարինող է, քանի որ ցուցադրում է միայն բացասական ինդուկտիվ ազդեցություն:
Ֆենոլի մոլեկուլում հիդրօքսիլ խումբը էլեկտրոն նվիրաբերող փոխարինող է՝ դրական մեզոմերային ազդեցության գերակշռության պատճառով բացասական ինդուկտիվին։
 Բենզիլ սպիրտի մոլեկուլում հիդրօքսիլ խումբը չի մասնակցում կոնյուգացմանը և ցուցադրում է միայն բացասական ինդուկտիվ ազդեցություն։ Հետևաբար, այն էլեկտրոն քաշող փոխարինող է։
Բենզիլ սպիրտի մոլեկուլում հիդրօքսիլ խումբը չի մասնակցում կոնյուգացմանը և ցուցադրում է միայն բացասական ինդուկտիվ ազդեցություն։ Հետևաբար, այն էլեկտրոն քաշող փոխարինող է։
Այս օրինակները ցույց են տալիս, որ ընդհանրապես չի կարելի դիտարկել որևէ փոխարինողի ազդեցությունը, բայց պետք է հաշվի առնել դրա ազդեցությունը որոշակի մոլեկուլում:
 Միայն հալոգեններն են միշտ էլեկտրոն քաշող փոխարինիչներ, քանի որ դրանց բացասական ինդուկտիվ ազդեցությունն ավելի ուժեղ է, քան դրական մեզոմերականը: Օրինակ:
Միայն հալոգեններն են միշտ էլեկտրոն քաշող փոխարինիչներ, քանի որ դրանց բացասական ինդուկտիվ ազդեցությունն ավելի ուժեղ է, քան դրական մեզոմերականը: Օրինակ:

Այժմ վերադառնանք բենզոլի ածանցյալների էլեկտրոֆիլ փոխարինման ռեակցիաներին: Այսպիսով, մենք պարզեցինք, որ ռինգում արդեն առկա փոխարինողն ազդում է էլեկտրոֆիլ փոխարինման ռեակցիաների ընթացքի վրա: Ո՞րն է այս ազդեցությունը:
Փոխարինիչը ազդում է S E ռեակցիաների արագության և օղակի մեջ մտցված երկրորդ փոխարինողի դիրքի վրա. Դիտարկենք ազդեցության այս երկու ասպեկտները:
Ազդեցություն ռեակցիայի արագության վրա. Որքան բարձր է էլեկտրոնի խտությունը օղակում, այնքան ավելի հեշտ է ընթանում էլեկտրոֆիլ փոխարինման ռեակցիաները: Հասկանալի է, որ էլեկտրոն նվիրաբերող փոխարինիչները հեշտացնում են S E ռեակցիաները (դրանք ցիկլը ակտիվացնողներ են), իսկ էլեկտրոններ հանող փոխարինողները խանգարում են նրանց (նրանք ապաակտիվացնում են ցիկլը)։ Ուստի էլեկտրոֆիլ փոխարինող ռեակցիաները բենզոլի ածանցյալներում, որոնք պարունակում են էլեկտրոններ քաշող փոխարինիչներ, իրականացվում են ավելի ծանր պայմաններում։
 Համեմատենք ֆենոլի, տոլուոլի, բենզոլի, քլորբենզոլի և նիտրոբենզոլի ակտիվությունը նիտրացման ռեակցիայում։
Համեմատենք ֆենոլի, տոլուոլի, բենզոլի, քլորբենզոլի և նիտրոբենզոլի ակտիվությունը նիտրացման ռեակցիայում։
Քանի որ ֆենոլը և տոլուոլը պարունակում են էլեկտրոն նվիրաբերող փոխարինիչներ, նրանք ավելի ակտիվ են S E ռեակցիաներում, քան բենզոլը: Ընդհակառակը, քլորոբենզոլը և նիտրոբենզոլը ավելի քիչ ակտիվ են այդ ռեակցիաներում, քան բենզոլը, քանի որ. պարունակում են էլեկտրոններ հանող փոխարինիչներ։ Ֆենոլն ավելի ակտիվ է, քան տոլուոլը՝ շնորհիվ OH խմբի դրական մեզոմերային ազդեցության։ Քլորն այնքան ուժեղ չէ, որ էլեկտրոններ քաշող փոխարինիչ է, որքան նիտրո խումբը, քանի որ Նիտրո խումբը ցուցադրում է ինչպես բացասական ինդուկտիվ, այնպես էլ բացասական մեզոմերային ազդեցություն: Այսպիսով, այս շարքում էլեկտրոֆիլային փոխարինման ռեակցիաներում ակտիվությունը նվազում է ֆենոլից մինչև նիտրոբենզոլ: Փորձնականորեն հաստատվել է, որ եթե բենզոլի նիտրացման ռեակցիայի արագությունը վերցվի 1, ապա այս շարքը կունենա հետևյալ տեսքը.
Էլեկտրաֆիլ փոխարինող ռեակցիաների ընթացքի վրա անուշաբույր օղակում փոխարինողի ազդեցության երկրորդ ասպեկտը այսպես կոչված. փոխարինիչների կողմնորոշիչ գործողություն. Բոլոր փոխարինողները կարելի է բաժանել երկու խմբի՝ օրթո-, պարա-օրիենտանտներ (1-ին տեսակի փոխարինիչներ) և մետա-օրիենտանտներ (2-րդ տեսակի փոխարինիչներ):
Դեպի 1-ին տեսակի փոխարինողներներառում են՝ -OH, -O -, -NH 2, ալկիլ խմբեր (-CH 3, -C 2 H 5 և այլն) և հալոգեններ: Դուք կարող եք տեսնել, որ այս բոլոր փոխարինիչները դրսևորում են դրական ինդուկտիվ ազդեցություն և/կամ դրական մեզոմերային ազդեցություն: Նրանք բոլորը, բացառությամբ հալոգենների, մեծացնում են էլեկտրոնի խտությունը օղակում, հատկապես օրթո և պարա դիրքերում։ Հետեւաբար, էլեկտրոֆիլն ուղղված է այս դիրքերին: Որպես օրինակ վերցնենք ֆենոլը.
Հիդրօքսիլ խմբի դրական մեզոմերային ազդեցության շնորհիվ էլեկտրոնային խտությունը վերաբաշխվում է խոնարհված համակարգի երկայնքով, իսկ օրթո և պարա դիրքերում այն հատկապես մեծանում է։
 Երբ ֆենոլը բրոմացվում է, ձևավորվում է օրթո- և պարա-բրոմֆենոլի խառնուրդ.
Երբ ֆենոլը բրոմացվում է, ձևավորվում է օրթո- և պարա-բրոմֆենոլի խառնուրդ.
Եթե բրոմացումը կատարվում է բևեռային լուծիչում (բրոմաջուր) և օգտագործվում է բրոմի ավելցուկ, ռեակցիան անմիջապես ընթանում է երեք դիրքով.
 |
2-րդ տեսակի փոխարինողներեն՝ -NH 3 +, -COOH, -CHO (ալդեհիդային խումբ), -NO 2, -SO 3 H: Այս բոլոր փոխարինիչները նվազեցնում են էլեկտրոնի խտությունը արոմատիկ օղակում, սակայն մետա դիրքերում դրա վերաբաշխման պատճառով դա այդպես չէ. իջեցվել է այնքան ուժեղ, որքան օրթո- և պարա-: Դիտարկենք սա՝ օգտագործելով բենզոաթթվի օրինակը.
Կարբոքսիլ խումբը ցուցադրում է բացասական ինդուկտիվ և բացասական մեզոմերային ազդեցություն: Համակցված համակարգի երկայնքով մետա դիրքերում վերաբաշխման պատճառով էլեկտրոնի խտությունը մնում է ավելի բարձր, քան օրթո և պարա դիրքերում, ուստի էլեկտրոֆիլը հարձակվելու է մետա դիրքերի վրա.
 |
Ռեակցիաների առաջին խումբը փոխարինման ռեակցիաներն են։ Մենք ասացինք, որ արենները մոլեկուլային կառուցվածքում չունեն բազմաթիվ կապեր, այլ պարունակում են վեց էլեկտրոններից կազմված խոնարհված համակարգ, որը շատ կայուն է և լրացուցիչ ամրություն է հաղորդում բենզոլային օղակին։ Ուստի քիմիական ռեակցիաներում առաջին հերթին տեղի է ունենում ջրածնի ատոմների փոխարինում, այլ ոչ թե բենզոլային օղակի քայքայում։
Ալկանների մասին խոսելիս արդեն հանդիպել ենք փոխարինման ռեակցիաների, սակայն նրանց համար այդ ռեակցիաներն ընթացել են արմատական մեխանիզմով, իսկ արենների համար բնորոշ է փոխարինման ռեակցիաների իոնային մեխանիզմը։
Առաջինքիմիական հատկությունների հալոգենացում. Ջրածնի ատոմի փոխարինում հալոգենի ատոմով քլորով կամ բրոմով:
Ռեակցիան ընթանում է տաքացման ժամանակ և միշտ կատալիզատորի մասնակցությամբ։ Քլորի դեպքում դա կարող է լինել ալյումինի քլորիդ կամ երկաթի քլորիդ երեք: Կատալիզատորը բևեռացնում է հալոգենի մոլեկուլը, որի արդյունքում հետերոլիտիկ կապը կոտրվում է և ստացվում են իոններ։
Դրական լիցքավորված քլորիդ իոնը փոխազդում է բենզոլի հետ։
Եթե ռեակցիան տեղի է ունենում բրոմի հետ, ապա երկաթի տրիբրոմիդը կամ ալյումինի բրոմիդը գործում են որպես կատալիզատոր։

Կարևոր է նշել, որ ռեակցիան տեղի է ունենում մոլեկուլային բրոմի և ոչ թե բրոմ ջրի հետ: Բենզոլը չի արձագանքում բրոմ ջրի հետ:
Բենզոլի հոմոլոգների հալոգենացումը ունի իր առանձնահատկությունները: Տոլուոլի մոլեկուլում մեթիլ խումբը հեշտացնում է փոխարինումը օղակում, ռեակտիվությունը մեծանում է, և ռեակցիան ընթանում է ավելի մեղմ պայմաններում, այսինքն՝ արդեն սենյակային ջերմաստիճանում։
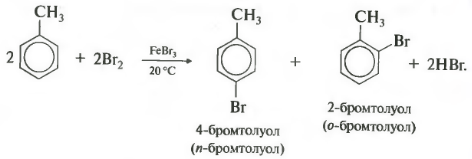
Կարևոր է նշել, որ փոխարինումը միշտ տեղի է ունենում օրթո և պարա դիրքերում, ուստի ստացվում է իզոմերների խառնուրդ։
Երկրորդբենզոլի սեփականության նիտրացում, նիտրո խմբի ներմուծում բենզոլային օղակ:

Ձևավորվում է դառը նուշի նիտրոբենզոլի հոտով թանձր դեղնավուն հեղուկ, ուստի ռեակցիան կարող է որակական լինել բենզոլի համար։ Նիտրացիայի համար օգտագործվում է խտացված ազոտական և ծծմբական թթուների նիտրացնող խառնուրդ։ Ռեակցիան իրականացվում է տաքացման միջոցով։
Հիշեցնեմ, որ Կոնովալովի ռեակցիայում ալկանների նիտրացման համար օգտագործվել է նոսր ազոտական թթու՝ առանց ծծմբաթթվի ավելացման։
Տոլուոլի նիտրացման, ինչպես նաև հալոգենացման ժամանակ առաջանում է օրթո– և պարաիզոմերների խառնուրդ։
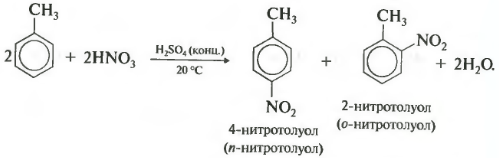
Երրորդբենզոլի հատկության ալկիլացում հալոալկաններով.

Այս ռեակցիան թույլ է տալիս ածխաջրածնային ռադիկալ ներմուծել բենզոլային օղակ և կարելի է համարել բենզոլի հոմոլոգներ ստանալու մեթոդ։ Որպես կատալիզատոր օգտագործվում է ալյումինի քլորիդը, որը նպաստում է հալոալկանի մոլեկուլի իոնների քայքայմանը։ Ունի նաև ջեռուցման կարիք։
Չորրորդբենզոլի հատկության ալկիլացում ալկեններով.
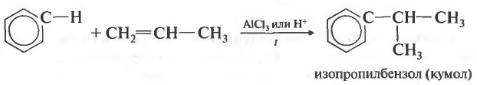
Այս կերպ, օրինակ, կարելի է ստանալ կումեն կամ էթիլբենզոլ։ Կատալիզատոր ալյումինի քլորիդ:
2. Բենզոլին ավելացման ռեակցիաներ
Ռեակցիաների երկրորդ խումբը հավելման ռեակցիաներն են։ Մենք ասացինք, որ այդ ռեակցիաները բնորոշ չեն, բայց դրանք հնարավոր են բավականին կոշտ պայմաններում պի-էլեկտրոնային ամպի ոչնչացման և վեց սիգմա կապերի ձևավորման դեպքում։
Հինգերորդհատկություն ընդհանուր ցանկում ջրածինացում, ջրածնի ավելացում։
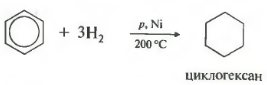
Ջերմաստիճան, ճնշում, կատալիզատոր նիկել կամ պլատին: Տոլուենը կարողանում է նույն կերպ արձագանքել։
վեցերորդգույքի քլորացում. Խնդրում ենք նկատի ունենալ, որ մենք կոնկրետ խոսում ենք քլորի հետ փոխազդեցության մասին, քանի որ բրոմը չի մտնում այս ռեակցիայի մեջ:
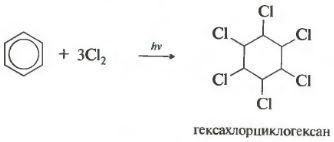
Ռեակցիան ընթանում է կոշտ ուլտրամանուշակագույն ճառագայթման տակ։ Առաջանում է հեքսաքլորցիկլոհեքսան՝ հեքսաքլորանի մեկ այլ անվանում՝ պինդ։
Կարևոր է հիշել, որ բենզոլի համար անհնարջրածնի հալոգենիդների ավելացման ռեակցիաներ (հիդրոհալոգենացում) և ջրի ավելացում (հիդրացիա):
3. Բենզոլի հոմոլոգների կողային շղթայում փոխարինում
Ռեակցիաների երրորդ խումբը վերաբերում է միայն բենզոլային հոմոլոգներին. սա փոխարինում է կողային շղթայում:
յոթերորդհատկություն ընդհանուր ցանկում հալոգենացում ածխածնի ալֆա ատոմում կողային շղթայում:

Ռեակցիան տեղի է ունենում տաքացման կամ ճառագայթման ժամանակ և միշտ միայն ալֆա ածխածնի վրա: Քանի որ հալոգենացումը շարունակվում է, երկրորդ հալոգենի ատոմը կվերադառնա ալֆա դիրքի:
4. Բենզոլի հոմոլոգների օքսիդացում
Ռեակցիաների չորրորդ խումբը օքսիդացումն է։
Բենզոլի օղակը չափազանց ամուր է, ուստի բենզոլ չի օքսիդանումկալիումի պերմանգանատը չի գունաթափում իր լուծույթը: Սա շատ կարևոր է հիշել:
Մյուս կողմից, բենզոլի հոմոլոգները տաքացնելիս օքսիդացվում են կալիումի պերմանգանատի թթվացված լուծույթով։ Եվ սա ութերորդ քիմիական հատկությունն է։

Ստացվում է բենզոաթթու։ Նկատվում է լուծույթի գունաթափում։ Այս դեպքում, անկախ նրանից, թե որքան երկար է փոխարինողի ածխածնային շղթան, այն միշտ կոտրվում է առաջին ածխածնի ատոմից հետո և ալֆա ատոմը օքսիդացվում է կարբոքսիլային խմբի՝ բենզոաթթվի ձևավորմամբ։ Մոլեկուլի մնացած մասը օքսիդացվում է համապատասխան թթուով կամ, եթե դա ընդամենը մեկ ածխածնի ատոմ է, ածխաթթու:
Եթե բենզոլի հոմոլոգն ունի մեկից ավելի ածխաջրածնային փոխարինիչներ արոմատիկ օղակի վրա, ապա օքսիդացումը տեղի է ունենում նույն կանոններով՝ ալֆա դիրքում գտնվող ածխածինը օքսիդացված է։
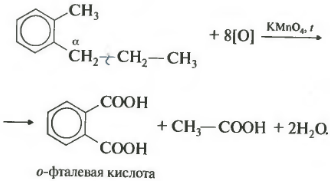
Այս օրինակում ստացվում է երկհիմնական անուշաբույր թթու, որը կոչվում է ֆտալաթթու։
Հատուկ կերպով նշում եմ կումենի՝ իզոպրոպիլբենզոլի օքսիդացումը մթնոլորտի թթվածնով ծծմբաթթվի առկայության դեպքում։

Սա ֆենոլի արտադրության այսպես կոչված կումենի մեթոդն է։ Որպես կանոն, այս ռեակցիայի հետ պետք է զբաղվել ֆենոլի արտադրության հետ կապված հարցերում։ Սա արդյունաբերական ճանապարհն է։
իններորդգույքի այրում, ամբողջական օքսիդացում թթվածնով։ Բենզոլը և նրա հոմոլոգները այրվում են մինչև ածխաթթու գազ և ջուր:
Եկեք գրենք բենզոլի այրման հավասարումը ընդհանուր ձևով:
Ըստ զանգվածի պահպանման օրենքի՝ ձախ կողմում պետք է լինի այնքան ատոմ, որքան աջ կողմում։ Որովհետև, ի վերջո, քիմիական ռեակցիաներում ատոմները ոչ մի տեղ չեն գնում, այլ ուղղակի փոխվում է նրանց միջև կապերի կարգը։ Այսպիսով, կլինեն այնքան ածխածնի երկօքսիդի մոլեկուլներ, որքան ածխածնի ատոմներ կան արենի մոլեկուլում, քանի որ մոլեկուլը պարունակում է մեկ ածխածնի ատոմ: Դա n CO 2 մոլեկուլ է: Կլինեն ջրի մոլեկուլների կեսը, որքան ջրածնի ատոմները, այսինքն՝ (2n-6) / 2, ինչը նշանակում է n-3:
Ձախ և աջ կողմում կան նույն թվով թթվածնի ատոմներ: Աջ կողմում կա 2n ածխաթթու գազից, քանի որ յուրաքանչյուր մոլեկուլում կա երկու թթվածնի ատոմ, գումարած n-3 ջրից, ընդհանուր առմամբ 3n-3: Ձախ կողմում կան նույն թվով թթվածնի ատոմներ 3n-3, ինչը նշանակում է, որ մոլեկուլները երկու անգամ ավելի քիչ են, քանի որ մոլեկուլը պարունակում է երկու ատոմ։ Այսինքն (3n-3)/2 թթվածնի մոլեկուլ։
Այսպիսով, մենք կազմել ենք բենզոլի հոմոլոգների այրման հավասարումը ընդհանուր ձևով:
Բենզոլի ցիկլային կառուցվածքն առաջին անգամ առաջարկվել է Ֆ.Ա. Կեկուլեն 1865 թ

Ֆրիդրիխ Ավգուստ Կեկուլե ֆոն Ստրադոնիցը 19-րդ դարի նշանավոր գերմանացի քիմիկոս էր։ 1854 թվականին նա հայտնաբերեց ծծումբ պարունակող առաջին օրգանական միացությունը՝ թիոքացախաթթուն (թիոէթանաթթու)։ Բացի այդ, նա հաստատել է դիազո միացությունների կառուցվածքը։ Այնուամենայնիվ, քիմիայի զարգացման մեջ նրա ամենահայտնի ներդրումը բենզոլի կառուցվածքի հաստատումն է (1866 թ.)։ Կեկուլեն ցույց տվեց, որ բենզոլի կրկնակի կապերը հերթափոխվում են օղակի շուրջ (այս միտքը առաջին անգամ նրա մոտ առաջացել է երազում): Հետագայում նա ցույց տվեց, որ երկու հնարավոր կրկնակի կապի դասավորությունները նույնական են, և որ բենզոլային օղակը հիբրիդ է երկու կառույցների միջև: Այսպիսով, նա ակնկալում էր ռեզոնանսի (մեզոմերիզմ) հայեցակարգը, որը հայտնվեց քիմիական կապի տեսության մեջ 1930-ականների սկզբին։
Եթե բենզոլն իրոք ուներ նման կառուցվածք, ապա նրա 1,2-դիփոխարինված ածանցյալները պետք է ունենան երկուական իզոմեր։ Օրինակ,

Այնուամենայնիվ, 1,2-դիփոխարինված բենզոլներից և ոչ մեկը չի կարող մեկուսացնել երկու իզոմեր:
Հետևաբար, Կեկուլեն առաջարկեց, որ բենզոլի մոլեկուլը գոյություն ունի որպես երկու կառուցվածք, որոնք արագորեն անցնում են միմյանց մեջ.

Նշենք, որ բենզոլի մոլեկուլների և դրանց ածանցյալների նման սխեմատիկ պատկերները սովորաբար չեն նշում բենզոլի օղակի ածխածնի ատոմներին կցված ջրածնի ատոմները:
Ժամանակակից քիմիայում բենզոլի մոլեկուլը համարվում է որպես այս երկու սահմանափակող ռեզոնանսային ձևերի ռեզոնանսային հիբրիդ (տես բաժին 2.1): Բենզոլի մոլեկուլի մեկ այլ նկարագրությունը հիմնված է նրա մոլեկուլային ուղեծրերի հաշվի վրա: Վրկ. 3.1, նշվեց, որ կապող ուղեծրերում տեղակայված -էլեկտրոնները տեղաբաշխված են բենզոլի օղակի բոլոր ածխածնի ատոմների միջև և ձևավորում են -էլեկտրոնային ամպ: Այս ներկայացման համաձայն՝ բենզոլի մոլեկուլը պայմանականորեն կարելի է պատկերել հետևյալ կերպ.
Փորձարարական տվյալները հաստատում են բենզոլում հենց այդպիսի կառուցվածքի առկայությունը։ Եթե բենզոլը ունենար այն կառուցվածքը, որն ի սկզբանե առաջարկել էր Կեկուլեն, երեք խոնարհված կրկնակի կապերով, ապա բենզոլը պետք է մտներ հավելման ռեակցիաների մեջ, ինչպես ալկենները: Այնուամենայնիվ, ինչպես նշվեց վերևում, բենզոլը չի մտնում հավելման ռեակցիաների մեջ: Բացի այդ, բենզոլն ավելի կայուն է, քան եթե այն ունենար երեք մեկուսացված կրկնակի կապեր: Վրկ. 5.3 Նշվեց, որ բենզոլի հիդրոգենացման էթալպիան ցիկլոհեքսանի առաջացմամբ ունի ավելի մեծ բացասական
Աղյուսակ 18.3. Տարբեր ածխածին-ածխածին կապերի երկարություն


Բրինձ. 18.6. Բենզոլի մոլեկուլի երկրաչափական կառուցվածքը.
արժեքը, քան ցիկլոհեքսենի հիդրոգենացման էթալպիան երեք անգամ: Այս արժեքների միջև տարբերությունը սովորաբար կոչվում է տեղաբաշխման էնթալպիա, ռեզոնանսային էներգիա կամ բենզոլի կայունացման էներգիա:
Բենզոլային օղակի բոլոր ածխածին-ածխածին կապերն ունեն նույն երկարությունը, որը փոքր է ալկաններում C-C կապերի երկարությունից, բայց ավելի երկար, քան ալկեններում C=C կապերի երկարությունը (Աղյուսակ 18.3): Սա հաստատում է, որ բենզոլում ածխածին-ածխածին կապերը հիբրիդ են միայնակ և կրկնակի կապերի միջև:
Բենզոլի մոլեկուլն ունի հարթ կառուցվածք, որը ցույց է տրված Նկ. 18.6.
Ֆիզիկական հատկություններ
Նորմալ պայմաններում բենզոլը անգույն հեղուկ է, որը սառչում է 5,5°C-ում և եռում 80°C-ում։ Այն ունի բնորոշ հաճելի հոտ, բայց, ինչպես նշվեց վերևում, շատ թունավոր է։ Բենզոլը ջրի հետ չի խառնվում, իսկ բենզոլային համակարգում ջուրը կազմում է երկու շերտերի վերին մասը։ Այնուամենայնիվ, այն լուծելի է ոչ բևեռ օրգանական լուծիչներում և ինքնին լավ լուծիչ է այլ օրգանական միացությունների համար:
Քիմիական հատկություններ
Թեև բենզոլը մտնում է որոշակի հավելման ռեակցիաների մեջ (տես ստորև), այն չի ցուցաբերում դրանցում առկա ալկեններին բնորոշ ռեակտիվություն։ Օրինակ, այն չի գունազրկում բրոմային ջուրը կամ α-իոնային լուծույթը: Բացի այդ, բենզոլ
մտնում է ավելացման ռեակցիաների մեջ ուժեղ թթուների հետ, ինչպիսիք են հիդրոքլորային կամ ծծմբաթթուները:
Միաժամանակ բենզոլը մասնակցում է մի շարք էլեկտրոֆիլ փոխարինման ռեակցիաների։ Անուշաբույր միացություններն այս տեսակի ռեակցիաների արդյունք են, քանի որ այդ ռեակցիաներում պահպանվում է բենզոլի ապատեղայնացված էլեկտրոնային համակարգը: Ջրածնի ատոմի փոխարինման ընդհանուր մեխանիզմը բենզոլի օղակի վրա որոշ էլեկտրոֆիլներով նկարագրված է Բ. 17.3. Բենզոլի էլեկտրոֆիլ փոխարինման օրինակներ են նրա նիտրացումը, հալոգենացումը, սուլֆոնացումը և Ֆրիդել-Կրաֆթսի ռեակցիաները։
Նիտրացիա. Բենզոլը կարելի է նիտրացնել (խումբ ներմուծելով դրա մեջ)՝ այն մշակելով խտացված ազոտական և ծծմբական թթուների խառնուրդով.

Նիտրոբենզոլ
Այս ռեակցիայի պայմանները և դրա մեխանիզմը նկարագրված են բաժնում: 17.3.
Նիտրոբենզոլը գունատ դեղին հեղուկ է՝ բնորոշ նուշի հոտով։ Բենզոլի նիտրացման ժամանակ, բացի նիտրոբենզոլից, առաջանում են նաև 1,3-դինիտրոբենզոլի բյուրեղներ, որոնք հետևյալ ռեակցիայի արդյունքն են.

Հալոգենացում. Եթե մթության մեջ բենզոլը խառնեք քլորի կամ բրոմի հետ, քաղցկեղ չի առաջանա: Սակայն Լյուիս թթուների հատկություններով կատալիզատորների առկայության դեպքում նման խառնուրդներում տեղի են ունենում էլեկտրոֆիլ փոխարինման ռեակցիաներ։ Այս ռեակցիաների բնորոշ կատալիզատորներն են երկաթի (III) բրոմիդը և ալյումինի քլորիդը: Այս կատալիզատորների գործողությունը կայանում է նրանում, որ նրանք ստեղծում են բևեռացում հալոգենի մոլեկուլներում, որոնք այնուհետև կատալիզատորի հետ բարդություն են կազմում.
չնայած չկա ուղղակի ապացույց, որ այս դեպքում ազատ իոններ են գոյանում։ Բենզոլի բրոմացման մեխանիզմը՝ օգտագործելով երկաթի (III) բրոմը որպես իոնային կրիչ, կարող է ներկայացվել հետևյալ կերպ.

Սուլֆոնացիա. Բենզոլը կարող է սուլֆոնացվել (դրանում ջրածնի ատոմը փոխարինելով սուլֆո խմբով)՝ մի քանի ժամով իր խառնուրդը խտացված ծծմբաթթվի հետ վերադարձնելով։ Փոխարենը, բենզոլը կարող է նրբորեն տաքացնել՝ խառնելով ծխած ծծմբաթթվի հետ: Ծծմբաթթուն պարունակում է ծծմբի եռօքսիդ: Այս ռեակցիայի մեխանիզմը կարելի է ներկայացնել սխեմայով

Friedel-Crafts-ի ռեակցիաները. Friedel-Crafts ռեակցիաները սկզբնապես կոչվում էին խտացման ռեակցիաներ արոմատիկ միացությունների և ալկիլ հալոգենիդների միջև՝ անջուր ալյումինի քլորիդ կատալիզատորի առկայության դեպքում։
Կոնդենսացիայի ռեակցիաներում ռեակտիվների երկու մոլեկուլ (կամ մեկ ռեակտիվ) միանում են միմյանց՝ ձևավորելով նոր միացության մոլեկուլ, մինչդեռ որոշ պարզ միացությունների մոլեկուլը, օրինակ՝ ջուրը կամ քլորաջրածինը, բաժանվում է (վերացնում) դրանցից։
Ներկայումս Friedel-Crafts-ի ռեակցիան անուշաբույր միացության ցանկացած էլեկտրոֆիլ փոխարինում է, որում էլեկտրոֆիլի դեր է խաղում կարբոկատիոնը կամ բարձր բևեռացված համալիրը՝ դրական լիցքավորված ածխածնի ատոմով: Էլեկտրաֆիլ նյութը սովորաբար ալկիլ հալոգեն կամ կարբոքսիլաթթվի քլորիդ է, թեև դա կարող է լինել նաև, օրինակ, ալկեն կամ սպիրտ։ Անջուր ալյումինի քլորիդը սովորաբար օգտագործվում է որպես այս ռեակցիաների կատալիզատոր: Friedel-Crafts ռեակցիաները սովորաբար բաժանվում են երկու տեսակի՝ ալկիլացում և ացիլացում։
Ալկիլացում. Friedel-Crafts-ի այս տեսակի ռեակցիաներում բենզոլի օղակում ջրածնի մեկ կամ մի քանի ատոմ փոխարինվում են ալկիլային խմբերով։ Օրինակ, երբ բենզոլի և քլորմեթանի խառնուրդը զգուշորեն տաքացվում է անջուր ալյումինի քլորիդի առկայության դեպքում, առաջանում է մեթիլբենզոլ։ Այս ռեակցիայում քլորոմեթանը կատարում է էլեկտրոֆիլ նյութի դեր։ Այն բևեռացված է ալյումինի քլորիդով այնպես, ինչպես դա տեղի է ունենում հալոգենի մոլեկուլների դեպքում.
Դիտարկվող ռեակցիայի մեխանիզմը կարող է ներկայացվել հետևյալ կերպ.

Պետք է նշել, որ բենզոլի և քլորմեթանի միջև խտացման այս ռեակցիայի ժամանակ քլորաջրածնի մոլեկուլը բաժանվում է: Նաև նշում ենք, որ ազատ իոնի տեսքով մետաղական կարբոկացիայի իրական գոյությունը կասկածելի է։
Բենզոլի ալկիլացումը քլորմեթանով կատալիզատորի առկայության դեպքում՝ անջուր ալյումինի քլորիդը չի ավարտվում մեթիլբենզոլի առաջացմամբ։ Այս ռեակցիայում տեղի է ունենում բենզոլային օղակի հետագա ալկիլացում, ինչը հանգեցնում է 1,2-դիմեթիլբենզոլի ձևավորմանը.

Ացիլացում. Friedel-Crafts-ի այս տեսակի ռեակցիաներում բենզոլի օղակում ջրածնի ատոմը փոխարինվում է ացիլային խմբով, ինչի արդյունքում առաջանում է արոմատիկ կետոն։
Ակիլային խումբն ունի ընդհանուր բանաձև
Ակիլային միացության սիստեմատիկ անվանումը ձևավորվում է համապատասխան կարբոքսիլաթթվի անվան մեջ, որի ածանցյալն է տվյալ ացիլային միացությունը, փոխարինելով -ով վերջածանցը՝ -(o)yl վերջածանցով։ Օրինակ

Բենզոլի ացիլացումն իրականացվում է կարբոքսիլաթթվի քլորիդ կամ անհիդրիդ օգտագործելով՝ ալյումինի քլորիդի անջուր կատալիզատորի առկայության դեպքում։ Օրինակ

Այս ռեակցիան խտացում է, որի ժամանակ տեղի է ունենում քլորաջրածնի մոլեկուլի վերացում։ Նկատի ունեցեք նաև, որ «ֆենիլ» անվանումը հաճախ օգտագործվում է բենզոլի օղակը նշելու համար այն միացություններում, որտեղ բենզոլը հիմնական խումբը չէ.

Ավելացման ռեակցիաներ. Թեև բենզոլը առավել բնորոշ է էլեկտրոֆիլ փոխարինման ռեակցիաներին, այն նաև մտնում է որոշ հավելումների ռեակցիաների մեջ: Նրանցից մեկին մենք արդեն հանդիպել ենք։ Խոսքը բենզոլի հիդրոգենացման մասին է (տես բաժին 5.3): Երբ բենզոլի և ջրածնի խառնուրդն անցնում է մանր աղացած նիկելի կատալիզատորի մակերեսով 150–160 °C ջերմաստիճանում, առաջանում է ռեակցիաների մի ամբողջ հաջորդականություն, որն ավարտվում է ցիկլոհեքսանի առաջացմամբ։ Այս ռեակցիայի ընդհանուր ստոյխիոմետրիկ հավասարումը կարող է ներկայացվել հետևյալ կերպ.

Ուլտրամանուշակագույն ճառագայթման կամ արևի ուղիղ ճառագայթների ազդեցության տակ բենզոլը նույնպես արձագանքում է քլորին։ Այս ռեակցիան իրականացվում է բարդ արմատական մեխանիզմով։ Նրա վերջնական արտադրանքը 1,2,3,4,5,6-հեքսաքլորցիկլոհեքսան է.

Նմանատիպ ռեակցիա տեղի է ունենում բենզոլի և բրոմի միջև ուլտրամանուշակագույն ճառագայթման կամ արևի լույսի ազդեցության տակ:
Օքսիդացում. Բենզոլը և բենզոլի օղակը այլ անուշաբույր միացություններում, ընդհանուր առմամբ, դիմացկուն են օքսիդացմանը նույնիսկ այնպիսի ուժեղ օքսիդացնող նյութերի կողմից, ինչպիսիք են կալիումի պերմանգանատի թթվային կամ ալկալային լուծույթը: Այնուամենայնիվ, բենզոլը և այլ արոմատիկ նյութերը այրվում են օդում կամ թթվածնում՝ ձևավորելով շատ ծխագույն բոց, որը բնորոշ է ածխածնի հարաբերական բարձր պարունակությամբ ածխաջրածիններին։
ՍԱՀՄԱՆՈՒՄ
Բենզոլ- անգույն հեղուկ է՝ բնորոշ հոտով; եռման ջերմաստիճանը 80,1 o C, հալման ջերմաստիճանը 5,5 o C. Ջրում չլուծվող, թունավոր:
Բենզոլի անուշաբույր հատկությունները, որոնք որոշվում են նրա կառուցվածքի առանձնահատկություններով, արտահայտվում են բենզոլի օղակի հարաբերական կայունությամբ՝ չնայած բաղադրության մեջ բենզոլի չհագեցվածությանը։ Այսպիսով, ի տարբերություն էթիլենի կրկնակի կապերով չհագեցած միացությունների, բենզոլը դիմացկուն է օքսիդացնող նյութերի նկատմամբ։
Բրինձ. 1. Բենզոլի մոլեկուլի կառուցվածքն ըստ Կեկուլեի.
Բենզոլի ստացում
Բենզոլ ստանալու հիմնական ուղիները ներառում են.
– հեքսանի ջրազերծում (կատալիզատորներ – Pt, Cr 3 O 2)
CH 3 - (CH 2) 4 -CH 3 → C 6 H 6 + 4H 2 (t o C, p, kat \u003d Cr 2 O 3);
- ցիկլոհեքսանի ջրազրկում
C 6 H 12 → C 6 H 6 + 3H 2 (t o C, kat = Pt, Ni);
- ացետիլենի տրիմերացում (ռեակցիան շարունակվում է, երբ տաքացվում է մինչև 600 o C, կատալիզատորը ակտիվացված ածխածին է)
3HC≡CH → C 6 H 6 (t = 600 o C, kat = C ակտիվ):
Բենզոլի քիմիական հատկությունները
Բենզոլը բնութագրվում է փոխարինման ռեակցիաներով, որոնք ընթանում են ըստ էլեկտրոֆիլ մեխանիզմի.
Հալոգենացում (բենզոլը փոխազդում է քլորի և բրոմի հետ կատալիզատորների առկայության դեպքում՝ անջուր AlCl 3 , FeCl 3 , AlBr 3 )
C 6 H 6 + Cl 2 \u003d C 6 H 5 -Cl + HCl;
- նիտրացիա (բենզոլը հեշտությամբ փոխազդում է նիտրացնող խառնուրդի հետ՝ խտացված ազոտական և ծծմբական թթուների խառնուրդ)

- ալկիլացում ալկեններով
C 6 H 6 + CH 2 \u003d CH-CH 3 → C 6 H 5 -CH (CH 3) 2
Բենզոլին ավելացման ռեակցիաները հանգեցնում են անուշաբույր համակարգի ոչնչացմանը և ընթանում են միայն ծանր պայմաններում.
- հիդրոգենացում (ռեակցիայի արտադրանք - ցիկլոհեքսան)
C 6 H 6 + 3H 2 → C 6 H 12 (t o C, kat = Pt);
- քլորի ավելացում (առաջանում է ուլտրամանուշակագույն ճառագայթման ազդեցության տակ պինդ արտադրանքի ձևավորմամբ՝ հեքսաքլորցիկլոհեքսան (հեքսաքլորան) - C 6 H 6 Cl 6)
C 6 H 6 + 6Cl 2 → C 6 H 6 Cl 6:
Բենզոլի կիրառում
Բենզոլը լայնորեն կիրառվում է արդյունաբերական օրգանական քիմիայում։ Գրեթե բոլոր միացությունները, որոնք իրենց բաղադրության մեջ ունեն բենզոլային օղակներ, ստացվում են բենզոլից, օրինակ՝ ստիրոլից, ֆենոլից, անիլինից, հալոգենով փոխարինված արեններից։ Բենզոլն օգտագործվում է ներկանյութերի, մակերեսային ակտիվ նյութերի և դեղագործական նյութերի սինթեզի համար։
Խնդիրների լուծման օրինակներ
ՕՐԻՆԱԿ 1
| Զորավարժություններ | Նյութի գոլորշիների խտությունը 3,482 գ/լ է։ Դրա պիրոլիզի արդյունքում ստացվել է 6 գ մուր և 5,6 լիտր ջրածին։ Որոշեք այս նյութի բանաձևը. |
| Լուծում | Մուրը ածխածին է։ Խնդրի պայմաններից ելնելով գտնենք մուր նյութի քանակը (ածխածնի մոլային զանգվածը 12 գ/մոլ է). n (C) = m (C) / M (C); n(C) \u003d 6 / 12 \u003d 0,5 մոլ: Հաշվել ջրածնի նյութի քանակը. n (H 2) \u003d V (H 2) / V մ; n (H 2) \u003d 5.6 / 22.4 \u003d 0.25 մոլ: Այսպիսով, մեկ ջրածնի ատոմի նյութի քանակը հավասար կլինի. n(H) = 2 × 0.25 = 0.5 մոլ: Ածխաջրածնի մոլեկուլում ածխածնի ատոմների թիվը նշանակենք «x», իսկ ջրածնի ատոմների թիվը՝ «y», ապա այս ատոմների հարաբերակցությունը մոլեկուլում. x: y \u003d 0.5: 0.5 \u003d 1: 1: Այնուհետև ածխաջրածինների ամենապարզ բանաձևը կարտահայտվի CH բաղադրությամբ։ CH բաղադրության մոլեկուլի մոլեկուլային քաշը հետևյալն է. M(CH) = 13 գ/մոլ Եկեք պարզենք ածխաջրածնի մոլեկուլային քաշը՝ հիմնվելով խնդրի պայմանների վրա. M (C x H y) = ρ × V m; M (C x H y) \u003d 3,482 × 22,4 \u003d 78 գ / մոլ: Եկեք սահմանենք ածխաջրածնի իրական բանաձևը. k \u003d M (C x H y) / M (CH) \u003d 78/13 \u003d 6, հետևաբար, «x» և «y» գործակիցները պետք է բազմապատկվեն 6-ով, ապա ածխաջրածինների բանաձևը կստանա C 6 H 6 ձևը: Դա բենզին է: |
| Պատասխանել | Ցանկալի ածխաջրածինը ունի C 6 H 6 բաղադրություն: Դա բենզին է: |
ՕՐԻՆԱԿ 2
| Զորավարժություններ | Հաշվե՛ք ացետիլենի քանակությունը, որն անհրաժեշտ է 400 մլ բենզոլ ստանալու համար (խտությունը 0,8 գ/մլ): |
| Լուծում | Մենք գրում ենք ացետիլենից բենզոլի արտադրության ռեակցիայի հավասարումը. |