បែងចែករវាងអេឡិចត្រូលីតខ្លាំង និងខ្សោយ។ អេឡិចត្រូលីតខ្លាំងនៅក្នុងដំណោះស្រាយត្រូវបានបំបែកស្ទើរតែទាំងស្រុង។ ក្រុមនៃអេឡិចត្រូលីតនេះរួមមានអំបិលភាគច្រើន អាល់កាឡាំង និង អាស៊ីតខ្លាំង. អេឡិចត្រូលីតខ្សោយរួមមានអាស៊ីតខ្សោយ និងមូលដ្ឋានខ្សោយ និងអំបិលមួយចំនួន៖ បារត (II) ក្លរួ, បារត (II) ស៊ីយ៉ានុត, ជាតិដែក (III) thiocyanate, និង cadmium iodide ។ ដំណោះស្រាយនៃអេឡិចត្រូលីតខ្លាំងនៅកំហាប់ខ្ពស់មានចរន្តអគ្គិសនីយ៉ាងសំខាន់ហើយវាកើនឡើងបន្តិចជាមួយនឹងការរំលាយដំណោះស្រាយ។
ដំណោះស្រាយ អេឡិចត្រូលីតខ្សោយនៅកំហាប់ខ្ពស់ ពួកវាមានភាពខុសប្លែកគ្នានៅក្នុងចរន្តអគ្គិសនីដែលមិនសំខាន់ ដែលកើនឡើងយ៉ាងខ្លាំងជាមួយនឹងការរំលាយដំណោះស្រាយ។
នៅពេលដែលសារធាតុត្រូវបានរំលាយនៅក្នុងសារធាតុរំលាយណាមួយ អ៊ីយ៉ុងសាមញ្ញ (មិនរលាយ) ត្រូវបានបង្កើតឡើង ម៉ូលេគុលអព្យាក្រឹតនៃសារធាតុរំលាយ អ៊ីយ៉ុងរលាយ (ជាតិទឹកក្នុងដំណោះស្រាយ aqueous) អ៊ីយ៉ុង (ឧទាហរណ៍។ល។) គូអ៊ីយ៉ុង (ឬអ៊ីយ៉ុងភ្លោះ) ដែល គឺជាក្រុមដែលទាក់ទងដោយអេឡិចត្រូស្តាតនៃអ៊ីយ៉ុងដែលមានបន្ទុកផ្ទុយគ្នា (ឧទាហរណ៍) ការបង្កើតដែលត្រូវបានសង្កេតឃើញនៅក្នុងភាគច្រើននៃដំណោះស្រាយអេឡិចត្រូលីតដែលមិនមានជាតិទឹក អ៊ីយ៉ុងស្មុគស្មាញ (ឧទាហរណ៍) ម៉ូលេគុលរលាយ។ល។
នៅក្នុងដំណោះស្រាយ aqueous នៃអេឡិចត្រូលីតខ្លាំង មានតែ cations និង anions សាមញ្ញ ឬ solvated ប៉ុណ្ណោះ។ មិនមានម៉ូលេគុលរលាយនៅក្នុងដំណោះស្រាយរបស់ពួកគេទេ។ ដូច្នេះ វាមិនត្រឹមត្រូវទេក្នុងការសន្មតថាវត្តមានរបស់ម៉ូលេគុល ឬអត្ថិភាពនៃចំណងរយៈពេលវែងរវាង ឬ និងនៅក្នុង ដំណោះស្រាយទឹក។សូដ្យូមក្លរួ។
នៅក្នុងដំណោះស្រាយ aqueous នៃអេឡិចត្រូលីតខ្សោយ សារធាតុរំលាយអាចមាននៅក្នុងទម្រង់នៃអ៊ីយ៉ុងសាមញ្ញ និងរលាយ (-hydrated) និងម៉ូលេគុលដែលមិនជាប់ពាក់ព័ន្ធ។
នៅក្នុងដំណោះស្រាយដែលមិនមានជាតិទឹក អេឡិចត្រូលីតខ្លាំងមួយចំនួន (ឧទាហរណ៍ ) មិនត្រូវបានបំបែកទាំងស្រុងទេ សូម្បីតែនៅកំហាប់ខ្ពស់ល្មម។ នៅក្នុងសារធាតុរំលាយសរីរាង្គភាគច្រើន ការបង្កើតគូអ៊ីយ៉ុងនៃអ៊ីយ៉ុងដែលមានបន្ទុកផ្ទុយគ្នាត្រូវបានគេសង្កេតឃើញ (សម្រាប់ព័ត៌មានលម្អិត សូមមើលសៀវភៅទី 2) ។
ក្នុងករណីខ្លះវាមិនអាចទៅរួចទេ ព្រំដែនមុតស្រួចរវាងអេឡិចត្រូលីតខ្លាំង និងខ្សោយ។
កម្លាំងអន្តរកម្ម។ នៅក្រោមសកម្មភាពនៃកម្លាំងអន្តរកម្មជុំវិញអ៊ីយ៉ុងនីមួយៗដែលផ្លាស់ទីដោយសេរី អ៊ីយ៉ុងផ្សេងទៀតត្រូវបានដាក់ជាក្រុមដោយស៊ីមេទ្រី ចោទប្រកាន់ដោយសញ្ញាផ្ទុយ បង្កើតបានជាបរិយាកាសអ៊ីយ៉ុង ឬពពកអ៊ីយ៉ុង ដែលបន្ថយចលនារបស់អ៊ីយ៉ុងនៅក្នុងដំណោះស្រាយ។
ឧទាហរណ៍ នៅក្នុងដំណោះស្រាយមួយ ក្លរួអ៊ីយ៉ុងក្លរួ នៅជុំវិញអ៊ីយ៉ុងប៉ូតាស្យូមផ្លាស់ទី ហើយបរិយាកាសនៃអ៊ីយ៉ុងប៉ូតាស្យូមត្រូវបានបង្កើតឡើងនៅជិតអ៊ីយ៉ុងក្លរួដែលផ្លាស់ទី។
អ៊ីយ៉ុង ភាពចល័តដែលត្រូវបានចុះខ្សោយដោយកម្លាំងនៃផ្នែកបន្ថែមអន្តរកម្ម បង្ហាញពីសកម្មភាពគីមីថយចុះនៅក្នុងដំណោះស្រាយ។ នេះបណ្តាលឱ្យមានគម្លាតនៅក្នុងឥរិយាបថនៃអេឡិចត្រូលីតខ្លាំងពីទម្រង់បុរាណនៃច្បាប់នៃសកម្មភាពម៉ាស។
អ៊ីយ៉ុងបរទេសដែលមាននៅក្នុងដំណោះស្រាយនៃអេឡិចត្រូលីតដែលបានផ្តល់ឱ្យក៏មានឥទ្ធិពលខ្លាំងលើការចល័តនៃអ៊ីយ៉ុងរបស់វា។ កំហាប់កាន់តែខ្ពស់ អន្តរកម្មអន្តរកម្មកាន់តែសំខាន់ ហើយអ៊ីយ៉ុងបរទេសកាន់តែមានឥទ្ធិពលលើការចល័តអ៊ីយ៉ុង។
អាស៊ីតខ្សោយ និងមូលដ្ឋានមានចំណងអ៊ីដ្រូសែន ឬអ៊ីដ្រូសែននៅក្នុងម៉ូលេគុលរបស់ពួកគេ ដែលភាគច្រើនជា covalent ជាជាងអ៊ីយ៉ុង។ ដូច្នេះនៅពេលដែលរំលាយអេឡិចត្រូលីតខ្សោយនៅក្នុងសារធាតុរំលាយដែលខុសគ្នានៅក្នុង daoyue ធំ ការអនុញ្ញាត, ភាគច្រើនម៉ូលេគុលរបស់ពួកគេមិនបំបែកទៅជាអ៊ីយ៉ុងទេ។
ដំណោះស្រាយនៃអេឡិចត្រូលីតខ្លាំង ខុសពីដំណោះស្រាយនៃអេឡិចត្រូលីតខ្សោយ ដែលពួកវាមិនមានម៉ូលេគុលដែលមិនជាប់ពាក់ព័ន្ធ។ នេះត្រូវបានបញ្ជាក់ដោយការសិក្សាផ្នែករូបវិទ្យា និងគីមីវិទ្យាទំនើប។ ឧទាហរណ៍ការសិក្សាអំពីគ្រីស្តាល់នៃអេឡិចត្រូលីតខ្លាំងនៃប្រភេទកាំរស្មីអ៊ិចបញ្ជាក់ពីការពិតដែលថា បន្ទះឈើគ្រីស្តាល់អំបិលត្រូវបានបង្កើតឡើងពីអ៊ីយ៉ុង។
នៅពេលដែលរំលាយនៅក្នុងសារធាតុរំលាយជាមួយនឹងថេរ dielectric ខ្ពស់ សែល solvate (hydrated ក្នុងទឹក) ត្រូវបានបង្កើតឡើងនៅជុំវិញអ៊ីយ៉ុង ការពារការបញ្ចូលគ្នារបស់ពួកគេទៅជាម៉ូលេគុល។ ដូច្នេះ ចាប់តាំងពីអេឡិចត្រូលីតខ្លាំង សូម្បីតែនៅក្នុងស្ថានភាពគ្រីស្តាល់ មិនមានម៉ូលេគុលក៏ដោយ ពួកវាមិនមានម៉ូលេគុលនៅក្នុងដំណោះស្រាយសូម្បីតែច្រើនទៀត។
ទោះបីជាយ៉ាងណាក៏ដោយ វាត្រូវបានគេរកឃើញដោយពិសោធន៍ថា ចរន្តអគ្គិសនីនៃដំណោះស្រាយ aqueous នៃអេឡិចត្រូលីតខ្លាំង គឺមិនស្មើនឹងចរន្តអគ្គិសនី ដែលអាចត្រូវបានគេរំពឹងទុកក្នុងអំឡុងពេលបំបែកម៉ូលេគុលនៃអេឡិចត្រូលីតរលាយទៅជាអ៊ីយ៉ុង។
ដោយប្រើទ្រឹស្ដីនៃការបំបែកចរន្តអគ្គិសនីដែលស្នើឡើងដោយ Arrhenius វាបានប្រែក្លាយទៅជាមិនអាចពន្យល់អំពីរឿងនេះ និងការពិតមួយចំនួនទៀត។ ដើម្បីពន្យល់ពួកគេ បទប្បញ្ញត្តិវិទ្យាសាស្ត្រថ្មីត្រូវបានដាក់ទៅមុខ។
នាពេលបច្ចុប្បន្ននេះភាពខុសគ្នារវាងលក្ខណៈសម្បត្តិនៃអេឡិចត្រូលីតខ្លាំង ទម្រង់បុរាណច្បាប់នៃសកម្មភាពម៉ាស់អាចត្រូវបានពន្យល់ដោយប្រើទ្រឹស្តីនៃអេឡិចត្រូលីតខ្លាំងដែលស្នើឡើងដោយ Debye និង Hückel។ គំនិតចម្បងនៃទ្រឹស្តីនេះគឺថាកម្លាំងនៃការទាក់ទាញគ្នាទៅវិញទៅមកកើតឡើងរវាងអ៊ីយ៉ុងនៃអេឡិចត្រូលីតខ្លាំងនៅក្នុងដំណោះស្រាយ។ កម្លាំងអន្តរកម្មទាំងនេះបណ្តាលឱ្យឥរិយាបថនៃអេឡិចត្រូលីតខ្លាំងដើម្បីងាកចេញពីច្បាប់នៃដំណោះស្រាយដ៏ល្អ។ វត្តមាននៃអន្តរកម្មទាំងនេះបណ្តាលឱ្យមានការថយចុះទៅវិញទៅមកនៃ cations និង anions ។
ឥទ្ធិពលនៃការពនរលើការទាក់ទាញអន្តរកម្ម។ ការទាក់ទាញអន្តរម៉ូលេគុលបណ្តាលឱ្យមានគម្លាតនៅក្នុងឥរិយាបថនៃដំណោះស្រាយពិតប្រាកដក្នុងវិធីដូចគ្នានឹងការទាក់ទាញអន្តរម៉ូលេគុលនៅក្នុងឧស្ម័នពិតធ្វើឱ្យមានគម្លាតនៅក្នុងអាកប្បកិរិយារបស់ពួកគេពីច្បាប់នៃឧស្ម័នឧត្តមគតិ។ កំហាប់នៃសូលុយស្យុងកាន់តែច្រើន បរិយាកាសអ៊ីយ៉ុងកាន់តែក្រាស់ និងការថយចុះនៃការចល័តរបស់អ៊ីយ៉ុង ហេតុដូច្នេះហើយ ចរន្តអគ្គិសនីនៃអេឡិចត្រូលីត។
ដូចគ្នានឹងលក្ខណៈសម្បត្តិនៃឧស្ម័នពិត សម្ពាធទាបចូលទៅជិតលក្ខណៈសម្បត្តិនៃឧស្ម័នឧត្តមគតិ ដូច្នេះលក្ខណសម្បត្តិនៃដំណោះស្រាយអេឡិចត្រូលីតដ៏រឹងមាំនៅពេលការរំលាយខ្ពស់ ខិតទៅជិតលក្ខណៈសម្បត្តិនៃដំណោះស្រាយដ៏ល្អ។
ម៉្យាងទៀត នៅក្នុងដំណោះស្រាយរលាយ ចម្ងាយរវាងអ៊ីយ៉ុងគឺធំណាស់ ដែលការទាក់ទាញទៅវិញទៅមក ឬការច្រានចោលដែលជួបប្រទះដោយអ៊ីយ៉ុងគឺតូចខ្លាំងណាស់ ហើយអនុវត្តជាក់ស្តែងកាត់បន្ថយដល់សូន្យ។
ដូច្នេះការកើនឡើងនៃចរន្តអគ្គិសនីនៃអេឡិចត្រូលីតខ្លាំងនៅពេលរំលាយដំណោះស្រាយរបស់ពួកគេត្រូវបានពន្យល់ដោយការចុះខ្សោយនៃកម្លាំងអន្តរកម្មនៃការទាក់ទាញនិងការច្រានចោលដែលបណ្តាលឱ្យមានការកើនឡើងនៃល្បឿននៃចលនាអ៊ីយ៉ុង។
អេឡិចត្រូលីតដែលបែកខ្ញែកតិច និងរលាយសូលុយស្យុងកាន់តែច្រើន អាំងទែរតូនិចកាន់តែទាប ឥទ្ធិពលអគ្គិសនីហើយគម្លាតតិចជាងពីច្បាប់នៃសកម្មភាពដ៏ធំត្រូវបានសង្កេតឃើញ ហើយផ្ទុយទៅវិញ ការប្រមូលផ្តុំនៃដំណោះស្រាយកាន់តែច្រើន ឥទ្ធិពលអគ្គិសនីអន្តរកម្មកាន់តែធំ និងគម្លាតកាន់តែច្រើនពីច្បាប់នៃសកម្មភាពម៉ាស់ត្រូវបានអង្កេត។
សម្រាប់ហេតុផលខាងលើ ច្បាប់នៃសកម្មភាពម៉ាស់នៅក្នុងទម្រង់បុរាណរបស់វាមិនអាចត្រូវបានអនុវត្តចំពោះដំណោះស្រាយ aqueous នៃអេឡិចត្រូលីតខ្លាំង ក៏ដូចជាចំពោះដំណោះស្រាយ aqueous ប្រមូលផ្តុំនៃអេឡិចត្រូលីតខ្សោយ។
, , 21 , , ,
, 25-26 , 27-28 ,
, 30, , , , , , , , /2003
§ 6.3 ។ អេឡិចត្រូលីតខ្លាំងនិងខ្សោយ
សម្ភារៈនៅក្នុងផ្នែកនេះគឺស្គាល់មួយផ្នែកសម្រាប់អ្នកពីវគ្គសិក្សាគីមីវិទ្យាដែលបានសិក្សាពីមុន និងពីផ្នែកមុន។ សូមពិនិត្យមើលដោយសង្ខេបនូវអ្វីដែលអ្នកដឹង និងស្គាល់សម្ភារៈថ្មី។
នៅក្នុងផ្នែកមុន យើងបានពិភាក្សាអំពីអាកប្បកិរិយានៅក្នុងដំណោះស្រាយ aqueous នៃអំបិល និងសារធាតុសរីរាង្គមួយចំនួនដែល decompose ទាំងស្រុងទៅជា ions នៅក្នុងដំណោះស្រាយ aqueous ។
មានភ័ស្តុតាងសាមញ្ញមួយចំនួន ប៉ុន្តែមិនសង្ស័យថា សារធាតុមួយចំនួននៅក្នុងដំណោះស្រាយ aqueous រលាយទៅជាភាគល្អិត។ ដូច្នេះ ដំណោះស្រាយ aqueous នៃ sulfuric H 2 SO 4 , nitric HNO 3 , chlorine HClO 4 , hydrochloric (hydrochloric) HCl , acetic CH 3 COOH និងអាស៊ីតផ្សេងទៀតមានរសជាតិជូរ។ នៅក្នុងរូបមន្តនៃអាស៊ីត ភាគល្អិតទូទៅគឺអាតូមអ៊ីដ្រូសែន ហើយវាអាចត្រូវបានសន្មត់ថាវា (ក្នុងទម្រង់ជាអ៊ីយ៉ុង) គឺជាមូលហេតុនៃរសជាតិដូចគ្នានៃសារធាតុទាំងអស់នេះ។
អ៊ីយ៉ុងអ៊ីដ្រូសែនដែលបានបង្កើតឡើងកំឡុងពេលបំបែកនៅក្នុងដំណោះស្រាយ aqueous ផ្តល់ឱ្យដំណោះស្រាយនូវរសជាតិជូរ ដែលជាមូលហេតុដែលសារធាតុបែបនេះត្រូវបានគេហៅថាអាស៊ីត។ នៅក្នុងធម្មជាតិមានតែអ៊ីយ៉ុងអ៊ីដ្រូសែនមានរសជាតិជូរ។ ពួកគេបង្កើតបរិយាកាសអាស៊ីត (អាស៊ីត) នៅក្នុងដំណោះស្រាយ aqueous ។
សូមចាំថា នៅពេលអ្នកនិយាយថា "អ៊ីដ្រូសែនក្លរួ" អ្នកមានន័យថាស្ថានភាពឧស្ម័ន និងគ្រីស្តាល់នៃសារធាតុនេះ ប៉ុន្តែសម្រាប់ដំណោះស្រាយ aqueous អ្នកគួរតែនិយាយថា "ដំណោះស្រាយអាស៊ីត hydrochloric" "អាស៊ីត hydrochloric" ឬប្រើឈ្មោះទូទៅ "អាស៊ីត hydrochloric" ទោះបីជា សមាសភាពនៃសារធាតុនៅក្នុងរដ្ឋណាមួយដែលបង្ហាញដោយរូបមន្តដូចគ្នា - Hcl ។
ដំណោះស្រាយទឹកនៃអ៊ីដ្រូសែននៃលីចូម (LiOH) សូដ្យូម (NaOH) ប៉ូតាស្យូម (KOH) បារីយ៉ូម (Ba (OH) 2) កាល់ស្យូម (Ca (OH) 2) និងលោហធាតុផ្សេងទៀតមានរសជាតិជូរចត់ - សាប៊ូ និងមូលហេតុដូចគ្នា នៅលើស្បែកនៃដៃមានអារម្មណ៍រអិល។ ជាក់ស្តែង អ៊ីយ៉ុង OH- hydroxide ដែលជាផ្នែកមួយនៃសមាសធាតុបែបនេះ ទទួលខុសត្រូវចំពោះទ្រព្យសម្បត្តិនេះ។
Hydrochloric HCl, hydrobromic HBr និងអាស៊ីត hydroiodic HI មានប្រតិកម្មជាមួយស័ង្កសីតាមរបៀបដូចគ្នា ទោះបីជាមានសមាសភាពខុសគ្នាក៏ដោយ ព្រោះវាមិនមែនជាអាស៊ីតដែលពិតជាមានប្រតិកម្មជាមួយស័ង្កសី៖
Zn + 2HCl = ZnCl 2 + H2,
និងអ៊ីយ៉ុងអ៊ីដ្រូសែន៖
Zn + 2H + = Zn 2+ + H 2,
ហើយឧស្ម័នអ៊ីដ្រូសែន និងអ៊ីយ៉ុងស័ង្កសីត្រូវបានបង្កើតឡើង។
ការលាយនៃដំណោះស្រាយអំបិលមួយចំនួន ឧទាហរណ៍ ប៉ូតាស្យូមក្លរួ KCl និងសូដ្យូមនីត្រាត NaNO 3 មិនត្រូវបានអមដោយឥទ្ធិពលកម្ដៅគួរឱ្យកត់សម្គាល់នោះទេ ទោះបីជាបន្ទាប់ពីការហួតនៃដំណោះស្រាយក៏ដោយ ល្បាយនៃគ្រីស្តាល់នៃសារធាតុចំនួនបួនត្រូវបានបង្កើតឡើង៖ សារធាតុដើម - ប៉ូតាស្យូម ក្លរួ និងសូដ្យូមនីត្រាត - និងថ្មី - ប៉ូតាស្យូមនីត្រាត KNO 3 និងសូដ្យូមក្លរួ NaCl ។ វាអាចត្រូវបានសន្មត់ថានៅក្នុងសូលុយស្យុង អំបិលដំបូងទាំងពីរបានរលួយទាំងស្រុងទៅជាអ៊ីយ៉ុង ដែលនៅពេលហួតរបស់វា បង្កើតបានជាបួន។ សារធាតុគ្រីស្តាល់:
ការប្រៀបធៀបព័ត៌មាននេះជាមួយនឹងចរន្តអគ្គិសនីនៃទឹក។ ដំណោះស្រាយអាស៊ីតអ៊ីដ្រូអុកស៊ីត និងអំបិល និងជាមួយនឹងបទប្បញ្ញត្តិមួយចំនួនទៀត S.A. Arrhenius ក្នុងឆ្នាំ 1887 បានដាក់ចេញនូវសម្មតិកម្មនៃការបំបែកអេឡិចត្រូលីត ដែលយោងទៅតាមម៉ូលេគុលនៃអាស៊ីត អ៊ីដ្រូសែន និងអំបិល នៅពេលដែលរលាយក្នុងទឹក បំបែកទៅជាអ៊ីយ៉ុង។
ការសិក្សានៃផលិតផលអេឡិចត្រូលីតអនុញ្ញាតឱ្យអ្នកកំណត់ការចោទប្រកាន់វិជ្ជមានឬអវិជ្ជមានទៅអ៊ីយ៉ុង។ ជាក់ស្តែង ប្រសិនបើអាស៊ីតមួយ ឧទាហរណ៍ nitric HNO 3 dissociates ឧបមាថា ចូលទៅក្នុងអ៊ីយ៉ុងពីរ និងអ៊ីដ្រូសែនត្រូវបានបញ្ចេញកំឡុងពេលអេឡិចត្រូលីតនៃដំណោះស្រាយ aqueous នៅលើ cathode (អេឡិចត្រូតដែលមានបន្ទុកអវិជ្ជមាន) ដូច្នេះហើយមានអ៊ីយ៉ុងអ៊ីដ្រូសែនដែលមានបន្ទុកវិជ្ជមាន។ H + នៅក្នុងដំណោះស្រាយ។ បន្ទាប់មកសមីការ dissociation គួរតែត្រូវបានសរសេរដូចខាងក្រោម:
HNO 3 \u003d H + + ។
ការផ្តាច់ចរន្តអគ្គិសនី- ការរលួយទាំងស្រុង ឬដោយផ្នែកនៃសមាសធាតុ នៅពេលដែលវាត្រូវបានរំលាយនៅក្នុងទឹកទៅជាអ៊ីយ៉ុង ដែលជាលទ្ធផលនៃអន្តរកម្មជាមួយម៉ូលេគុលទឹក (ឬសារធាតុរំលាយផ្សេងទៀត)។
អេឡិចត្រូលីត- អាស៊ីត បាស ឬអំបិល ដំណោះស្រាយ aqueous ដែលដំណើរការ អគ្គិសនីជាលទ្ធផលនៃការបែកបាក់។
សារធាតុដែលមិនបំបែកទៅជាអ៊ីយ៉ុងនៅក្នុងដំណោះស្រាយ aqueous និងដំណោះស្រាយដែលមិនដំណើរការអគ្គិសនីត្រូវបានគេហៅថា មិនមែនអេឡិចត្រូលីត.
ការបំបែកនៃអេឡិចត្រូលីតត្រូវបានកំណត់ជាបរិមាណ កម្រិតនៃការបែកបាក់- សមាមាត្រនៃចំនួន "ម៉ូលេគុល" (ឯកតារូបមន្ត) បំបែកទៅជាអ៊ីយ៉ុងទៅ ចំនួនសរុប"ម៉ូលេគុល" នៃសារធាតុរំលាយ។ កំរិតនៃការបែកគ្នាត្រូវបានបញ្ជាក់ អក្សរក្រិក. ឧទាហរណ៍ ប្រសិនបើក្នុងចំណោម 100 "ម៉ូលេគុល" នៃសារធាតុរំលាយ 80 រលាយទៅជាអ៊ីយ៉ុង នោះកម្រិតនៃការបំបែកនៃសារធាតុរំលាយគឺ: = 80/100 = 0.8 ឬ 80% ។
យោងតាមសមត្ថភាពក្នុងការបំបែក (ឬដូចដែលពួកគេនិយាយថា "ដោយកម្លាំង") អេឡិចត្រូលីតត្រូវបានបែងចែកទៅជា ខ្លាំង,
មធ្យមនិង ខ្សោយ. យោងទៅតាមកម្រិតនៃការបែកគ្នា អេឡិចត្រូលីតខ្លាំងរួមមានអ្នកដែលដំណោះស្រាយ> 30% ខ្សោយ -< 3%, к средним – 3% 30%. Сила электролита –
величина, зависящая от концентрации вещества,
температуры, природы растворителя и др.
នៅក្នុងករណីនៃដំណោះស្រាយ aqueous, អេឡិចត្រូលីតខ្លាំង(> 30%) ជាកម្មសិទ្ធិរបស់ក្រុមនៃសមាសធាតុខាងក្រោម។
1
. អាស៊ីតអសរីរាង្គជាច្រើនដូចជា hydrochloric HCl, nitric HNO 3, sulfuric H 2 SO 4 នៅក្នុងដំណោះស្រាយពនឺ។ អាស៊ីតអសរីរាង្គខ្លាំងបំផុតគឺ perchloric HClO 4 ។
ភាពខ្លាំងនៃអាស៊ីតដែលមិនមានអុកស៊ីហ្សែនកើនឡើងនៅក្នុងស៊េរីនៃសមាសធាតុនៃប្រភេទដូចគ្នានៅពេលផ្លាស់ទីចុះក្រោមក្រុមរងនៃធាតុបង្កើតអាស៊ីត៖
HCl-HBr-HI ។
អាស៊ីត Hydrofluoric (hydrofluoric) HF រំលាយកញ្ចក់ ប៉ុន្តែនេះមិនបង្ហាញពីកម្លាំងរបស់វាទាល់តែសោះ។ អាស៊ីតនេះបានមកពីអាស៊ីដដែលគ្មានផ្ទុកហាឡូហ្សែនគ្មានអុកស៊ីហ្សែនជាកម្មសិទ្ធិរបស់អាស៊ីតកម្លាំងមធ្យមដោយសារ ថាមពលខ្ពស់។ចំណង H-F សមត្ថភាពនៃម៉ូលេគុល HF ក្នុងការរួបរួម (ភ្ជាប់) ដោយសារចំណងអ៊ីដ្រូសែនខ្លាំង អន្តរកម្មនៃអ៊ីយ៉ុង F ជាមួយម៉ូលេគុល HF (ចំណងអ៊ីដ្រូសែន) ជាមួយនឹងការបង្កើតអ៊ីយ៉ុង និងភាគល្អិតស្មុគស្មាញផ្សេងទៀត។ ជាលទ្ធផលការប្រមូលផ្តុំអ៊ីយ៉ុងអ៊ីដ្រូសែននៅក្នុងដំណោះស្រាយ aqueous នៃអាស៊ីតនេះត្រូវបានកាត់បន្ថយយ៉ាងខ្លាំង ដូច្នេះអាស៊ីត hydrofluoric ត្រូវបានចាត់ទុកថាមានកម្លាំងមធ្យម។
អ៊ីដ្រូសែនហ្វ្លុយអូរីមានប្រតិកម្មជាមួយស៊ីលីកុនឌីអុកស៊ីត ដែលជាផ្នែកមួយនៃកញ្ចក់ យោងតាមសមីការ៖SiO 2 + 4HF \u003d SiF 4 + 2H 2 O ។
អាស៊ីត Hydrofluoric មិនត្រូវរក្សាទុកក្នុងកែវឡើយ។ ចំពោះបញ្ហានេះ នាវាដែលធ្វើពីសំណ ប្លាស្ទិក និងកញ្ចក់មួយចំនួនត្រូវបានប្រើប្រាស់ ជញ្ជាំងដែលត្រូវបានគ្របពីខាងក្នុងជាមួយនឹងស្រទាប់ក្រាស់នៃប៉ារ៉ាហ្វីន។ ប្រសិនបើឧស្ម័នអ៊ីដ្រូសែនហ្វ្លុយអូរីតត្រូវបានប្រើដើម្បី "ឆ្លាក់" កញ្ចក់ នោះផ្ទៃកញ្ចក់នឹងក្លាយទៅជាម៉ាត់ ដែលត្រូវបានប្រើដើម្បីអនុវត្តសិលាចារឹក និងលំនាំផ្សេងៗនៅលើកញ្ចក់។ "Etching" កញ្ចក់ជាមួយនឹងដំណោះស្រាយ aqueous នៃអាស៊ីត hydrofluoric លុបផ្ទៃកញ្ចក់ដែលនៅតែមានតម្លាភាព។ នៅលើការលក់ជាធម្មតាដំណោះស្រាយ 40% នៃអាស៊ីត hydrofluoric ។
ភាពខ្លាំងនៃប្រភេទដូចគ្នានៃអាស៊ីតអុកស៊ីហ្សែនផ្លាស់ប្តូរក្នុងទិសដៅផ្ទុយ ឧទាហរណ៍ អាស៊ីតអ៊ីយ៉ូត HIO 4 គឺខ្សោយជាងអាស៊ីត perchloric HClO 4 ។
ប្រសិនបើធាតុបង្កើតជាអាស៊ីតអុកស៊ីហ៊្សែនច្រើន នោះអាស៊ីតដែលធាតុបង្កើតអាស៊ីតមាន valence ខ្ពស់បំផុតមានកម្លាំងខ្លាំងបំផុត។ ដូច្នេះនៅក្នុងស៊េរីនៃអាស៊ីត HclO (hypochlorous) - HclO 2 (chloric) - HclO 3 (chloric) - HclO 4 (chloric) ក្រោយមកទៀតគឺខ្លាំងបំផុត។
បរិមាណទឹកមួយរលាយប្រហែលពីរភាគនៃក្លរីន។ ក្លរីន (ប្រហែលពាក់កណ្តាលរបស់វា) ធ្វើអន្តរកម្មជាមួយទឹក៖
Cl 2 + H 2 O \u003d HCl + HClO ។
អាស៊ីត hydrochloric គឺខ្លាំង; ជាក់ស្តែងមិនមានម៉ូលេគុល HCl នៅក្នុងដំណោះស្រាយ aqueous របស់វា។ សមីការត្រឹមត្រូវសម្រាប់ប្រតិកម្មគឺ៖
Cl 2 + H 2 O \u003d H + + Cl - + HClO - 25 kJ / mol ។
ដំណោះស្រាយលទ្ធផលត្រូវបានគេហៅថាទឹកក្លរីន។
អាស៊ីត Hypochlorous- ភ្នាក់ងារអុកស៊ីតកម្មដែលមានសកម្មភាពលឿន ដូច្នេះវាត្រូវបានប្រើសម្រាប់ក្រណាត់ bleaching ។
2 . អ៊ីដ្រូសែននៃធាតុនៃក្រុមរងសំខាន់នៃក្រុម I និង II ប្រព័ន្ធតាមកាលកំណត់៖ LiOH, NaOH, KOH, Ca (OH) 2 ។ល។ នៅពេលដែលផ្លាស់ទីចុះក្រោមក្រុមរង នៅពេលដែលលក្ខណៈសម្បត្តិលោហធាតុនៃធាតុកើនឡើង កម្លាំងនៃអ៊ីដ្រូសែនកើនឡើង។ អ៊ីដ្រូសែនរលាយនៃក្រុមរងសំខាន់នៃក្រុម I ត្រូវបានចាត់ថ្នាក់ជាអាល់កាឡាំង។
មូលដ្ឋានរលាយក្នុងទឹកត្រូវបានគេហៅថាអាល់កាឡាំង។ ទាំងនេះក៏រួមបញ្ចូលអ៊ីដ្រូសែននៃធាតុនៃក្រុមរងសំខាន់នៃក្រុមទី II (លោហធាតុអាល់កាឡាំងផែនដី) និងអាម៉ូញ៉ូមអ៊ីដ្រូស៊ីត (ដំណោះស្រាយទឹកនៃអាម៉ូញាក់) ។ ជួនកាលអាល់កាឡាំងគឺជាអ៊ីដ្រូសែនដែលបង្កើតកំហាប់ខ្ពស់នៃអ៊ីយ៉ុងអ៊ីដ្រូសែននៅក្នុងដំណោះស្រាយទឹកមួយ។ នៅក្នុងអក្សរសិល្ប៍ហួសសម័យ អ្នកអាចរកឃើញប៉ូតាស្យូមកាបូណាត K 2 CO 3 (ប៉ូតាស្យូម) និងសូដ្យូម Na 2 CO 3 (សូដា) សូដ្យូមប៊ីកាបូណាត NaHCO 3 ( ផឹកសូដា), borax Na 2 B 4 O 7 , sodium hydrosulfide NaHS និងប៉ូតាស្យូម KHS ជាដើម។
Calcium hydroxide Ca (OH) 2 ជាអេឡិចត្រូលីតខ្លាំងបំបែកជាជំហានមួយ៖
Ca (OH) 2 \u003d Ca 2+ + 2OH - ។
3 . អំបិលស្ទើរតែទាំងអស់។ អំបិល ប្រសិនបើវាជាអេឡិចត្រូលីតខ្លាំង បំបែកទៅជាជំហានមួយ ឧទាហរណ៍ ferric chloride៖
FeCl 3 \u003d Fe 3+ + 3Cl - ។
នៅក្នុងករណីនៃដំណោះស្រាយ aqueous, អេឡិចត្រូលីតខ្សោយ ( < 3%) относят перечисленные ниже соединения.
1 . ទឹក H 2 O គឺជាអេឡិចត្រូលីតដ៏សំខាន់បំផុត។
2
. អាស៊ីតសរីរាង្គ និងស្ទើរតែទាំងអស់៖ H 2 S (hydrosulfide), H 2 SO 3 (ស្ពាន់ធ័រ), H 2 CO 3 (កាបូន), HCN (hydrocyanic), H 3 PO 4 (ផូស្វ័រ, ផូស្វ័រ), H 2 SiO 3 (ស៊ីលីកុន), H 3 BO 3 (boric, orthoboric), CH 3 COOH (អាសេទិក) ។ល។
ចំណាំថាអាស៊ីតកាបូនមិនមាននៅក្នុងរូបមន្ត H 2 CO 3 ទេ។ នៅពេលរំលាយ កាបូនឌីអុកស៊ីត CO 2 នៅក្នុងទឹកបង្កើតជា hydrate CO 2 H 2 O របស់វា ដែលយើងសរសេរសម្រាប់ភាពងាយស្រួលនៃការគណនាដោយរូបមន្ត H 2 CO 3 ហើយសមីការសម្រាប់ប្រតិកម្ម dissociation មើលទៅដូចនេះ៖
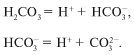
ការបំបែកអាស៊ីតកាបូនិកខ្សោយដំណើរការជាពីរជំហាន។ លទ្ធផលអ៊ីយ៉ុងប៊ីកាបូណាតក៏មានឥរិយាបទដូចអេឡិចត្រូលីតខ្សោយដែរ។
អាស៊ីត polybasic ផ្សេងទៀតបំបែកតាមរបៀបដូចគ្នា: H 3 PO 4 (ផូស្វ័រ), H 2 SiO 3 (ស៊ីលីកុន), H 3 BO 3 (boric) ។ នៅក្នុងដំណោះស្រាយ aqueous, dissociation អនុវត្តបានតែតាមរយៈដំណាក់កាលដំបូង។ តើធ្វើដូចម្តេចដើម្បីអនុវត្តការបំបែកនៅតាមបណ្តោយជំហានចុងក្រោយ?
3
. អ៊ីដ្រូសែននៃធាតុជាច្រើនដូចជា Al (OH) 3, Cu (OH) 2, Fe (OH) 2, Fe (OH) 3 ជាដើម។
អ៊ីដ្រូអុកស៊ីតទាំងអស់នេះបំបែកនៅក្នុងដំណោះស្រាយ aqueous ក្នុងជំហាន ឧទាហរណ៍ អ៊ីដ្រូអុកស៊ីតជាតិដែក
Fe (OH) 3:
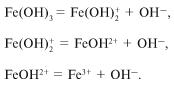
នៅក្នុងដំណោះស្រាយ aqueous, dissociation ដំណើរការអនុវត្តតែតាមរយៈដំណាក់កាលដំបូង។ តើធ្វើដូចម្តេចដើម្បីផ្លាស់ប្តូរលំនឹងឆ្ពោះទៅរកការបង្កើតអ៊ីយ៉ុង Fe 3+?
លក្ខណៈសម្បត្តិសំខាន់នៃអ៊ីដ្រូអុកស៊ីតនៃធាតុដូចគ្នាកើនឡើងជាមួយនឹងការថយចុះនៃវ៉ាឡង់នៃធាតុ។ ដូច្នេះលក្ខណៈសម្បត្តិសំខាន់នៃជាតិដែក dihydroxide Fe (OH) 2 គឺច្បាស់ជាង Fe (OH) 3 trihydroxide ។ សេចក្តីថ្លែងការណ៍នេះគឺស្មើនឹង លក្ខណៈសម្បត្តិអាស៊ីត Fe(OH) 3 គឺច្បាស់ជាង Fe(OH) 2 ។
4
. អាម៉ូញ៉ូមអ៊ីដ្រូសែន NH 4 OH ។
នៅពេលដែលឧស្ម័នអាម៉ូញាក់ NH 3 ត្រូវបានរំលាយនៅក្នុងទឹក ដំណោះស្រាយមួយត្រូវបានទទួល ដែលធ្វើចរន្តអគ្គិសនីបានតិចតួច និងមានរសជាតិជូរចត់។ ឧបករណ៍ផ្ទុកដំណោះស្រាយគឺមូលដ្ឋាន ឬអាល់កាឡាំង។ ឥរិយាបថនៃអាម៉ូញាក់នេះត្រូវបានពន្យល់ដូចខាងក្រោម។ នៅពេលដែលអាម៉ូញាក់ត្រូវបានរំលាយនៅក្នុងទឹក អាម៉ូញាក់អ៊ីដ្រូសែន NH 3 H 2 O ត្រូវបានបង្កើតឡើង ដែលយើងកំណត់លក្ខខណ្ឌតាមលក្ខខណ្ឌរូបមន្តនៃអាម៉ូញ៉ូមអ៊ីដ្រូសែន NH 4 ដែលមិនមាន។ OH សន្មត់ថាសមាសធាតុនេះផ្តាច់ជាមួយនឹងការបង្កើតអ៊ីយ៉ុងអាម៉ូញ៉ូម និងអ៊ីដ្រូសែនអ៊ីដ្រូសែន OH -៖
NH 4 OH \u003d + OH - ។
5 . អំបិលមួយចំនួន៖ ស័ង្កសីក្លរួ ZnCl 2, ជាតិដែក thiocyanate Fe (NCS) 3, បារត cyanide Hg (CN) 2 ។ល។ អំបិលទាំងនេះបំបែកជាជំហានៗ។
សម្រាប់អេឡិចត្រូលីតនៃកម្លាំងមធ្យម មួយចំនួនរួមមានអាស៊ីតផូស្វ័រ H 3 PO 4 ។ យើងនឹងពិចារណាអាស៊ីតផូស្វ័រជាអេឡិចត្រូលីតខ្សោយ ហើយសរសេរជំហានទាំងបីនៃការបំបែករបស់វា។ អាស៊ីតស៊ុលហ្វួរីកនៅក្នុងដំណោះស្រាយប្រមូលផ្តុំមានឥរិយាបទដូចជាអេឡិចត្រូលីតនៃកម្លាំងមធ្យម ហើយនៅក្នុងខ្លាំងណាស់ ដំណោះស្រាយប្រមូលផ្តុំជាអេឡិចត្រូលីតខ្សោយ។ យើងនឹងពិចារណាបន្ថែមលើអាស៊ីតស៊ុលហ្វួរិកជាអេឡិចត្រូលីតដ៏រឹងមាំ ហើយសរសេរសមីការសម្រាប់ការបំបែករបស់វាក្នុងមួយជំហាន។
ការបែកខ្ញែកនៃអេឡិចត្រូលីតត្រូវបានកំណត់ជាបរិមាណដោយកម្រិតនៃការបំបែក។ កម្រិតនៃការបែកបាក់គ្នា ក–គឺជាសមាមាត្រនៃចំនួនម៉ូលេគុលដែលបំបែកទៅជាអ៊ីយ៉ុង N ឌីស។,ទៅចំនួនសរុបនៃម៉ូលេគុលអេឡិចត្រូលីតរលាយ N :
ក =
កគឺជាប្រភាគនៃម៉ូលេគុលអេឡិចត្រូលីតដែលបំបែកទៅជាអ៊ីយ៉ុង។
កម្រិតនៃការបំបែកអេឡិចត្រូលីតអាស្រ័យទៅលើកត្តាជាច្រើន៖ ធម្មជាតិនៃអេឡិចត្រូលីត ធម្មជាតិនៃសារធាតុរំលាយ កំហាប់នៃដំណោះស្រាយ និងសីតុណ្ហភាព។
យោងតាមសមត្ថភាពក្នុងការបំបែកអេឡិចត្រូលីតត្រូវបានបែងចែកតាមលក្ខខណ្ឌទៅជាខ្លាំងនិងខ្សោយ។ អេឡិចត្រូលីតដែលមាននៅក្នុងដំណោះស្រាយតែជាអ៊ីយ៉ុងត្រូវបានគេហៅថា ខ្លាំង . អេឡិចត្រូលីត ដែលស្ថិតក្នុងស្ថានភាពរលាយមួយផ្នែកក្នុងទម្រង់ជាម៉ូលេគុល និងមួយផ្នែកក្នុងទម្រង់ជាអ៊ីយ៉ុង ត្រូវបានគេហៅថា ខ្សោយ .
អេឡិចត្រូលីតខ្លាំងរួមមានអំបិលស្ទើរតែទាំងអស់ អាស៊ីតមួយចំនួន៖ H 2 SO 4 HNO 3 HCl HI HClO 4 អ៊ីដ្រូសែននៃលោហធាតុអាល់កាឡាំង និងអាល់កាឡាំងផែនដី (សូមមើលឧបសម្ព័ន្ធតារាងទី 6) ។
ដំណើរការនៃការបំបែកអេឡិចត្រូលីតខ្លាំងទៅទីបញ្ចប់៖
HNO 3 \u003d H + + NO 3 -, NaOH \u003d Na + + OH -,
ហើយសញ្ញាស្មើគ្នាត្រូវបានដាក់ក្នុងសមីការការបំបែក។
ទាក់ទងនឹងអេឡិចត្រូលីតខ្លាំង គំនិតនៃ "កម្រិតនៃការផ្តាច់ខ្លួន" គឺ តាមលក្ខខណ្ឌ. « កម្រិតនៃការបែកគ្នាច្បាស់លាស់ (កនីមួយៗ) ខាងក្រោមពិត (សូមមើលឧបសម្ព័ន្ធ តារាងទី ៦)។ ជាមួយនឹងការកើនឡើងនៃកំហាប់នៃអេឡិចត្រូលីតដ៏ខ្លាំងនៅក្នុងដំណោះស្រាយ អន្តរកម្មនៃអ៊ីយ៉ុងដែលមានបន្ទុកផ្ទុយនឹងកើនឡើង។ ពេលចូលជិតគ្នាគ្រប់គ្រាន់ គេបង្កើតជាសហការី។ អ៊ីយ៉ុងនៅក្នុងពួកវាត្រូវបានបំបែកដោយស្រទាប់នៃម៉ូលេគុលទឹកប៉ូលជុំវិញអ៊ីយ៉ុងនីមួយៗ។ នេះប៉ះពាល់ដល់ការថយចុះនៃចរន្តអគ្គិសនីនៃដំណោះស្រាយ, i.e. ឥទ្ធិពលនៃការបំបែកមិនពេញលេញត្រូវបានបង្កើតឡើង។
ដើម្បីគិតគូរពីប្រសិទ្ធភាពនេះ មេគុណសកម្មភាព g ត្រូវបានណែនាំ ដែលថយចុះជាមួយនឹងការកើនឡើងនៃកំហាប់នៃដំណោះស្រាយ ប្រែប្រួលពី 0 ទៅ 1។ ដើម្បីពិពណ៌នាជាបរិមាណអំពីលក្ខណៈសម្បត្តិនៃដំណោះស្រាយនៃអេឡិចត្រូលីតខ្លាំង បរិមាណមួយហៅថា សកម្មភាព (ក).
សកម្មភាពរបស់អ៊ីយ៉ុង ត្រូវបានគេយល់ថាជា ការផ្តោតអារម្មណ៍ប្រកបដោយប្រសិទ្ធភាពយោងទៅតាមវាដើរតួក្នុងប្រតិកម្មគីមី។
សកម្មភាពអ៊ីយ៉ុង ( ក) គឺស្មើនឹងកំហាប់នៃថ្គាមរបស់វា ( ពី) គុណនឹងកត្តាសកម្មភាព (g)៖
ក = g ពី.
ការប្រើប្រាស់សកម្មភាពជំនួសឱ្យការផ្តោតអារម្មណ៍ធ្វើឱ្យវាអាចអនុវត្តទៅដំណោះស្រាយភាពទៀងទាត់ដែលបានបង្កើតឡើងសម្រាប់ដំណោះស្រាយដ៏ល្អ។
អេឡិចត្រូលីតខ្សោយរួមមានសារធាតុរ៉ែមួយចំនួន (HNO 2, H 2 SO 3, H 2 S, H 2 SiO 3, HCN, H 3 PO 4) និងភាគច្រើន។ អាស៊ីតសរីរាង្គ(CH 3 COOH, H 2 C 2 O 4 ។
ការបំបែកនៃអេឡិចត្រូលីតខ្សោយគឺអាចបញ្ច្រាស់បាន។ នៅក្នុងដំណោះស្រាយនៃអេឡិចត្រូលីតខ្សោយ លំនឹងមួយត្រូវបានបង្កើតឡើងរវាងអ៊ីយ៉ុង និងម៉ូលេគុលដែលមិនមានទំនាក់ទំនង។ នៅក្នុងសមីការ dissociation ដែលត្រូវគ្នា សញ្ញានៃការបញ្ច្រាស់ ("") ត្រូវបានដាក់។ ជាឧទាហរណ៍ សមីការការបំបែកសម្រាប់អាស៊ីតអាសេទិកខ្សោយត្រូវបានសរសេរដូចខាងក្រោម៖
CH 3 COOH « CH 3 COO - + H + ។
នៅក្នុងដំណោះស្រាយនៃអេឡិចត្រូលីតគោលពីរខ្សោយ ( ខេ) លំនឹងខាងក្រោមត្រូវបានបង្កើតឡើង កំណត់ដោយថេរលំនឹងដែលហៅថា ថេរ dissociation ទៅឃ៖
KA "K + + A -,
![]() .
.
ប្រសិនបើរំលាយក្នុង 1 លីត្រនៃដំណោះស្រាយ ពី moles នៃអេឡិចត្រូលីត ខេហើយកម្រិតនៃការបែកគ្នាគឺស្មើនឹង a ដែលមានន័យថាផ្តាច់ aС moles នៃអេឡិចត្រូលីតនិងអ៊ីយ៉ុងនីមួយៗត្រូវបានបង្កើតឡើងយោងទៅតាម aСប្រជ្រុយ។ នៅតែស្ថិតក្នុងស្ថានភាពមិនទាក់ទងគ្នា ( ពី – aС) ប្រជ្រុយ ខេ.
KA « K + + A - .
គ - aC aC aC
បន្ទាប់មក ថេរ dissociation នឹងស្មើនឹង៖
![]() (6.1)
(6.1)
ដោយសារតែថេរ dissociation មិនអាស្រ័យលើការផ្តោតអារម្មណ៍, ទំនាក់ទំនងដែលទទួលបានបង្ហាញពីការពឹងផ្អែកនៃកម្រិតនៃការ dissociation នៃអេឡិចត្រូលីតគោលពីរខ្សោយនៅលើការប្រមូលផ្តុំរបស់វា។ សមីការ (6.1) បង្ហាញថាការថយចុះនៃកំហាប់នៃអេឡិចត្រូលីតខ្សោយនៅក្នុងដំណោះស្រាយនាំឱ្យមានការកើនឡើងនៃកម្រិតនៃការបំបែករបស់វា។ សមីការ (6.1) បង្ហាញ ច្បាប់នៃការរំលាយរបស់ Ostwald .
សម្រាប់អេឡិចត្រូលីតខ្សោយខ្លាំង (នៅ ក<<1), уравнение Оствальда можно записать следующим образом:
ទៅឃ a 2 គ, ឬ ក» (6.2)
ថេរ dissociation សម្រាប់អេឡិចត្រូលីតនីមួយៗគឺថេរនៅសីតុណ្ហភាពដែលបានផ្តល់ឱ្យវាមិនអាស្រ័យលើការប្រមូលផ្តុំនៃដំណោះស្រាយនិងកំណត់លក្ខណៈសមត្ថភាពនៃអេឡិចត្រូលីតដើម្បី decompose ទៅជាអ៊ីយ៉ុង។ Kd កាន់តែខ្ពស់ អេឡិចត្រូលីតកាន់តែបំបែកទៅជាអ៊ីយ៉ុង។ ថេរ dissociation នៃអេឡិចត្រូលីតខ្សោយត្រូវបានដាក់ជាតារាង (សូមមើលឧបសម្ព័ន្ធតារាងទី 3) ។
អេឡិចត្រូលីតខ្លាំងនិងខ្សោយ
នៅក្នុងដំណោះស្រាយនៃអេឡិចត្រូលីតមួយចំនួន មានតែផ្នែកមួយនៃម៉ូលេគុលប៉ុណ្ណោះដែលបំបែក។ សម្រាប់លក្ខណៈបរិមាណនៃកម្លាំងនៃអេឡិចត្រូលីត គំនិតនៃកម្រិតនៃការបំបែកត្រូវបានណែនាំ។ សមាមាត្រនៃចំនួនម៉ូលេគុលដែលបំបែកទៅជាអ៊ីយ៉ុងទៅនឹងចំនួនសរុបនៃម៉ូលេគុលនៃសារធាតុរំលាយត្រូវបានគេហៅថា កម្រិតនៃការបំបែក a.
ដែល C គឺជាកំហាប់នៃម៉ូលេគុលដែលបែកគ្នា mol/l;
C 0 - កំហាប់ដំបូងនៃដំណោះស្រាយ, mol / l ។
យោងទៅតាមកម្រិតនៃការបំបែកអេឡិចត្រូលីតទាំងអស់ត្រូវបានបែងចែកទៅជាខ្លាំងនិងខ្សោយ។ អេឡិចត្រូលីតខ្លាំង រួមមានអ្នកដែលមានកម្រិតនៃការផ្តាច់ខ្លួនលើសពី 30% (a> 0.3)។ ទាំងនេះរួមបញ្ចូលទាំង:
អាស៊ីតខ្លាំង (H 2 SO 4, HNO 3, HCl, HBr, HI);
· អ៊ីដ្រូសែនរលាយ លើកលែងតែ NH 4 OH;
អំបិលរលាយ។
ការបំបែកអេឡិចត្រូលីតនៃអេឡិចត្រូលីតខ្លាំងដំណើរការដោយមិនអាចត្រឡប់វិញបាន។
HNO 3 ® H + + NO - 3 ។
អេឡិចត្រូលីតខ្សោយមានកម្រិតបំបែកតិចជាង 2% (ក< 0,02). К ним относятся:
អាស៊ីតអសរីរាង្គខ្សោយ (H 2 CO 3, H 2 S, HNO 2, HCN, H 2 SiO 3 ជាដើម) និងសារធាតុសរីរាង្គទាំងអស់ ឧទាហរណ៍ អាស៊ីតអាសេទិក (CH 3 COOH);
· អ៊ីដ្រូសែនមិនរលាយ ក៏ដូចជាអ៊ីដ្រូសែនរលាយ NH 4 OH;
អំបិលមិនរលាយ។
អេឡិចត្រូលីតដែលមានតម្លៃមធ្យមនៃកម្រិតនៃការបំបែកត្រូវបានគេហៅថាអេឡិចត្រូលីតនៃកម្លាំងមធ្យម។
កម្រិតនៃការបែកបាក់ (ក) អាស្រ័យលើកត្តាខាងក្រោម៖
នៅលើធម្មជាតិនៃអេឡិចត្រូលីត, នោះគឺនៅលើប្រភេទនៃចំណងគីមី; ការបែកខ្ញែកកើតឡើងយ៉ាងងាយស្រួលបំផុតនៅកន្លែងនៃចំណងប៉ូលបំផុត;
ពីធម្មជាតិនៃសារធាតុរំលាយ - ប៉ូលកាន់តែច្រើននៅពេលក្រោយ ដំណើរការបំបែកកាន់តែងាយស្រួលនៅក្នុងវា;
នៅលើសីតុណ្ហភាព - ការកើនឡើងនៃសីតុណ្ហភាពបង្កើនការបំបែក;
នៅលើកំហាប់នៃដំណោះស្រាយ - នៅពេលដែលដំណោះស្រាយត្រូវបានពនឺការបំបែកក៏កើនឡើងផងដែរ។
ជាឧទាហរណ៍នៃការពឹងផ្អែកនៃកម្រិតនៃការផ្តាច់ទំនាក់ទំនងលើធម្មជាតិនៃចំណងគីមី សូមពិចារណាការបំបែកនៃសូដ្យូមអ៊ីដ្រូស៊ុលហ្វាត (NaHSO 4) នៅក្នុងម៉ូលេគុលដែលមានប្រភេទចំណងដូចខាងក្រោមៈ 1- អ៊ីយ៉ុង; 2 - covalent ប៉ូល; 3 - ចំណងរវាងអាតូមស្ពាន់ធ័រ និងអុកស៊ីហ្សែន មានប៉ូលតិច។ ការដាច់រហែកកើតឡើងយ៉ាងងាយបំផុតនៅកន្លែងនៃចំណងអ៊ីយ៉ុង (១)៖
| Na 1 O 3 O S 3 H 2 O | 1. NaHSO 4 ® Na + + HSO - 4, 2. បន្ទាប់មកនៅកន្លែងនៃចំណងប៉ូលនៃសញ្ញាប័ត្រតិចជាង: HSO - 4 ® H + + SO 2 - 4 ។ 3. សំណល់អាស៊ីតមិនបំបែកទៅជាអ៊ីយ៉ុងទេ។ |
កម្រិតនៃការបំបែកអេឡិចត្រូលីតគឺពឹងផ្អែកយ៉ាងខ្លាំងទៅលើលក្ខណៈនៃសារធាតុរំលាយ។ ឧទាហរណ៍ HCl dissociates យ៉ាងខ្លាំងនៅក្នុងទឹក, ខ្សោយនៅក្នុងអេតាណុល C 2 H 5 OH, ស្ទើរតែមិន dissociate នៅក្នុង benzene ដែលក្នុងនោះវាមិនអនុវត្តចរន្តអគ្គិសនី។ សារធាតុរំលាយដែលមានភាពអនុញ្ញាតខ្ពស់ (e) បង្កើតប៉ូឡូញម៉ូលេគុលរលាយ និងបង្កើតអ៊ីយ៉ុងដែលរលាយ (hydrated) ជាមួយពួកវា។ នៅ 25 0 С e (H 2 O) \u003d 78.5, e (C 2 H 5 OH) \u003d 24.2, e (C 6 H 6) \u003d 2.27 ។
នៅក្នុងដំណោះស្រាយនៃអេឡិចត្រូលីតខ្សោយ ដំណើរការបំបែកដំណើរការបញ្ច្រាស់ ហើយដូច្នេះច្បាប់នៃលំនឹងគីមីអាចអនុវត្តបានចំពោះលំនឹងនៅក្នុងដំណោះស្រាយរវាងម៉ូលេគុល និងអ៊ីយ៉ុង។ ដូច្នេះសម្រាប់ការបំបែកអាស៊ីតអាសេទិក
CH 3 COOH « CH 3 COO - + H + ។
លំនឹងថេរ K ជាមួយ នឹងត្រូវបានកំណត់ជា
K c \u003d K d \u003d CCH 3 COO - · C H + / CCH 3 COOH ។
ថេរលំនឹង (K c) សម្រាប់ដំណើរការ dissociation ត្រូវបានគេហៅថា dissociation constant (K d)។ តម្លៃរបស់វាអាស្រ័យលើធម្មជាតិនៃអេឡិចត្រូលីត សារធាតុរំលាយ និងសីតុណ្ហភាព ប៉ុន្តែវាមិនអាស្រ័យលើកំហាប់នៃអេឡិចត្រូលីតនៅក្នុងដំណោះស្រាយនោះទេ។ ថេរ dissociation គឺជាលក្ខណៈសំខាន់នៃអេឡិចត្រូលីតខ្សោយ ព្រោះវាបង្ហាញពីកម្លាំងនៃម៉ូលេគុលរបស់ពួកគេនៅក្នុងដំណោះស្រាយ។ ភាពថេរនៃការបំបែកកាន់តែតូច អេឡិចត្រូលីតកាន់តែខ្សោយ ហើយម៉ូលេគុលរបស់វាកាន់តែមានស្ថេរភាព។ បានផ្តល់ឱ្យថាកម្រិតនៃការ dissociation ផ្ទុយទៅនឹង dissociation ថេរការផ្លាស់ប្តូរជាមួយនឹងការផ្តោតអារម្មណ៍នៃដំណោះស្រាយ, វាគឺជាការចាំបាច់ដើម្បីស្វែងរកទំនាក់ទំនងរវាង K d និង a ។ ប្រសិនបើកំហាប់ដំបូងនៃដំណោះស្រាយត្រូវបានយកស្មើនឹង C ហើយកម្រិតនៃការបំបែកដែលត្រូវគ្នាទៅនឹងកំហាប់ a នេះ នោះចំនួននៃម៉ូលេគុលអាស៊ីតអាសេទិកដែលបែកគ្នានឹងស្មើនឹង C. ចាប់តាំងពី
CCH 3 COO - \u003d C H + \u003d a C,
បន្ទាប់មកកំហាប់នៃម៉ូលេគុលអាស៊ីតអាសេទិកដែលមិនទាន់រលួយនឹងស្មើនឹង (C - a C) ឬ C (1 - a C) ។ ពីទីនេះ
K d \u003d aC a C / (C - a C) \u003d a 2 C / (1- a) ។ (1)
សមីការ (1) បង្ហាញពីច្បាប់នៃការរំលាយ Ostwald ។ សម្រាប់អេឡិចត្រូលីតខ្សោយខ្លាំង ក<<1, то приближенно К @ a 2 С и
a=(K/C)។ (2)
ដូចដែលអាចមើលឃើញពីរូបមន្ត (2) ជាមួយនឹងការថយចុះនៃកំហាប់នៃសូលុយស្យុងអេឡិចត្រូលីត (នៅពេលត្រូវបានពនឺ) កម្រិតនៃការបំបែកនឹងកើនឡើង។
អេឡិចត្រូលីតខ្សោយបំបែកជាដំណាក់កាលឧទាហរណ៍៖
1 ដំណាក់កាល H 2 CO 3 "H + + HCO - 3,
2 ដំណាក់កាល HCO - 3 "H + + CO 2 - 3 ។
អេឡិចត្រូលីតបែបនេះត្រូវបានកំណត់លក្ខណៈដោយថេរជាច្រើន - អាស្រ័យលើចំនួនដំណាក់កាលនៃការរលួយទៅជាអ៊ីយ៉ុង។ សម្រាប់អាស៊ីតកាបូន
K 1 \u003d CH + CHCO - 2 / CH 2 CO 3 \u003d 4.45 × 10 -7; K 2 \u003d CH + · CCO 2- 3 / CHCO - 3 \u003d 4.7 × 10 -11 ។
ដូចដែលអាចមើលឃើញ ការបំបែកទៅជាអ៊ីយ៉ុងអាស៊ីតកាបូនត្រូវបានកំណត់ជាចម្បងដោយដំណាក់កាលទី 1 ខណៈពេលដែលទីពីរអាចបង្ហាញដោយខ្លួនឯងបានតែនៅពេលដែលដំណោះស្រាយត្រូវបានពនរខ្លាំង។
លំនឹងសរុប H 2 CO 3 « 2H + + CO 2 - 3 ត្រូវគ្នាទៅនឹងថេរ dissociation សរុប
K d \u003d C 2 n + · CCO 2- 3 / CH 2 CO 3 ។
តម្លៃនៃ K 1 និង K 2 គឺទាក់ទងគ្នាទៅវិញទៅមកដោយទំនាក់ទំនង
K d \u003d K 1 K ២.
មូលដ្ឋាននៃលោហធាតុចម្រុះបំបែកក្នុងលក្ខណៈស្រដៀងគ្នា។ ឧទហរណ៍ ពីរជំហាននៃការបំបែកនៃ hydroxide ទង់ដែង
Cu (OH) 2 "CuOH + + OH -,
CuOH + "Cu 2+ + OH -
ត្រូវនឹងថេរ dissociation
K 1 \u003d CCuOH + SON - / CCu (OH) 2 និង K 2 \u003d Ccu 2+ SON - / CCuOH + ។
ចាប់តាំងពីអេឡិចត្រូលីតខ្លាំងត្រូវបានបំបែកទាំងស្រុងនៅក្នុងដំណោះស្រាយ នោះពាក្យថា dissociation ថេរសម្រាប់ពួកវាគឺគ្មានន័យទេ។
ការបំបែកនៃថ្នាក់ផ្សេងៗនៃអេឡិចត្រូលីត
តាមទស្សនៈនៃទ្រឹស្តីនៃការផ្តាច់ចរន្តអគ្គិសនី អាស៊ីត សារធាតុមួយត្រូវបានគេហៅថា កំឡុងពេលបំបែក ដែលមានតែអ៊ីយ៉ុងអ៊ីដ្រូសែន H 3 O (ឬសាមញ្ញ H +) ត្រូវបានបង្កើតឡើងជា cation ។
គ្រឹះសារធាតុត្រូវបានគេហៅថាសារធាតុដែលនៅក្នុងដំណោះស្រាយ aqueous បង្កើតជា OH hydroxide ions ជា anion និងមិនមាន anions ផ្សេងទៀត។
យោងតាមទ្រឹស្ដីរបស់ Bronsted អាស៊ីតមួយគឺជាអ្នកបរិច្ចាគប្រូតុង ហើយមូលដ្ឋានគឺជាអ្នកទទួលប្រូតុង។
កម្លាំងនៃមូលដ្ឋាន ដូចជាកម្លាំងនៃអាស៊ីត អាស្រ័យលើតម្លៃនៃថេរ dissociation ។ ភាពថេរនៃការបំបែកកាន់តែធំ អេឡិចត្រូលីតកាន់តែខ្លាំង។
មានអ៊ីដ្រូសែនដែលអាចធ្វើអន្តរកម្ម និងបង្កើតជាអំបិលមិនត្រឹមតែជាមួយអាស៊ីតប៉ុណ្ណោះទេ ប៉ុន្តែក៏មានមូលដ្ឋានផងដែរ។ អ៊ីដ្រូសែនបែបនេះត្រូវបានគេហៅថា amphoteric ។ ទាំងនេះរួមបញ្ចូលទាំង Be(OH) 2 , Zn(OH) 2 , Sn(OH) 2 , Pb(OH) 2 , Cr(OH) 3 , Al(OH) 3. លក្ខណៈសម្បត្តិរបស់ពួកគេគឺដោយសារតែការពិតដែលថាពួកវាបំបែកទៅជាកម្រិតខ្សោយយោងទៅតាមប្រភេទនៃអាស៊ីតនិងប្រភេទនៃមូលដ្ឋាន។
H++ RO- « ROH « R + + OH -.
លំនឹងនេះត្រូវបានពន្យល់ដោយការពិតដែលថាភាពខ្លាំងនៃចំណងរវាងលោហៈនិងអុកស៊ីហ៊្សែនខុសគ្នាបន្តិចបន្តួចពីភាពរឹងមាំនៃចំណងរវាងអុកស៊ីសែននិងអ៊ីដ្រូសែន។ ដូច្នេះនៅពេលដែល beryllium hydroxide មានប្រតិកម្មជាមួយនឹងអាស៊ីត hydrochloric, beryllium chloride ត្រូវបានទទួល។
Be (OH) 2 + HCl \u003d BeCl 2 + 2H 2 O,
ហើយនៅពេលធ្វើអន្តរកម្មជាមួយសូដ្យូមអ៊ីដ្រូសែន - សូដ្យូមបេរីឡាត
Be (OH) 2 + 2NaOH \u003d Na 2 BeO 2 + 2H 2 O ។
អំបិលអាចត្រូវបានកំណត់ថាជាអេឡិចត្រូលីតដែលបំបែកក្នុងដំណោះស្រាយក្នុងការបង្កើតជា cations ផ្សេងពីអ៊ីដ្រូសែន cations និង anions ផ្សេងទៀតជាង hydroxide ions ។
អំបិលមធ្យម, ទទួលបានជាមួយនឹងការជំនួសពេញលេញនៃអ៊ីយ៉ុងអ៊ីដ្រូសែននៃអាស៊ីតដែលត្រូវគ្នាជាមួយ cations ដែក (ឬ NH + 4) ផ្តាច់ទាំងស្រុង Na 2 SO 4 "2Na + + SO 2-4 ។
អំបិលអាស៊ីតបំបែកជាជំហាន ៗ
1 ដំណាក់កាល NaHSO 4 « Na + + HSO - 4 ,
2 ដំណាក់កាល HSO - 4 "H + + SO 2-4 ។
កម្រិតនៃការបែកគ្នានៅដំណាក់កាលទី 1 គឺធំជាងដំណាក់កាលទី 2 ហើយអាស៊ីតកាន់តែខ្សោយ កម្រិតនៃការបែកគ្នានៅដំណាក់កាលទី 2 កាន់តែទាប។
អំបិលមូលដ្ឋាន,ទទួលបានដោយការជំនួសមិនពេញលេញនៃអ៊ីយ៉ុង hydroxide ជាមួយនឹងសំណល់អាស៊ីត ក៏បំបែកជាជំហានៗ៖
1 ជំហាន (CuOH) 2 SO 4 "2 CuOH + + SO 2- 4,
2 ដំណាក់កាល CuOH + "Cu 2+ + OH - ។
អំបិលមូលដ្ឋាននៃមូលដ្ឋានខ្សោយបំបែកជាចម្បងនៅក្នុងជំហានទី 1 ។
អំបិលស្មុគស្មាញ,មានអ៊ីយ៉ុងស្មុគ្រស្មាញដែលរក្សាស្ថេរភាពរបស់វានៅពេលរំលាយ បំបែកទៅជាអ៊ីយ៉ុងស្មុគស្មាញ និងអ៊ីយ៉ុងនៃលំហខាងក្រៅ
K 3 « 3K + + 3 - ,
SO 4 "2+ + SO 2 − 4 ។
នៅកណ្តាលអ៊ីយ៉ុងស្មុគស្មាញគឺជាអាតូម - ភ្នាក់ងារស្មុគស្មាញ។ តួនាទីនេះជាធម្មតាត្រូវបានអនុវត្តដោយអ៊ីយ៉ុងដែក។ នៅជិតភ្នាក់ងារស្មុគ្រស្មាញមានទីតាំងនៅ (សំរបសំរួល) ម៉ូលេគុលប៉ូល ឬអ៊ីយ៉ុង ហើយជួនកាលទាំងពីររួមគ្នា ពួកវាត្រូវបានគេហៅថា លីហ្គែន។ភ្នាក់ងារស្មុគ្រស្មាញរួមជាមួយនឹង ligands បង្កើតជាលំហខាងក្នុងនៃស្មុគស្មាញ។ អ៊ីយ៉ុងដែលស្ថិតនៅឆ្ងាយពីភ្នាក់ងារស្មុគ្រស្មាញ ដែលមិនសូវមានទំនាក់ទំនងខ្លាំងជាមួយវា គឺស្ថិតនៅក្នុងបរិយាកាសខាងក្រៅនៃបរិវេណស្មុគស្មាញ។ រង្វង់ខាងក្នុងជាធម្មតាត្រូវបានរុំព័ទ្ធដោយតង្កៀបការ៉េ។ លេខដែលបង្ហាញពីចំនួននៃ ligands នៅក្នុងរង្វង់ខាងក្នុងត្រូវបានគេហៅថា ការសម្របសម្រួល. ចំណងគីមីរវាងអ៊ីយ៉ុងស្មុគ្រស្មាញ និងសាមញ្ញត្រូវបានបំបែកយ៉ាងងាយស្រួលនៅក្នុងដំណើរការនៃការបំបែកអេឡិចត្រូលីត។ ចំណងដែលនាំទៅដល់ការបង្កើតអ៊ីយ៉ុងស្មុគ្រស្មាញត្រូវបានគេហៅថា ចំណងអ្នកទទួលជំនួយ។
អ៊ីយ៉ុងនៃលំហខាងក្រៅងាយបំបែកចេញពីអ៊ីយ៉ុងស្មុគស្មាញ។ ការបែកបាក់នេះត្រូវបានគេហៅថាបឋម។ ការបំបែកផ្នែកខាងក្នុងដែលអាចបញ្ច្រាស់បានគឺពិបាកជាង ហើយត្រូវបានគេហៅថាការបំបែកបន្ទាប់បន្សំ។
Cl " + + Cl - - ការបំបែកបឋម,
+ « Ag + +2 NH 3 - ការបែកគ្នាបន្ទាប់បន្សំ។
ការបែកបាក់បន្ទាប់បន្សំ ដូចជាការបំបែកនៃអេឡិចត្រូលីតខ្សោយ ត្រូវបានកំណត់លក្ខណៈដោយអស្ថិរភាព
ដើម្បីសំបុក។ \u003d × 2 / [ + ] \u003d 6.8 × 10 -8 ។
អស្ថិរភាព (K inst.) នៃអេឡិចត្រូលីតផ្សេងៗ គឺជារង្វាស់នៃស្ថេរភាពនៃស្មុគស្មាញ។ សំបុក K តិច។ ភាពស្មុគស្មាញកាន់តែមានស្ថេរភាព។
ដូច្នេះក្នុងចំណោមប្រភេទដូចគ្នានៃសមាសធាតុ៖
| - | + | + | + |
| K សំបុក \u003d 1.3 × 10 -3 | K nest \u003d 6.8 × 10 -8 | K សំបុក \u003d 1 × 10 -13 | K សំបុក \u003d 1 × 10 -21 |
ស្ថេរភាពនៃស្មុគស្មាញកើនឡើងជាមួយនឹងការផ្លាស់ប្តូរពី - ទៅ + ។
តម្លៃនៃថេរអស្ថិរភាពត្រូវបានផ្តល់ឱ្យនៅក្នុងសៀវភៅយោងស្តីពីគីមីសាស្ត្រ។ ដោយប្រើតម្លៃទាំងនេះ គេអាចទស្សន៍ទាយពីដំណើរនៃប្រតិកម្មរវាងសមាសធាតុស្មុគ្រស្មាញ ជាមួយនឹងភាពខុសគ្នាខ្លាំងនៃអស្ថិរភាព ប្រតិកម្មនឹងឆ្ពោះទៅរកការបង្កើតស្មុគស្មាញដែលមានអស្ថិរភាពទាប។
អំបិលស្មុគស្មាញដែលមានអ៊ីយ៉ុងស្មុគស្មាញមិនស្ថិតស្ថេរត្រូវបានគេហៅថា អំបិលទ្វេដង. អំបិលទ្វេរដង មិនដូចសារធាតុស្មុគស្មាញទេ បំបែកទៅជាអ៊ីយ៉ុងទាំងអស់ដែលបង្កើតសមាសភាពរបស់វា។ ឧទាហរណ៍:
KAl(SO 4) 2 "K + + Al 3+ + 2SO 2- 4,
NH 4 Fe (SO 4) 2 "NH 4 + + Fe 3+ + 2SO 2- 4 ។
ការវាស់វែងកម្រិតនៃការបំបែកនៃអេឡិចត្រូលីតផ្សេងៗបានបង្ហាញថា អេឡិចត្រូលីតនីមួយៗនៅកំហាប់ធម្មតានៃដំណោះស្រាយដូចគ្នាបំបែកទៅជាអ៊ីយ៉ុងខុសគ្នាខ្លាំង។
ភាពខុសគ្នានៃតម្លៃនៃកម្រិតនៃការបំបែកនៃអាស៊ីតគឺអស្ចារ្យជាពិសេស។ ឧទាហរណ៍អាស៊ីតនីទ្រីកនិងអ៊ីដ្រូក្លរីកក្នុង 0.1 N ។ ដំណោះស្រាយស្ទើរតែរលួយទាំងស្រុងទៅជាអ៊ីយ៉ុង; កាបូនិក អ៊ីដ្រូស៊ីយ៉ានិក និងអាស៊ីតផ្សេងទៀត បំបែកនៅក្រោមលក្ខខណ្ឌដូចគ្នាតែក្នុងកម្រិតតូចមួយប៉ុណ្ណោះ។
នៃមូលដ្ឋានរលាយក្នុងទឹក (អាល់កាឡាំង) អាម៉ូញ៉ូមអុកស៊ីតអ៊ីដ្រូសែនត្រូវបានបំបែកយ៉ាងទន់ខ្សោយ អាល់កាឡាំងដែលនៅសល់បំបែកបានល្អ។ អំបិលទាំងអស់ដោយមានករណីលើកលែងមួយចំនួនក៏បំបែកបានយ៉ាងល្អទៅជាអ៊ីយ៉ុងផងដែរ។
ភាពខុសគ្នានៃតម្លៃនៃកម្រិតនៃការបំបែកនៃអាស៊ីតបុគ្គលគឺដោយសារតែធម្មជាតិនៃចំណង valence រវាងអាតូមដែលបង្កើតជាម៉ូលេគុលរបស់វា។ កាលណាប៉ូលកាន់តែច្រើនចំណងរវាងអ៊ីដ្រូសែន និងម៉ូលេគុលដែលនៅសល់ វាកាន់តែងាយស្រួលបំបែក អាស៊ីតនឹងកាន់តែបែក។
អេឡិចត្រូលីតដែលបំបែកបានយ៉ាងល្អទៅជាអ៊ីយ៉ុងត្រូវបានគេហៅថា អេឡិចត្រូលីតខ្លាំង ផ្ទុយទៅនឹងអេឡិចត្រូលីតខ្សោយដែលបង្កើតបានតែអ៊ីយ៉ុងមួយចំនួនតូចនៅក្នុងដំណោះស្រាយ aqueous ។ ដំណោះស្រាយនៃអេឡិចត្រូលីតដ៏រឹងមាំរក្សាបាននូវចរន្តអគ្គិសនីខ្ពស់ ទោះបីជាមានកំហាប់ខ្ពស់ក៏ដោយ។ ផ្ទុយទៅវិញ ចរន្តអគ្គិសនីនៃដំណោះស្រាយនៃអេឡិចត្រូលីតខ្សោយថយចុះយ៉ាងឆាប់រហ័សជាមួយនឹងការកើនឡើងកំហាប់។ អេឡិចត្រូលីតខ្លាំងរួមមានអាស៊ីតដូចជា hydrochloric, nitric, sulfuric និងមួយចំនួនផ្សេងទៀត បន្ទាប់មក alkalis (លើកលែងតែ NH 4 OH) និងអំបិលស្ទើរតែទាំងអស់។
អាស៊ីត Polyoonic និងមូលដ្ឋាន polyacid បំបែកជាជំហានៗ។ ដូច្នេះ ជាឧទាហរណ៍ ម៉ូលេគុលអាស៊ីតស៊ុលហ្វួរីក ជាដំបូងនៃការផ្តាច់ខ្លួនតាមសមីការ
H 2 SO 4 ⇄ H + HSO 4 '
ឬច្បាស់ជាងនេះ៖
H 2 SO 4 + H 2 O ⇄ H 3 O + HSO 4 '
ការលុបបំបាត់អ៊ីយ៉ុងអ៊ីដ្រូសែនទីពីរយោងទៅតាមសមីការ
HSO 4 '⇄ H + SO 4 »
ឬ
HSO 4 '+ H 2 O ⇄ H 3 O + SO 4 "
វាពិបាកជាងនេះទៅទៀត ព្រោះវាត្រូវតែយកឈ្នះលើការទាក់ទាញពីអ៊ីយ៉ុង SO 4 ” ដែលត្រូវបានចោទប្រកាន់ទ្វេដង ដែលជាការពិតណាស់ ទាក់ទាញអ៊ីយ៉ុងអ៊ីដ្រូសែនទៅខ្លួនវាខ្លាំងជាងអ៊ីយ៉ុង HSO 4 'ដែលបានចោទប្រកាន់តែមួយ។ ដូច្នេះដំណាក់កាលទី 2 នៃការបែកគ្នា ឬដូចដែលពួកគេនិយាយថា ការបែកគ្នាបន្ទាប់បន្សំកើតឡើងក្នុងទំហំតូចជាង។ដឺក្រេជាងកម្រិតបឋម ហើយដំណោះស្រាយអាស៊ីតស៊ុលហ្វួរីកធម្មតាមានផ្ទុកអ៊ីយ៉ុង SO 4 តិចតួចប៉ុណ្ណោះ
អាស៊ីតផូស្វ័រ H 3 RO 4 បំបែកជាបីជំហាន៖
H 3 PO 4 ⇄ H + H 2 PO 4 '
H 2 PO 4 ⇄ H + HPO4 »
HPO 4 » ⇄ H + PO 4 »'
ម៉ូលេគុល H 3 RO 4 បំបែកយ៉ាងខ្លាំងទៅជាអ៊ីយ៉ុង H និង H 2 RO 4 ។ អ៊ីយ៉ុង H 2 PO 4 'មានឥរិយាបទដូចជាអាស៊ីតខ្សោយ ហើយបំបែកទៅជា H និង HPO 4 "ក្នុងកម្រិតតិចជាង។ ម្យ៉ាងវិញទៀត អ៊ីយ៉ុង HPO 4 បំបែកជាអាស៊ីតខ្សោយខ្លាំង ហើយស្ទើរតែមិនផ្តល់អ៊ីយ៉ុង H
និង PO បួន "'
មូលដ្ឋានដែលមានក្រុម hydroxyl ច្រើនជាងមួយនៅក្នុងម៉ូលេគុលក៏បំបែកជាជំហានៗផងដែរ។ ឧទាហរណ៍:
វ៉ា(OH) 2 ⇄ BaOH + OH'
VaOH ⇄ វ៉ា + អូ
ចំពោះអំបិល អំបិលធម្មតាតែងតែបំបែកទៅជាអ៊ីយ៉ុងដែក និងសំណល់អាស៊ីត។ ឧទាហរណ៍:
CaCl 2 ⇄ Ca + 2Cl ' Na 2 SO 4 ⇄ 2Na + SO 4 "
អំបិលអាស៊ីត ដូចជាអាស៊ីត polybasic បំបែកជាជំហានៗ។ ឧទាហរណ៍:
NaHCO 3 ⇄ Na + HCO 3 '
HCO 3 '⇄ H + CO 3 »
ទោះជាយ៉ាងណាក៏ដោយដំណាក់កាលទីពីរគឺតូចណាស់ដូច្នេះដំណោះស្រាយអំបិលអាស៊ីតមានអ៊ីយ៉ុងអ៊ីដ្រូសែនតិចតួចប៉ុណ្ណោះ។
អំបិលមូលដ្ឋានបំបែកទៅជាអ៊ីយ៉ុងនៃសំណល់អាស៊ីត និងមូលដ្ឋាន។ ឧទាហរណ៍:
Fe(OH)Cl 2 ⇄ FeOH + 2Cl"
ការបំបែកបន្ទាប់បន្សំនៃអ៊ីយ៉ុងនៃសំណល់សំខាន់ៗចូលទៅក្នុងលោហៈ និងអ៊ីយ៉ុងអ៊ីដ្រូស៊ីល ស្ទើរតែមិនកើតឡើងទេ។
នៅក្នុងតារាង។ 11 បង្ហាញតម្លៃលេខនៃកម្រិតនៃការបំបែកនៃអាស៊ីត មូលដ្ឋាន និងអំបិលមួយចំនួនក្នុង 0 , 1 ន. ដំណោះស្រាយ។
ថយចុះជាមួយនឹងការបង្កើនការផ្តោតអារម្មណ៍។ ដូច្នេះនៅក្នុងដំណោះស្រាយដែលប្រមូលផ្តុំខ្លាំង សូម្បីតែអាស៊ីតខ្លាំងក៏ត្រូវបានបំបែកដោយទំនាក់ទំនងខ្សោយដែរ។ សម្រាប់
តារាង 11
អាស៊ីត មូលដ្ឋាន និងអំបិលក្នុង 0.1 N.ដំណោះស្រាយនៅ 18 °
| អេឡិចត្រូលីត | រូបមន្ត | កម្រិតនៃការបែកបាក់ក្នុង % |
| អាស៊ីត | ||
| អំបិល | HCl | 92 |
| អ៊ីដ្រូប្រូមិច | HBr | 92 |
| អ៊ីដ្រូអ៊ីយ៉ូត | HJ | . 92 |
| អាសូត | HNO3 | 92 |
| ស្ពាន់ធ័រ | ហ 2 SO 4 | 58 |
| ស្ពាន់ធ័រ | ហ 2 SO 3 | 34 |
| ផូស្វ័រ | ហ 3 PO 4 | 27 |
| អ៊ីដ្រូហ្វ្លុយអូរី | អេហ្វអេហ្វ | 8,5 |
| អាសេទិក | CH3COOH | 1,3 |
| ធ្យូងថ្ម | H2 ឧស្ម័នកាបូនិក | 0,17 |
| Sulfide អ៊ីដ្រូសែន | H 2 S | 0,07 |
| អ៊ីដ្រូស៊ីយ៉ានិក | HCN | 0,01 |
| បូណាយ៉ា | ហ ៣ បូ ៣ | 0,01 |
| មូលនិធិ | ||
| បារីយ៉ូមអ៊ីដ្រូសែន | បា (OH) ២ | 92 |
| ប៉ូតាស្យូម caustic | con | 89 |
| សូដ្យូមអ៊ីដ្រូសែន | ណាអូន | 84 |
| អាម៉ូញ៉ូមអ៊ីដ្រូសែន | NH4OH | 1,3 |
| អំបិល | ||
| ក្លរ | KCl | 86 |
| អាម៉ូញ៉ូមក្លរីត | NH4Cl | 85 |
| ក្លរ | NaCl | 84 |
| នីត្រាត | KNO ៣ | 83 |
| AgNO3 | 81 | |
| អាស៊ីតអាសេទិច | NaCH 3 COO | 79 |
| ក្លរ | ZnCl ២ | 73 |
| ស៊ុលហ្វាត | ណា ២ SO ៤ | 69 |
| ស៊ុលហ្វាត | ZnSO4 | 40 |
| ស៊ុលហ្វាត |








